查看完整版本请点击这里:
【求助】关于Western Blot的几个问题
最近在做western,发现不少问题,想请大家指点一下!【求助】关于Western Blot的几个问题
1 制备积层胶时,拔梳子的时候,总会有一些零碎的胶清除不干净,对加样影响比较大,大家有没有什么好的办法?
2 加一抗之前我采用了5%BSA室温封闭1小时,一抗二抗也是用5%BSA进行稀释的,做出来的结果为什么背景还那么深呢?有没有什么好的办法?
3 市场上卖的完达山脱脂奶粉(1.5%fat),有没有哪位站友用过,封闭效果怎么样?
4 稀释一抗、二抗用多大浓度的BSA结果比较好,可不可以也用含脱脂奶粉的TTBS稀释呢?
这些问题有点低级,大家不要笑话我哦!
查看完整版本请点击这里:
【求助】关于Western Blot的几个问题
【求助】关于Western Blot的几个问题
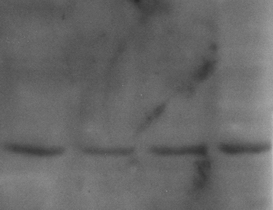
56350562.jpg



最新回复
orangecake (2013-10-12 13:26:17)
1,我是这样做胶的,供你参考。在分离胶聚合完全之后,先用去离子水冲净分离胶顶部未聚合的丙稀酰胺。再尽可能排去分离胶上的液体,可用吸水纸吸干。然后插入齿状梳,灌入配好的积层胶,室温30min后,积层胶就可聚合完全。之后将胶放入电泳槽中,先下槽再上槽缓慢倒入电泳buffer。接着即可拔去齿状梳,记住一定要用双手拔,两手用力均匀一致,而且动作要缓慢;如此这样,就不会出现问题;
2,封闭时间有些短,室温2h;或者4度过夜效果最佳。5%BSA的浓度已经足够,我一般只用1%,用TBST配制;背景深的原因也有很多,不过你试着降低一抗以及二抗的稀释浓度,效果会很明显;
3,做磷酸化的WB最好都要用BSA来封闭,不能用普通的脱脂奶粉,因为奶粉中也存在磷酸化的蛋白。但普通的脱脂奶粉是可以用来做非磷酸化的WB的,我见过有人用过,效果也可以;
4,既然你要用BSA来封闭,那么就不要用脱脂奶粉,两者不能互相代替。我做实验的经验是:稀释一抗、二抗用1%-5%均可,就看你自己条件摸索如何了。
祝你顺利
iii_ii (2013-10-12 13:26:52)
1 我每次拔梳子的时候,都会发现上样孔里面有好多气泡,我一般都是用去离子水冲去气泡的,按照你的做法的话,加了电泳buffer以后拔梳子,上样孔里面的气泡怎么办啊,还是不管它?
2 我发现老外发的文章里面,好多做磷酸化蛋白的都用的是脱脂奶粉,所以我也想用脱脂奶粉,毕竟5%BSA做起来不太经济,呵呵!
xue258 (2013-10-12 13:27:13)
我以前也遇到这种问题,你可以尝试下面的方法:
1.可以用细的针头,比如针灸的细针进行排出上样孔的气泡,效果很好,只是稍微麻烦一些。
2.用脱脂奶粉也可以,我稀释一抗和二抗都是用TBST配制的5%脱脂奶粉封闭液,关键要注意奶粉要完全溶解,我觉得溶解后进行过滤处理。
3.对背景的处理,主要是封闭要充分,同时一抗和二抗的浓度太高也会引起背景深。
一点经验,仅供参考 !!
祝你实验顺利!!
zhenxin (2013-10-12 13:27:34)
1,“加了电泳buffer以后拔梳子”,上样孔不会出现气泡的,你可以想象:当电泳buffer进入上样孔之后,上样孔里面充满液体,怎么肯会有气泡?
2,我也看过国外做磷酸化用脱脂奶粉(non-fat milk)的,但这种奶粉和咱们国内的普通脱脂奶粉应该不是一样的吧,呵呵,原因你应该明白。国内的文献我也看,一般做磷酸化的国内还是最常用BSA的。如果你嫌5%不划算,你就试试1%的吧。
iii_ii (2013-10-12 13:28:11)
还想问一个问题,我做的是35~40KD的蛋白,分离胶选择8%SDS可行吗?
8princess8 (2013-10-12 13:28:51)
用5%的脱脂奶粉封闭和一抗二抗稀释很不错的, 封闭可以适当延长一些, 二抗不可以太长,否则背景太深影响.
mysmdbl (2013-10-12 13:29:13)
iii_ii (2013-10-12 13:30:14)
我想同时做38KD和65KD的蛋白,电转膜时用恒流还是恒压好呢?转膜后将膜自中间剪开,可以吗?
谢谢各位了!
pengke1983 (2013-10-12 13:30:32)
我也要做western blot ,以后又不懂得我也来请教大家
idea2011 (2013-10-12 13:31:07)
一般二抗孵育时间是多少?我在室温下温孵了2个小时,结果背景很高。降低一抗二抗的稀释度,目标条带也看不到了。
pencil菲 (2013-10-12 13:31:34)
我想同时做38KD和65KD的蛋白,电转膜时用恒流还是恒压好呢?转膜后将膜自中间剪开,可以吗?
谢谢各位了!
===========================================================================================================
我不知道你选择什么样的电泳系统,一般电泳用恒压,积层胶电压为80u,分离胶为120-130u;
转膜用恒流,可以0.8mA/cm2,转膜时间2-3h。转完膜当然可以将膜剪开了,但不要忘记标好marker条带位置;之后封闭,接着你可以用不同的一抗来温育杂交。
pencil菲 (2013-10-12 13:31:52)
================================================================
一般二抗孵育1h即可。不要将一抗二抗稀释的梯度降得太大,梯度可以降500个点试试。
iii_ii (2013-10-12 13:32:50)
谢谢各位!
idea2011 (2013-10-12 13:33:22)
QUOTE:
在转完膜丽春红染色之后,我一般都是沿着泳道即与泳道平行的方向剪膜,而你所说的意思给我感觉是与泳道垂直的方向剪,我觉得这样可能会破坏膜上的蛋白。你可以在上样时多做几个平行孔,丽春红染色后,在膜上做好marker条带标记,然后沿着泳道方向剪膜。
iii_ii (2013-10-12 13:33:48)
楼上所说的“与泳道垂直的方向剪,我觉得这样可能会破坏膜上的蛋白”,我不是很明白,我觉得我从47KD的位置剪膜应该对38KD和68KD的蛋白没有影响吧?望指点
还有,我今天转膜时用的10V恒压,电流大概在170mA的样子(胶厚度0.75mm,Roche的PVDF膜),大家觉得一般要转多长时间比较合适啊?
jujuba (2013-10-12 13:34:20)
1.与泳道垂直的方向剪,不会破坏膜上的蛋白,对你的实验没有影响。
2.对于38KD和68KD的蛋白进行转膜,我的经验是恒流,180mA,时间在70min 左右比较好。
3.关于胶的浓度,10%的胶比较合适。
仅供参考!!
iii_ii (2013-10-12 13:35:09)
cocacola (2013-10-12 13:35:31)
我用的是恒压20V转了45分钟,间隙了15分钟,又恒压转了45分钟,可我转的效率很低,样品的带钱,请高手不吝赐教!
iii_ii (2013-10-12 13:36:25)
今天的实验结果证实,转膜效率比较低,条件需要改进。
请站友们帮我看一下,65KD和38KD大概在什么位置?
86568947.jpg
tie8 (2013-10-12 13:36:52)
祝你好运!!
【求助】关于Western Blot的几个问题