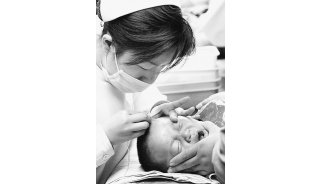
疫苗安全之道
药物警戒数据和信息的积累,对于疫苗后续的研发和改进也有重要的

9月11日,一对双胞胎在安徽省淮北市卫生疾控中心接种麻疹疫苗。
一亿剂麻疹疫苗绞杀麻疹,规模之大世界范围内也少有。一时间各种质疑声四起。“麻疹强化疫苗是国外的生物武器,千万不能给小孩接种。”“免费接种的疫苗肯定没有质量的保证,还是不打为好。”
负责此次免疫接种规划的中国疾病预防控制中心免疫规划中心主任梁晓峰面对这些没常识的质疑哭笑不得。梁晓峰表示,麻疹疫苗用了几十年被证明是安全有效的。“和太平洋地区其他国家相比,中国的麻疹发病率较高,而且中国也承诺在2012年消除麻疹。从根本上说,麻疹强化免疫是很正常的,世界上其他一些国家也是通过这种手段消除了麻疹”。
从“山西疫苗致残”到“江苏假狂犬疫苗”再到麻疹疫苗遭遇的质疑,疫苗安全一次又一次挑战人们的心理承受能力,让大众对疫苗产生了恐惧心理。
用在健康人身上的疫苗由于其使用的广泛性,对于疫苗的安全性要求非常高。有上百年疫苗研发经验的赛诺菲巴斯德公司专家说:“在进行疫苗研发时,赛诺菲巴斯德认为疫苗的安全性往往比有效性更加重要。如果疫苗的安全性存在问题,即使有效性很好的候选疫苗也会被淘汰或者进一步改进以提高其安全性。”
在临床前研发阶段,赛诺菲巴斯德会进行多种专门的试验和测试,以评估疫苗的安全性;而在临床试验阶段,应用科学的试验设计,规范的操作执行,翔实的结果记录,合理的统计分析以及试验的全程过程控制来确保临床试验的安全性评价结果科学可信。
在赛诺菲巴斯德的疫苗生产过程中,70%的时间用于质量控制。“只有通过细致全面的工作,才能确保疫苗的质量,尽量降低因疫苗设计和质量引发的安全性风险。”赛诺菲巴斯德研发人员如是说。
公司研发人员进一步解释,“对于赛诺菲巴斯德来说,疫苗的上市并不意味着这种疫苗研发的终止。在疫苗上市后,公司要做大量的疫苗上市后评价研究,同时公司研发部门也会继续对现有疫苗进行改进,包括在疫苗的组分、剂量、剂型、佐剂、联合疫苗、生产工艺、给药方式、接种途径等各方面开展研究。”
中国的疫苗监管有两个部门负责,在流通领域由药监局监管,而接种则由卫生部负责监督。政府颁布的《疫苗流通和预防接种管理条例》以及《药品不良反应报告和监测管理办法》要求药品生产、经营企业和医疗卫生机构对于预防接种过程中发现的可疑病例及时报告。
赛诺菲巴斯德公司在这方面走在了同行业的前面。
关于疫苗使用后的不良事件监测,赛诺菲巴斯德公司建立了全球完备的上市后不良反应监测报告系统。它在法国、加拿大、美国设有3个疫苗安全监测平台,随时为各国的疫苗不良反应工作者提供相关案例检索,因果评价分析和医学技术支持。
在中国,赛诺菲巴斯德设有不良反应处理小组和免费热线电话,以解决客户和患者有关不良反应的问题。
此外,赛诺菲巴斯德还将上一年度或前五年度的药品不良反应/事件,定期汇总并填写《药品不良反应/事件定期汇总表》,上报国家药品不良反应监测中心。
“药物警戒数据和信息的积累对于疫苗后续的研发和改进也有重要的科学意义,”赛诺菲巴斯德公司的相关负责人说。
当然,要消除中国公众对于疫苗安全性的恐惧和疑虑,需要相关各方面的协作配合,生产企业要提高产品的质量和售后监测与服务,药监部门进行行业监管,疫苗的接种部门加强管理,疫苗受种者提高科学认识,等等。
梁晓峰表示,即便质量控制完全合格,监管完备的疫苗,也会出现极少量的不良反应,这是药品管理法规和国际卫生组织允许的正常情况,国家也对此建立了补偿机制。但是,由于一些公众的不信任和个别媒体的不当报道,极低几率的疫苗事故有时会被放大成严重的公共卫生事件,“这给我们的工作带来了很大的压力。”他告诉《科学新闻》。
要推进疫苗的安全使用,促进公众的免疫接种,除了企业和政府部门外,媒体和社会其他组织也要积极行动。“这是大家的事,每个人都有责任。”梁晓峰说。
-
实验室动态

-
焦点事件