复旦管坤良、袁海心等JBC癌症新成果
血栓素A2受体(TP)已知参与血管损伤后的再狭窄,这会导致血管平滑肌细胞(VSMC)迁移和扩散。然而,这一过程的根本机制还是未知的。7月5 日,复旦大学、加州大学圣地亚哥分校、中科院上海生命科学研究院和北卡罗来纳大学教堂山分校的研究人员,在国际学术期刊《Journal of Biological Chemistry》发表一项研究指出,血栓素A2信号可激活YAP/TAZ蛋白来促进VSMCs迁移和增殖,从而表明VSMCs可作为心血管疾病的一个潜在治疗靶点。任职于复旦大学及加州大学圣地亚哥分校的管坤良(Kun-Liang Guan)、复旦大学生物医学研究院的青年研究员袁海心(Hai-Xin Yuan)博士以及熊跃博士,是本文共同通讯作者,点击阅读该研究小组的近期成果:管坤良教授Cancer Cell亮点推荐癌症新成果;复旦管坤良、袁海心亮点推荐Science文章:聚焦mTORC1;管坤良教授Genes&Dev点评重要致癌通路。
血栓素A2(TxA2)是在许多细胞/组织中产生的,特别是血小板,并对于血小板激活、血 管损伤积聚以及动脉粥状硬化,起着重要的作用。在动脉粥样硬化患者或接受经皮冠状血管成形术(一种非手术程序,用于治疗在心血管疾病中的冠状动脉狭窄)的 患者中,TxA2的浓度明显增加。类似的现象也出现在相应的小鼠模型中。TxA2和血栓素A2受体(TP)被认为可导致血管损伤后的再狭窄,虽然药物洗脱 支架可以减少再狭窄的风险,但这仍然是一个挑战性的临床问题。
TxA2是一种前列腺素,是环氧酶产生的一个脂质介质家族。TxA2不太稳定,半衰期约几秒,可非酶促地降解成生物失活形式的血栓素 B2(TxB2)。TxA2通过其同源TP受体——一个G蛋白耦合受体(GPCR),来发挥其生物学活性。TP在人类中被表达为两个亚型——TPα和 TPβ。除了TxA2之外,前列腺素H2、异前列素和羟基二十碳四烯酸也可以激活TP受体。
除了血小板激活之外,TxA2或TP受体已知也促进细胞迁移和血管平滑肌细胞(VSMCs)的增殖,这个重要的过程与大量的血管疾病有关,例如血管 成形术后的再狭窄、动脉粥样硬化等。VSMCs对血管损伤的增殖反应,在过表达人类TPα受体的转基因小鼠中是明显增大的,这可以通过TP特异性拮抗剂 S18886而得以抑制。此外,创伤性血管增殖和血小板活化在TP受体缺陷型小鼠中是被抑制的。在动脉粥样硬化小鼠模型中,药物对抗和TP受体缺失可延缓 病变的发展。综上所述,这些先前的研究结果表明,TxA2和TP受体有助于VSMCs介导的血管疾病,但是分子机制在很大程度上是未知的。
Hippo信号通路对于器官大小和组织稳态的调控,起着关键的作用。哺乳动物Hippo通 路的核心组件包括MST1/2及其接头蛋白SAV1、LATS1/2及其接头蛋白MOB1A/1B、两个下游转录效应因子YAP/TAZ。MST1/2磷 酸化和激活LATS1/2激酶,进而磷酸化和抑制YAP/TAZ。最近,MAP4Ks被确定为Hippo通路的一个核心组件,与MST1/2共同磷酸化和 激活LATS1/2。S127上的YAP磷酸化可导致细胞质隔离。
去磷酸化的YAP/TAZ易位到细胞核中,并与TEAD家族转录因子相互作用,而诱导靶基因,例如CTGF和CYR61,从而促进细胞增殖、迁移和 生存。Hippo通路的放松管制在各种人类癌症中都被观察到过,并经常与预后不良有关。Hippo通路的上游信号一直都是难以捉摸的,有研究证 实,GPCRs可将细胞外信号传递到Hippo通路。
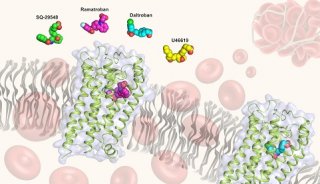
在这项研究中,研究人员报道称,TP信号可通过激活YAP/TAZ——Hippo信号通路的两大下游效应物,诱导VSMC迁移和扩散。TP特定受体 激动剂I-BOP和U -46619可在多个细胞系中诱导YAP /TAZ激活,包括VSMCs。通过I-BOP诱导的YAP /TAZ激活,可通过敲除受体TP或下游G蛋白Gα12/14而被阻断。
此外,Rho抑制或肌动蛋白细胞骨架破坏,可防止I-BOP诱导的YAP /TAZ激活。重要的是,在VSMCs中,TP激活可以一种依赖于YAP/TAZ的方式,促进DNA合成和细胞迁移。综上所述,血栓素A2信号可激活 YAP /TAZ以促进VSMCs迁移和增殖,从而表明YAP /TAZ可作为心血管疾病的一个潜在治疗靶点。
-
项目成果