高绍荣、王晓群Nature子刊发布表观遗传研究新成果
来自同济大学生命科学与技术学院、中科院生物物理研究所的研究人员证实,在发育小鼠大脑中LSD1共抑制因子Rcor2协调了神经发生。这一研究发现发布在1月22日的《自然通讯》(Nature Communications)杂志上。
同济大学生命科学与技术学院的高绍荣(Shaorong Gao)教授,与中科院生物物理研究所的王晓群(Xiaoqun Wang)研究员是这篇论文的共同通讯作者。
神经干细胞(NSC)是一类具有多分化潜力(能分化为神经细胞、星形胶质细胞、少突胶质细胞),能自我更新的细胞。具有以下的特点:(1)在整个生命过程中能够自我维持和自我更新。(2)能自我复制。(3)能够通过扩增得到大量的后代。(4)具有多分化潜能。
大量的研究表明,NSC的分化和细胞命运特化受到一系列内外部信号的调控。尽管目前尚未充分认识NSCs的区域限制和命运决定机制,很显然,通过DNA甲基化、组蛋白修饰和非编码RNA表达,内部的表观遗传调控与这些机制密切相关。
赖氨酸特异性组蛋白去甲基化酶LSD1,也称作为KDM1A,是一个黄素腺嘌呤二核苷酸(FAD)依赖性胺氧化酶,它能够特异性脱去单甲基化和二甲基化组蛋白H3第4位赖氨酸(H3K4)和H3K9位点上的甲基基团。LSD1可与一些转录共抑制因子,包括Rcor1 (CoREST)、BHC80、HDAC1/2、CtBP、BRAF35和几种锌指蛋白形成各种蛋白质复合物。
作为第一个鉴别出来的RCOR蛋白,科学家们在各种细胞类型中对Rcor1进行了广泛地研究,证实其通过改变染色质构型在小鼠红细胞生成及神经元或突触基因调控中起重要作用。与Rcor1具有70%的序列相似性,Rcor2可与LSD1形成一种蛋白质复合物,在胚胎干细胞(ESCs)中促进它对核小体的去甲基化酶活性。此外,有研究还发现Rcor2可作为Sox2替代物调控ESC增殖并促进诱导多能干细胞形成。但目前尚不清楚在体内Rcor2在发育过程中所起的作用。
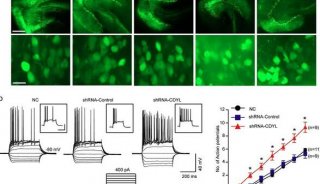
在这篇新文章中研究人员证实,LSD1共抑制因子Rcor2主要表达于中枢神经系统(CNS)中,在表观遗传调控皮质发育中起重要作用。耗尽 Rcor2可导致NPC增殖、神经元群、新皮质厚度和大脑尺寸均相应减小。他们发现发育新皮质中Rcor2直接靶向Dlx2和Shh,抑制了它们的表达。此外,在体内外抑制Shh信号均可挽救Rcor2耗尽所导致的神经发生缺陷。
因此,这些研究结果表明了共抑制因子Rcor2通过在端脑背侧抑制Shh信号通路对皮质发育起至关重要的作用。
-
精英视角

-
科技前沿

-
科技前沿

-
焦点事件

-
项目成果
-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
科技前沿
-
焦点事件

-
企业风采

-
科技前沿

-
科技前沿
-
科技前沿

-
科技前沿

-
项目成果
-
科技前沿

-
科技前沿

-
科技前沿

-
科技前沿
-
科技前沿
-
技术原理
-
焦点事件

-
项目成果
-
项目成果
-
项目成果

-
项目成果

-
项目成果

-
科技前沿

-
项目成果
-
项目成果

-
项目成果
-
项目成果
-
项目成果
-
项目成果
-
项目成果
-
项目成果
-
会议会展

-
焦点事件

-
项目成果
-
项目成果
-
焦点事件

-
焦点事件
-
焦点事件
-
焦点事件
-
焦点事件

-
焦点事件
-
项目成果