Biotechniques盘点癌症中的microRNA
microRNA是癌症个性化医疗的希望,人们一直希望能够解析它们的确切作用机理,并将其应用于临床。然而事实证明,这是一项充满挑战性的工作。
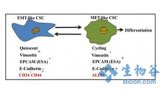
MicroRNA是可以沉默基因表达的非编码单链短RNA分子。尽管越来越多的证据表明,microRNA在癌症中的作用很重要,但人们依然对其知之甚少。康奈尔大学的系统生物学家Xiling Shen利用免疫荧光和RNA荧光原位杂交,在结肠癌干细胞CCSC的分裂早期进行研究。他发现一种肿瘤抑制microRNA(miR-34a),能够决定癌症干细胞是进行自我更新还是开始分化。研究显示,高水平miR-34a会减少Notch信号,促进细胞分化;而低水平miR-34a会增加Notch信号,使细胞保持干细胞状态。
研究人员指出,miR-34a作为决定细胞命运的开关,进行全或无(all-or-nothing)式选择,要么进行自我更新要么启动细胞分化。与此相反的是,Numb蛋白对Notch水平的调控,是一种连续的梯度模式。研究显示,与Numb蛋白相比,miR-34a对细胞命运的影响更强。
“我们原本以为microRNA是起微调作用的,” Shen说。“但miR-34a是主导性的,蛋白的作用反而较小,这一发现与传统观点背道而驰。”
五花八门的机制
另一项发表在Nature杂志上的研究指出,microRNA主要作为mRNA–mRNA互作的微调器,而不是on/off分子开关。剑桥大学的Carlos Caldas通过高通量测序和芯片分析,在大量人类乳腺癌肿瘤中,研究了microRNA和mRNA的表达。研究指出,在全基因组水平上,microRNA的作用主要是影响mRNA之间的互作。
这些研究的结论看起来互相矛盾,实际上却反映了microRNA作用机制的共存,H. Lee Moffitt癌症中心的Jin Cheng说。“人们发现microRNA有多种作用模式,例如一些microRNA阻止翻译,而另一些促使mRNA降解。”
在决定细胞命运时(例如细胞分化或者程序性细胞死亡),microRNA起到了分子开关的作用。但在一些更微妙的过程(例如代谢)中,microRNA也可以进行微调。有时同一种microRNA可能兼具上述两种作用形式。这是因为,microRNA作用于许多不同的mRNA靶标,可以灵活地行使功能,它们的作用机制可能更多的取决于其靶标。举例来说,如果microRNA的靶标具有多个结合位点,它的影响就更强烈。
2011年Nature Genetics杂志上的一篇文章,为上述观点提供了支持。麻省理工的Alexander van Oudenaarden利用定量荧光成像和流式细胞仪,研究了单个细胞中microRNA对基因表达的影响。他发现,不同细胞中的microRNA作用差异较大。研究指出,microRNA既有开关作用又可以进行微调,其影响力取决于它与靶标的相互作用情况。
总的来说,不同的microRNA实验出现了差异化的结果。“我们通常研究的是大量细胞的平均情况,”OSU的Stefano Volinia说。“为了提高结果的可靠性,我们应该尽量提高microRNA检测的通量和精度。肿瘤含有多种细胞类型,除了癌细胞以外,还有正常的间质细胞和免疫细胞。”
路漫漫其修远兮
OSU 的Volinia及其同事Carlo Croce,将microRNA研究成果推向了临床。他们在美国国家科学院院刊PNAS杂志上发表文章指出,Cancer Genome Atlas中的mRNA、microRNA和DNA甲基化二代测序数据,可以帮助人们预测常见乳腺癌(乳腺浸润性导管癌)患者的预后情况。与其他RNA指标相比,这样的综合指标能够更好地把低风险患者与高风险患者分开。
“研究显示,综合型指标的预测能力最强,”Volinia说。“我们现在使用的新技术,能够同时检测样本中的microRNA和mRNA。这样的测试可以帮助医生根据患者情况选择适当的治疗方式,实现个性化的医疗。”
研究显示,这些指标对于缺乏有效治疗的侵袭性癌症更有帮助,例如三阴性乳腺癌TNBC。TNBC患者体内缺乏雌性激素、孕酮和HER2/neu受体,无法应答以这些受体为靶标的药物。而分子指标可以帮助临床医生将TNBC分成不同的亚型,以制定更加个性化的治疗方案。
“我从蛋白角度对乳腺癌进行了长期的研究,”OSU综合癌症中心的Kay Huebner说。“我认为在乳腺癌分级方面,microRNA比其他方法更好。”Huebner与Pierluigi Gasparini在PLoS ONE上发表文章,通过分析microRNA和mRNA的表达谱,鉴定了四种TNBC分子亚型。研究指出,microRNA和mRNA表法谱不同的患者,可以受益于不同类型的药物,拥有高风险指标的患者适合更为强力的治疗。他们还发现miR-155可以预测所有患者的生存情况。
此前,曾有研究指出miR-155与癌细胞的生长和细胞生存有关。例如,Cheng和同事在Oncogene上发表文章指出,miR-155在乳腺癌中促进新血管的生长,与预后差、癌转移和三阴性肿瘤有关。“miR-155是乳腺癌转移的关键因子,”Cheng说。“我们的研究表明,miR-155可以作为治疗靶标,帮助人们治疗乳腺癌。”
不过Volinia的研究显示,虽然miR-155的确在乳腺癌中过表达(尤其是TNBC),但它与患者的预后似乎并无联系。这些相互冲突的结论,体现了microRNA功能的复杂性。“要完全了解某个microRNA是一个非常漫长的过程,”Huebner说。
参考文献:
1. Bu, P., K.Y. Chen, J.H. Chen, L. Wang, J. Walters, Y.J. Shin, J.P. Goerger, J. Sun, M. Witherspoon, N. Rakhilin, et al. 2013. A microRNA miR-34a-regulated bimodal switch targets Notch in colon cancer stem cells. Cell Stem Cell. 12(5):602-15. doi: 10.1016/j.stem.2013.03.002.
2. Dvinge, H., A. Git, S. Gräf, M. Salmon-Divon, C. Curtis, A. Sottoriva, Y. Zhao, M. Hirst, J. Armisen, E.A. Miska, et al. 2013. The shaping and functional consequences of the microRNA landscape in breast cancer. Nature. 497(7449):378-82. doi: 10.1038/nature12108.
3. Mukherji, S., M.S. Ebert, G.X. Zheng, J.S. Tsang, P.A. Sharp, and A. van Oudenaarden. 2011. MicroRNAs can generate thresholds in target gene expression. Nat Genet 43(9):854-9. doi: 10.1038/ng.905.
4. Volinia, S., and C.M. Croce. 2013. Prognostic microRNA/mRNA signature from the integrated analysis of patients with invasive breast cancer. Proc Natl Acad Sci U S A. 110(18):7413-7. doi: 10.1073/pnas.1304977110.
5. Cascione, L., P. Gasparini, F. Lovat, S. Carasi, A. Pulvirenti, A. Ferro, H. Alder, G. He, A. Vecchione, C.M. Croce, C.L. Shapiro, and K. Huebner. 2013. Integrated microRNA and mRNA signatures associated with survival in triple negative breast cancer. PLoS One. 8(2):e55910. doi: 10.1371/journal.pone.0055910.
6. Kong, W., L. He, E.J. Richards, S. Challa, C.X. Xu, J. Permuth-Wey, J.M. Lancaster, D. Coppola, T.A. Sellers, J.Y. Djeu, and J.Q. Cheng. 2013. Upregulation of miRNA-155 promotes tumour angiogenesis by targeting VHL and is associated with poor prognosis and triple-negative breast cancer. Oncogene. doi: 10.1038/onc.2012.636.
-
焦点事件
-
焦点事件
-
焦点事件

-
焦点事件

-
焦点事件













