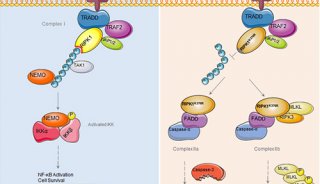
Nature:细胞坏死的新谜题
生物通报道:细胞死亡是所有多细胞生物体必需的基本生理过程。在机体一生当中,许多组织中的细胞都会发生自然死亡,新的细胞替换。细胞死亡和新细胞生成之间的适当平衡是维系健康组织功能,机体损伤后修复的关键所在。如果细胞只增加不减少,那么就会导致肿瘤发展。另一方面,过多的细胞死亡也会导致组织损伤和疾病。
正常来说我们的组织都是健康的,但是其中一些会发生炎症和疾病,“是什么引发炎症的呢?细胞程序性坏死(necroptosis)是否是炎症的开关,这种进程如何调控的呢?”德国科隆大学遗传学研究所教授Manolis Pasparakis说。Pasparakis教授研究组11月7日在Nature杂志上发表文章,部分回答了这些问题。
目前公认的主要细胞死亡类型有三种,第一种是“坏死”,第二种是“凋亡”,第三种是“自噬”。凋亡和自噬均需要能量和合成新的蛋白质,是一个细胞自我调控的主动过程,因此也被称为“程序性死亡”。
细胞坏死最初被认为是一类因病理而产生的被动死亡,这些细胞的膜通透性增高,致使细胞肿胀,细胞器变形或肿大,最后细胞破裂。因此被认为是无序的过程,无从进行调控,但是RIP1和RIP3调控研究改变了这种误解,在2005年,这种与死亡受体配基相关的程序性坏死被命名为“necroptosis”。
Pasparakis教授研究组构建了特殊皮肤细胞:角蛋白细胞(keratinocytes)中RIPK1基因缺失的小鼠,本来他们以为由于RIPK1 缺乏,细胞不会发生程序性坏死,但是结果研究人员得到了相反的结果:这些小鼠中的角蛋白细胞出现细胞坏死而死亡,引发了皮肤炎症。
这就提出了一个问题:为何缺失 RIPK1 也会导致程序性坏死?
通过进一步分析,研究人员发现了答案,由于 RIPK1 会抑制另外一种程序性坏死诱导因子: ZBP1 蛋白,遗传去除ZBP1能抑制RIPK1缺失引发的程序性坏死和炎症。
“我们知道,ZBP1是一种DNA传感蛋白,参与对抗某些病毒的免疫系统,但是至今还未发现它在炎症中的作用,”文章作者之一Chun Kim说。
那么 RIPK1是如何抑制 ZBP1的呢?
为了回答这个问题,研究人员利用CRISPR 基因编辑修改了 RHIM结构域中的3个氨基酸,这种结构域是RIPK1与另外两个调控程序性坏死的蛋白之间相互作用的关键结构。小鼠如果在所有细胞中都表达这种突变的RIPK1,那么出生后就会无法生存。不过只在角蛋白细胞中表达就只会引发皮肤炎症。
研究人员发现当RIPK1中PHIM结构域突变时,ZBP1会开启程序性死亡,引发围产期死亡和成鼠皮肤炎症。“这个一个令人惊讶的结果,RIPK1这三种氨基酸能阻止ZBP1诱导坏死,而这也是小鼠生存,防止皮肤炎症的关键所在,”文章作者之一林娟(Juan Lin,音译)说。
“我们解开了一些谜题,但是还有更大的谜题尚不清楚,”Pasparakis说,“ZBP1 作为病毒传感器,现在我们的研究将其与炎症和死亡联系在一起。在大多数情况下,人体内慢性炎症依然是个谜,为何某些情况下某些人体内炎症会发生呢?我们这项研究发现了ZBP1的重要作用,现在令我们疑惑的是病毒或者细菌是否能激活ZBP1,引发炎症?”
下一步研究人员将探索 ZBP1与炎症在人体内的进一步关联。
-
科技前沿
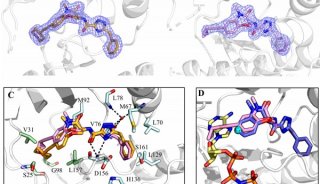
-
项目成果