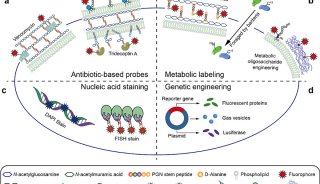
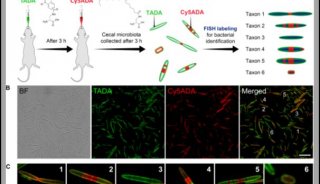
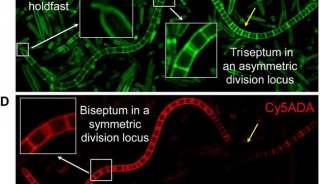
Nature等五篇文章直指肠道细菌特殊的代谢途径
来自UT西南医学中心,MD安德森癌症中心等多处的多个研究小组2018年开年陆续发表了五篇论文,分别论述了肠道细菌特殊的代谢途径,以及这种途径在多个疾病中的重要作用。相关成果分别发表在Nature,Science,以及Cell Host & Microbe杂志上。
肠道菌群与肠道疾病
Nature文章作者,UT西南医学中心的Sebastian Winter博士表示,精确编辑肠道细菌群来预防或减轻结肠炎,这一研究策略不仅被证明能有效减少小鼠结肠炎模型中的炎症,而且在对照组(健康,平衡的细菌群小鼠)中没有出现明显的变化。
“我们的研究结果为精确改变细菌群,从而有效减少与结肠炎和其他形式的炎症性肠病(IBD)有关的失控细菌增殖炎症提出了一个概念框架。”
美丽花园中需要许多种植物,同样在我们肠道上也有许多种微生物群体,它们被称为肠道菌群,这些细菌对人类健康至关重要,可以帮助消化,驯化免疫系统,抵御感染等。然而,当微生物群失去平衡时,这些本来有益的细菌就会变成了一种负担,就像花园中出现了侵入性的园艺植物,产生了竞争物种。
了解肠道菌群微生物学的一大阻碍就是其广泛的多样性。在人体肠道中发现了数百种不同的细菌,并且个体之间的肠道菌群组成的差别也非常大。
许多人类疾病,比如慢性终身炎症性疾病IBD,Crohn病和溃疡性结肠炎(ulcerative colitis)的患者体内都会出现肠道菌群的变化,据美国疾病控制和预防中心估计,美国至少有100万成年人受到IBD的影响,目前这一疾病无法治愈或预防。Winter博士指出,II型糖尿病,结肠癌,艾滋病相关肠道疾病,以及某些早产儿中出现的坏死性小肠结肠炎也存在肠道菌群的变化。
肠道菌群中与炎性疾病有关的一些细菌一般是肠杆细菌科(Enterobacteriaceae)的细菌,其中大部分家族成员,比如非致病性大肠杆菌(Escherichia coli)在健康肠道中存在少量,能用于防止诸如食物中毒的常见原因沙门氏菌(Salmonella)等病原体的感染。
然而,在IBD患者和小鼠结肠炎模型中,肠杆细菌科细菌生长失控,文章的第一作者,博士后研究员朱文汉(Wenhan Zhu,音译)博士说。
这一研究组近期也在Cell Host&Microbe杂志上发表文章,指出这些细菌家族具有独特的代谢方式:它们产生用于生长的细胞能量,以及获得营养的方式不同于其它肠道细菌。肠杆细菌科细菌采用特殊的代谢技巧来促进其过度生长,在疾病发生阶段会产生竞争优势的肠道细菌。
“这些途径是独特的,因为它们只存在于某些细菌中,只在肠道炎症中起作用。因此这也为针对肠道炎症相关疾病,如IBD的合理预防和治疗策略设计提供了机会”,Winter解释说。
由此在Nature文章中,研究人员提出了使用重金属钨:钨酸盐来抑制病原体的代谢。
朱文汉博士说:“总体思路就是,钨破坏了肠杆菌产生能量的方式,减缓发炎期间病原菌的生长。”
研究人员发现,钨被细菌吸收,无意中与一种重要的细菌辅助因子合作,因此导致毒性辅因子无法发挥功能,阻止了细菌在发炎的肠道中获取能量。小鼠模型证明,在饮用水中添加钨酸盐(一种可溶性钨盐)能有选择地阻止了肠道中肠杆细菌科细菌的繁殖。而附近的有益菌不会受影响,这显然是因为它们的能量生成代谢不依赖于特定的辅因子。
“值得注意的是,我们的这个方法策略只能抑制肠道炎症期间肠杆菌科细菌的繁殖,而不会完全摆脱它们。不过这一发现依然非常重要,因为在适当的比例下,肠杆菌科细菌也能够抵抗细菌病原体的定植作用。因此,在炎症发作期间控制这些细菌的繁殖,要比将其从系统中完全除去更好一些”,”Winter博士说。
在这项研究中,小鼠结肠炎模型中的钨酸盐治疗使肠道微生物菌群在细菌种类平衡方面转变为更为正常的状态,并且还减少了肠道炎症。虽然钨酸盐治疗并不能治愈这种疾病,但它改善了动物的整体健康状况。
Winter博士说:“这项研究只是通过‘概念验证’确定了一个潜在的分子靶标,目前还远没有把这个基本的发现转化为患者的治疗。因为钨是一种重金属,可能会产生严重的负面影响,如神经和生殖方面的危害”。
传统的治疗方法集中于治疗人类宿主,而这些最新的结果给出了新希望,从原则上说,可以利用正常的肠道细菌来改善宿主,比如说通过在消化道炎症过程中仔细指导肠道微生物群的功能和组成。
“这项研究中,我们找到了一种只针对一种肠杆菌科细菌的方法,希望通过更多的研究来寻找潜在的治疗人类疾病的方法,这是充满希望的第一步。”
肠道细菌与癌症免疫疗法
这篇文章的研究重点是人类——38名接受nivolumab或 pembrolizumab(抗-PD-1相关药物)检查点抑制剂和4名接受ipilimumab(抗-CTLA4相关药物)治疗的转移性黑色素瘤患者。
“早期的小鼠研究是一个意外发现。在此之前我们一直认为微生物可能只是次要因素,癌细胞阻挠免疫系统工作应该是一个多重效应,”文章作者,芝加哥大学癌症免疫疗法教授Thomas Gajewski博士说。“但是在这项最新研究中,我们发现,肠道菌群是预测患者免疫反应的重要指标。”
研究者们将注意力集中在了8种“有益”细菌和2种“有害”细菌。有益细菌在对治疗有反应的患者身上更为常见,反之,有害细菌是对疗效无应答患者肠道的优势菌。
从现象中,研究人员推测,特定的肠道细菌似乎增强了T细胞进入肿瘤微环境的能力和癌细胞杀伤力,从而使机体对免疫治疗产生持久且旺盛的反应。
考虑到细菌宿主的个体差异,研究人员联合使用16S rRNA测序、宏基因组shotgun测序和Q-PCR三种不同方法确定了微生物的基因序列。有益细菌比率较高的患者都显现出了较好的临床反应,即肿瘤体积明显缩小。
为了确认人类肠道细菌是否直接影响治疗效果,研究人员做了一个小型测试,分别收集3名响应治疗和3名不响应治疗的受试者的粪便细菌。将这些细菌移植给无菌小鼠(因为还不能用人做试验)。两周后,对小鼠进行黑色素瘤细胞移植处理。
2只移植了“有益”细菌的小鼠肿瘤生长缓慢,2只移植了“有害”细菌的小鼠肿瘤生长迅速。用PD-1阻断药物处理小鼠,只有移植了“有益”细菌的小鼠有反应,即肿瘤呈现皱缩。
另外两篇文章中,研究人员分析了112名接受抗PD-1免疫疗法的患者的口腔与肠道菌群。研究者们发现,PD-1免疫疗法应答者(R)与不应答者(NR)的肠道菌群的多样性和组成具有显着差异。通过病人粪便微生物的分析, R 具有明显更高的α多样性和相对丰度的瘤胃球菌科细菌。
还有一篇文章指出,患者对靶向PD-1 / PD-L1轴的免疫检查点抑制剂(ICI)的主要抵抗可能是由于肠道微生物组成的异常,而抗生素(ATB)可抑制晚期癌症患者ICI的临床获益。那些无法从免疫疗法中受益的患者,体内缺乏一种Akkermansia muciniphila的细菌。随后,小鼠实验证明了这种细菌的益处。研究者们利用粪便移植的方法,将“免疫疗法有反应”和“免疫疗法无反应”的患者的肠道菌群移植入抗生素处理过的小鼠体内。最终,前者对免疫疗法产生应答,而后者对免疫疗法没反应。倘若让后者再口服Akkermansia muciniphila,则能重塑免疫疗法的疗效。
-
企业风采

-
项目成果

-
焦点事件

-
科技前沿

-
科技前沿

-
项目成果

-
会议会展

-
会议会展

-
精英视角

-
科技前沿

-
项目成果
-
项目成果
-
项目成果

-
焦点事件

-
科技前沿

-
项目成果

-
项目成果

-
科技前沿
-
科技前沿

-
项目成果
-
焦点事件
-
项目成果

-
综述