Nature找到引发AD的关键分子途径
说到阿尔茨海默症(Alzheimer disease,AD),这也是一种一早被发现,但目前仍然没有有效治疗方法的顽疾。不过近期来自哥伦比亚大学医学中心(CUMC)的研究人员将系统生物学和细胞生物学研究技术结合在一起,创新的推出了一种针对阿尔茨海默症研究的新方法,从中破解了导致晚发型阿尔茨海默症(阿尔茨海默症最常见形式)的关键分子途径,并提出了几个新的潜在药物靶点。
这一研究新突破公布在Nature杂志上。
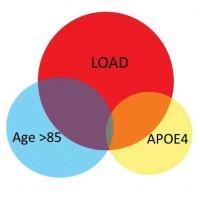
(此图显示了携带APOE4高风险突变,未受影响个体的大脑基因表达的变化,85岁以上,未受影响个体大脑基因表达的变化,以及晚发型阿尔茨海默症患者大脑基因表达的变化)
阿尔茨海默症分为早发型和晚发型,其中晚发型阿尔茨海默症(late-onset Alzheimer’s disease, LOAD)是最常见的一种阿兹海默症,但反而科学家们对于这种类型的疾病并不十分了解。
文章第一作者,CUMC研究所神经细胞生物学和病理学副教授Asa Abeliovich表示之前关于阿兹海默症的发现主要来自实验室针对罕见的早发型进行的研究,“造成了目前对于常见形式阿尔茨海默症的不了解,而且最重要的是,之前能在家族患病小鼠模型中起作用的几十种药物,最终证明都无法用于晚发型阿尔茨海默症的治疗,因此我们希望能深入探索这种常见形式疾病形式的作用机制。”
非家族性阿尔茨海默症的致病原因十分复杂,科学家们认为它是由遗传和环境危险因素共同导致的。此前曾有研究利用全基因组关联研究(GWAS)技术,找到了几个可能增加疾病风险的常见遗传突变,但关键在于解析这些常见遗传突变如何影响疾病患病风险的。
在这篇文章中,研究人员发现了将这些遗传风险因素与阿尔茨海默症联系在一起的关键分子途径,这项工作结合了细胞生物学和系统生物学的研究工具,利用计算机分析风险个体大脑中基因表达复杂网络的变化。
具体来说,研究人员首先集中于单个最重要的遗传因素:APOE4,这是大约三分之一的患者都会出现的突变,如果携带这种突变一个拷贝,就会增加三倍患上晚发型阿尔茨海默症的风险,如果有两个拷贝,就会增加十倍风险。
Abeliovich博士说:“在这项研究中,我们最初提出的问题就是:对于高风险患者来说,其尸检脑组织是否有统一的模式?”
令人惊讶的是,即使在没有患上阿尔茨海默症的情况下,高风险个体(携带APOE4)的脑组织依然出现了一些与患者相似的变化。由此研究人员聚焦于这些变化,他们认为大脑的变化主要基于“transcriptomics(转录组)”,因此采用上文提及的网络分析工具,进行了深入探索。
结果研究人员发现了十几个连接APOE4与阿尔茨海默症破坏性事件的主要调节因子。随后他们又通过细胞生物学研究,发现了一些参与大脑内神经元淀粉样前体蛋白(APP)加工和运输的主要调控元件,由此建立了高风险阿尔茨海默症个体,APOE4与疾病病理之间的关联。
在这些候选调控因子中,研究人员又进一步找出了两个基因:SV2A和RFN219。“我们对SV2A特别感兴趣,因为它是一种常用的抗癫痫药物:左乙拉西坦(levetiracetam)的靶标,这指出了一种新治疗策略。不过还需要进一步的研究数据”。
Abeliovich博士说,“我们的研究结果表明,这个两个基因(SV2A和RFN219)都可以作为候选药物靶标,令我们感到激动的是,这些方法未来也许将在常见的非家族形式阿尔茨海默症药物研发过程中起到重要作用。”
-
技术原理
-
焦点事件