Science:走向临床的光遗传学
光遗传学诞生后的头十年,大大推动了人们对正常和病理性神经回路的理解。今后的十年,光遗传学将迎来与转化医学的联姻,为疾病治疗带来新的机遇。本期Science杂志上,Bryson等人就展示了这样一个范例,他们将光遗传学工具与再生医学知识结合起来,在周围神经损伤的小鼠模型中恢复了肌肉的功能。
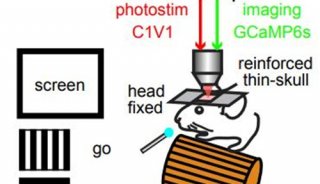
光遗传学实验面临的第一个问题是,如何在目的细胞群体中实现视蛋白opsin的稳定表达。Bryson等人对小鼠的胚胎干细胞进行了基因工程改造,使其稳定表达ChR2蛋白,ChR2是一种对蓝光敏感的阳离子通道。随后他们在体外诱导这些细胞分化,形成具有光遗传学活性的运动神经元。当这些ChR2运动神经元受到蓝光照射时,就会被激活。
研究人员通过结扎坐骨神经,构建了肌肉失去神经支配的小鼠模型,并将含有ChR2运动神经元的拟胚体移植到小鼠体内。他们将这些小鼠麻醉,用蓝光照射移植位点,成功恢复了小鼠腿部肌肉的功能。研究显示,移植的ChR2运动神经元能够在小鼠体内生存和成熟,帮助小鼠重新控制腿部肌肉。
研究人员指出,这种光遗传学刺激可以实现运动单位的“有序募集”,与正常的生理活动非常类似。而采用电刺激时,运动单位的募集往往是逆向或随机的。
这项研究开辟了许多新的研究方向,例如可以尝试在非麻醉的小鼠体内实现光激活的肌肉功能恢复。要在自由活动的动物体内进行持续的光遗传学刺激,就需要使用植入性的长期发光装置。
Bryson等人的研究显示,ChR2运动神经元的终板(endplate)存在一定畸形,这可能是因为移植后的神经元一开始并没有活性。而长期性的植入装置,可以在移植后立刻激活神经元,避免这样的畸形。另外,如何让移植神经元长期存活,也是一个重要的问题。
Bryson等人描述的这种细胞移植方案也可以用来治疗其他类型的神经学疾病。不过,在成功实现光遗传学治疗之前,人们还需要攻克一些难题。举例来说,人们需要将光遗传学技术从鼠类模型应用到非人类的灵长动物,尤其是大脑以外的神经回路。在病毒载体、细胞移植法等不同递送策略下,opsin表达的长期安全性也有待评估。此外,人们还需要开发机体能够耐受的植入性发光设备,进一步改善opsin蛋白的光敏感性和其他特性。尽管前方还存在着不少挑战,Bryson等人的这项研究仍旧是光遗传学走向临床的重要一步。
-
科技前沿
-
市场商机
-
科技前沿

-
项目成果
-
项目成果