SLAS 2013分会:微纳米技术探索生物系统
2013年6月6日,实验室自动化与筛选协会2013亚洲会展在上海金茂君悦大酒店盛大开幕,国内外知名药企、生物医学研究专家、学者等应邀参会。“微纳米技术探索生物系统”分论坛于6月6日下午在B厅举行,由中国科学院化学研究所有机固体院重点实验室研究员王树涛博士、上海交通大学教授施奇惠博士、清华大学医学院生物医学工程系研究员刘鹏博士和厦门大学化学生物学系教授杨朝勇博士作精彩演说。
本论坛主题是微纳米技术探索生物系统。微米和纳米技术极大地推动了生命科学的发展进程,同时,生命科学领域的新发现也为微纳米材料和微纳技术的发展提供了广阔的应用空间。本分会着重关注基于新型微纳米材料和微流控技术的自动化高通量筛选平台在探索生物系统领域的研究进展。报告将关注目前十分活跃的研究领域包括循环肿瘤细胞快速检测分选、高通量单分子、单细胞分析新方法,以及在肿瘤相关基因和蛋白等分子诊断中的应用。
中国科学院化学研究所有机固体院重点实验室研究员王树涛博士
首先,由中国科学院化学研究所有机固体院重点实验室研究员王树涛博士作《生物纳米界面及其癌症检测应用》精彩报告。
循环肿瘤细胞(CTCs)已经成为了一个新兴的生物标志物监测癌症的转移和预后手段。虽然现有隔离/技术CTCs技术、最常见的免疫磁珠,但都受限于低捕捉效率和低特异性。通过引入三维纳米基质,具体地说,硅纳米线的硅纳米线阵列涂有抗EpCAM,可以捕捉具有更高效率和特异性的CTCs。传统的方法依赖于生物分子隔离CTCs,如抗原-抗体相互作用的生物分子。王树涛博士在这里提出,纳米级的本地生物分子识别地形相互作用,除了灵感来自天然免疫识别系统。CTCs和基质之间的物理和化学协同效应导致增加CTCs的结合,大大提高捕捉效率。王树涛博士指出最近开发了一种三维细胞捕捉/释放系统触发的适体酶,有效而无损伤捕捉和释放癌症细胞。细胞捕捉和释放的仿生界面开启了稀有细胞基础诊断,如CTCs、胎儿细胞、干细胞等。
上海交通大学教授施奇惠博士
《单细胞蛋白组芯片在生物医学及临床诊断中的应用》这一演讲报告由上海交通大学教授施奇惠博士带来。
在生物学的进展已经使研究人员定义疾病在分子水平和视图疾病为微扰(基因或缓解)网络正常编程信息模式的问题结果。新的生物技术的承诺,来分析网络的交替与定量测定生物标志物(基因,蛋白质和代谢物),少量的病人的血液或组织样本,指导疾病早期识别和个性化的治疗特定疾病。蛋白质,作为直接执行生命功能的分子机器,是迄今为止最大的临床意义的诊断目标。施奇惠博士称我们已经开发了自动的,基于微单细胞蛋白质组芯片(SCPCs)定量分析几十多个单一肿瘤或免疫细胞中的信号转导通路相关的蛋白质。多重蛋白精确测量测量单细胞能力依赖于微型的、芯片上基于DNA编码抗体库(DEAL)技术的高密度DNA编码抗体微阵列。单细胞蛋白质组学分析揭示大量的独特传统技术的基础上集成看似相似的细胞,包括细胞特异性,不同蛋白质之间相互关系的不容易披露的疾病机制的相关信息,蛋白质的热力学稳定性影响外部扰动和一定微环境内的细胞间相互作用。因此,高吞吐量的单细胞蛋白质组学定量分析测量能够提供高灵敏度和低成本的方法来定量分析大蛋白质生物标志物(例如血液蛋白和信号转到网络相关的细胞内蛋白),为早期疾病鉴定、患者分层和个性化治疗的生物标志物的选择提供参考。
清华大学医学院生物医学工程系研究员 刘鹏博士
来自清华大学医学院生物医学工程系的刘鹏博士介绍了《用于高效基因分析的集成式微系统》。
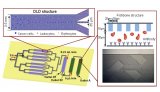
由于基因组相关研究项目的驱动,集成式微系统促进各种基因遗传分析方面得到了迅速的发展,一种用来鉴别人类身份的集成式微系统已经开发出来,包括了序列特异性的DNA模板的纯化,聚合酶链反应(PCR),扩增后的清理和毛细管电泳(CE)。片段基因组DNA与生物素标记捕获的寡核苷酸杂交,然后通过目标DNA被获取的微通道中固定化链霉抗生物素涂覆的流化床进行输送,然后这些片段转移到250nLPCR反应器中进行常染色体STR扩增。扩增后的产物通过链霉亲和素修饰的捕获凝胶进行电泳纯化而浓缩和纯化。热释放样品加入到毛细管柱中进行电泳分离和检测,口腔样品用这种微系统成功的进行了分析,这种输入传出的集成式微系统在快速和灵敏方面有着非常的优势,是一个可靠的人类鉴定的分析系统。基于这样的成就,我们目前也正在开发便携式微系统进行目标DNA测序,这也将会成功的应用在个性化医疗诊断和治疗中。
本次分会的最后一个报告题目为《超高通量琼脂糖液滴微流控单分子PCR及其在生物分析与生物工程中的应用》。
细胞的克隆和PCR,是单个DNA分子形成同种DNA分子群体的两种方法,这也是20世纪最重要的生物技术的发展。以细胞为基础的克隆这种方法,能从个体分子增长至整个群体。当需要独立的产品时,为了避免繁琐和冗长的细胞培养过程,PCR为基础的方法就要求个体空间都有单独的模板。乳液PCR(ePCR)可以通过缩小空间来克服这个缺点从而使数以百万计的模板在单独的管子里进行独立的放大。然而,传统的ePCR方法是有限的,因为液滴尺寸的大幅度变化而导致低效率和长链DNA片段扩增的不均匀性,更重要的是,从液滴中回收DNA产品是非常难的。为了解决这些问题,我们开发了一种琼脂糖滴微流控EPCR方法可以进行平行的、均匀的、高效的DNA克隆。我们的方法就是利用微流控芯片的性能从而迅速形成单分散的液滴和琼脂糖独特的热敏开关特性,微型琼脂糖发生器产生均匀的皮升琼脂糖凝胶乳液液滴进行基因组分析已经被开发和评估,然后在琼脂糖溶液液滴中有效的进行PCR扩增,扩增后形成微珠可以用来捕获和维持每个液滴的单克隆性。我们的研究结果表明单拷贝DNA能够在琼脂糖液滴中进行有效的扩增并且产生的单克隆微珠在下游工艺能方便的操纵。此外还介绍了琼脂糖液滴微流控ePCR的一些关键功能,及其方法的一些应用包括单细胞基因表达的研究、罕见突变的检测以及高通量筛选。
-
项目成果