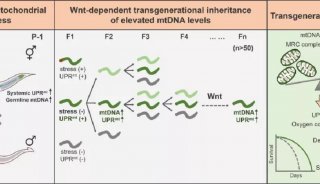
Cell揭示“渐冻人”病因机制
研究人员将肌萎缩侧索硬化症(amyotrophic lateral sclerosis ,ALS)与其他神经退行性疾病的一个致病基因的突变,与细胞中某些蛋白质和相关分子的毒性累积联系起来。这项发表在近期《细胞》(Cell)杂志上的研究,为开发出对抗这些破坏性疾病的治疗提供了一种新方法。
研究结果提供了首个证据,证实一种名为VCP的基因对分解和清除累积于RNA颗粒(RNA granule)这一临时结构中的蛋白质和RNA分子起重要的作用。RNAs执行着包括蛋白质生成在内的各种重要细胞功能。RNA颗粒支持了RNA的正常运作。
在ALS和相关神经退行性疾病中,RNA颗粒的组装和清除过程受损。与颗粒相关的蛋白质和RNAs往往累积在患者的神经细胞中。这一研究揭示了VCP突变有可能是如何推动这一过程和神经退行性疾病的。
“这些研究结果具有重要意义,它解释了与包括肌萎缩侧索硬化症、额颞痴呆以及称作为多系统蛋白病(multisystem proteinopathy)的大脑、肌肉和骨骼相关疾病在内的各种神经退行性疾病相关的这一过程,”论文的共同通讯作者、St. Jude儿童研究医院发育神经科学系成员J. Paul Taylor, M.D说。
ALS又称Lou Gehrig病,俗称“渐冻人”,是一种大脑和脊椎中控制运动的神经细胞渐进性退化的疾病,在美国每年大约有5,600人确诊。当前没有有效的治疗方法,通常在5年内死亡。
“这项研究的一个重要之处在于,它提供了关于不同遗传突变如何全部影响应激颗粒的一个统一假说,表明了解应激颗粒动态以及如何操控它们,有可能有利于治疗这些疾病,”论文的共同通讯作者、科罗拉多大学化学和生物化学系和霍华德休斯医学研究所Roy Parker博士说。
在早些时候的研究工作中,Taylor实验室确定了VCP突变是ALS和相关多系统蛋白病的病因。然而直到现在对于这些错误致病的机制仍知之甚少。最新的研究发现分别以两篇研究论文形式发表在6月20日和8月15日的《细胞》(Cell)杂志上。
论文的共同第一作者、Parker实验室博士后人员Regina-Maria Kolaitis说,新研究将VCP突变与RNA调控破坏联系到一起,而之前的研究证实了它与神经退行性疾病进展之间的联系。
这项研究工作将焦点放在一类称作为应激颗粒的RNA颗粒上。它们是由蛋白质和累积在细胞质中响应压力的mRNA分子所组成。压力细胞不希望浪费能量来生成不必要的蛋白质。细胞利用应激颗粒这一机制来停止蛋白质生成,直至应激颗粒分解,细胞环境恢复正常。
应激颗粒中包含有如TDP-43、FUS、hnRNPA1和hnRNPA2B1等调控基因活性的RNA结合蛋白。这些蛋白质突变也可引起ALS和相关疾病。
Kolaitis 说:“VCP在细胞中具有许多的功能,但它不是一种RNA结合蛋白,直到现在我们才将它与应激颗粒或RNA加工联系到一起。这项研究为了解疾病过程,阐明VCP在维持细胞健康中的作用提供了一扇新窗口。”
在这项研究中,研究人员利用酵母确定了影响应激颗粒的形成和行为的125个基因组成的网络。其中一个基因CDC48似乎在该网络中发挥中心作用,在酵母中它的功能与VCP相似。此外,还确定了许多与自噬过程有关的基因,细胞通常利用自噬来分解和回收不需要的分子,包括蛋白质。
用酵母和哺乳动物细胞开展实验,研究人员证实自噬清除了应激颗粒,而当VCP突变时这一机制停止运转。研究人员还报告,在CDC48或VCP突变后应激颗粒发生了累积。
“这项工作表明,激活自噬有助于细胞清除应激颗粒,从而为治疗神经退行性疾病提供了一种新方法,”Taylor说。
-
科技前沿
-
科技前沿