同济大学CellRes提高细胞重编程效率的新方法
来自上海同济大学生命科学与技术学院、中科院上海药物研究所的研究人员在新研究中证实利用高渗透压可提高体细胞的重编程效率,并揭示了其分子作用机制。相关论文“Stress-mediated p38 activation promotes somatic cell reprogramming” 发表在重要核心期刊《Cell Research 》上。
文章的通讯作者是现任职于上海同济大学生命科学与技术学院和中科院上海药物研究所/国家新药筛选中心的谢欣博士。主要研究方向为G蛋白偶联受体(GPCR)信号通路与重大疾病相关性研究及新药发现以及小分子化合物调控干细胞命运的研究及新药发现。
2006年,日本科学家山中伸弥通过向人体皮肤细胞中植入4个经过重新编码的基因,使皮肤细胞具备类似胚胎干细胞的功能,从而获得所谓iPS细胞。此项技术不仅为发展再生医疗开创了道路,也对整个医学研究的发展做出巨大贡献。尽管近年来科学家们针对iPS展开了广泛的研究,但目前对于其确切的基本分子机制还不是很清楚,人们相信在iPS诱导中涉及了整体的表观遗传改变。
为了避免利用癌基因和插入病毒DNA序列,使生成的iPS细胞更适合治疗应用,科学家们付出了大量的努力来改良最初的实验方案,或采用减少数量的因子,非整合性的基因传递方法,或是利用细胞渗透性蛋白来启动重编程。有研究报道许多的小分子,尤其是那些可以影响表观遗传调控的分子如VPA、 butyrate等可以促进iPS细胞诱导。
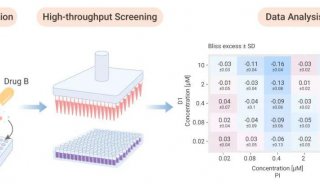
为了更好地发现细胞重编程的小分子增强子,谢欣课题组研究人员开发了一个96孔板筛查系统。出乎意料的是,研究人员发现相比于中心孔,角落孔中的 iPS细胞出现得更早,诱导效率更高。在排除pH和营养改变的可能性影响后,研究人员发现角落孔中增高的渗透压促进了iPS细胞生成。高渗透压不仅促进了四个因子介导的重编程,还增加了两个或一个因子结合其他化学物质诱导的iPS细胞生成。
过去的研究证实高渗透压可以激活许多压力相关信号通路,包括MAPK信号通路。在新研究中,研究人员证实高渗透压介导的p38激活在促进重编程中起关键性作用。组成性活性p38可模拟高渗透压的正效应,而显性负p38和p38抑制剂PD169316则可阻断高渗透压的效应。此外,进一步的研究表明压力介导的p38激活可能通过减少整体DNA甲基化水平,增强多能性基因表达而促进重编程。
新研究证实高渗透压可通过细胞内信号和表观遗传调控提高体细胞重编程效率,改变细胞的命运,从而为我们提供了一种促进iPS生成的简单安全的新途径。
作者简介:
谢欣
中科院上海药物研究所研究员,国家新药筛选中心模型建立II部主管,同济大学生命科学与技术学院兼职教授。1996年毕业于北京大学化学系,获理学学士学位。2002年获得美国新泽西医科和牙科大学神经科学专业的博士学位。随后转入新泽西医学院从事神经生物学方面的博士后研究工作,期间致力于神经节苷酯对神经细胞内钙离子平衡调控作用的研究。2004年加入国家新药筛选中心担任模型建立II部主管,从事G蛋白偶联受体的信号转导通路研究、小分子化合物对干细胞命运调控的研究及高通量/高内涵新药筛选模型建立及应用工作。2005年入选上海市“浦江人才计划”,中国科学院“百人计划”(2006年获择优资助);2007年被聘为同济大学生命科学与技术学院客座教授,参与同济受体生物医药实验室的建立及管理工作;2009年获“上海市科教系统三八红旗手”称号,入选“新世纪百千万人才工程”国家级人选。参加或主持多项国家、科学院及地方的科研项目,2009年作为首席科学家承担科技部重大科学研究计划项目。