上海生科院发现先天性再生障碍性贫血的致病机理
7月4日,国际学术期刊Cell Research 在线发表了中国科学院上海生命科学研究院健康科学研究所潘巍峻研究组的最新研究成果“Mutation of kri1l causes definitive hematopoiesis failure via PERK-dependent excessive autophagy induction”。该工作揭示了一种全新的造血干细胞增殖稳态调控机制,指出协调的核糖体蛋白合成机制是维持造血干细胞自我更新能力的重要保障;该研究工作为多种再生障碍性贫血的治疗提供了理论基础和药物干预手段。
先天性再生障碍性贫血是一种骨髓衰竭综合症,其主要表现为包括红细胞在内的多种血细胞减少,并经常伴随肿瘤易感,如急性髓系白血病和成骨瘤等。目前该疾病的致病机理仍存在较大争论,有观点认为再生障碍性贫血的发生往往是由于编码核糖体小/大亚基的基因突变引起,继而诱发造血干细胞发生p53信号通路依赖的细胞凋亡进而引发骨髓衰竭,目前该类疾病的有效治疗手段仍未被成功研发。
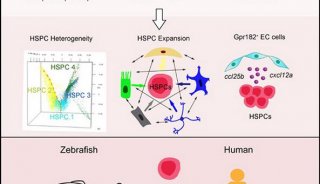
博士研究生贾小娥、马可和徐涛等人在研究员潘巍峻的指导下,对具有人类先天性再生障碍性贫血相似表型的斑马鱼突变株cas002进行研究分析,发现kri1l基因突变后核糖体40S小亚基中的18S rRNA合成受阻,核糖体无法正确组装,蛋白合成能力异常并诱导错误折叠蛋白在细胞中大量积累,由此激活了PERK-eif2α信号通路,进而引发高强度的细胞自噬,且该过程不依赖于p53信号通路介导的细胞凋亡;过度的自噬行为破坏了造血干细胞自我更新能力,进而导致骨髓衰竭。
该研究工作首次阐明了核糖体蛋白异常、过度自噬和骨髓衰竭三者间的联系;利用PERK信号通路的小分子抑制剂(GSK2656157)或直接针对自噬过程的小分子抑制剂(BafA1、3-MA)等有效恢复了斑马鱼再生障碍性贫血模型中造血干细胞增殖能力,揭示其应用于相关血液疾病靶向治疗的潜在价值;基于造血干细胞过渡自噬的临床检测有望成为相关血液疾病临床诊断的有效手段。
该研究得到了国家自然科学基金委、科技部、上海市科委及国家青年千人计划的资助,与瑞金医院血研所陈赛娟实验室和波士顿儿童医院Leonard I. Zon实验室合作完成。