PNAS:靶向癌症的全新途径
科学家们发现,一种多聚物可以帮助药物靶向肿瘤。Freiburg大学的研究团队通过纯化学方式,成功为治疗性的纳米颗粒指引了方向,文章发表在本期的美国国家科学院院刊PNAS杂志上。这项研究展示了为纳米颗粒导航的全新模式,这些颗粒约几百纳米大小,可以作为微小容器将药物运送到内皮细胞。
研究人员发现,只要带电荷的多聚物拥有正确的亲和力,就能够帮助纳米颗粒简单地通过化学性质,识别特定的细胞类型。“这是一项非凡的成就,我们抛开了传统的配体-受体方案,首次仅通过生物物理学法则,引导纳米颗粒特异性的靶标细胞,”领导这项研究的Prasad Shastri教授说。迄今为止,人们在开发纳米药物时,都需要给纳米颗粒安上能与细胞表面蛋白(受体)结合的分子。
这些受体就像是特定细胞的邮寄地址或者邮编。然而,在肿瘤中这些地址能够随着时间推移发生快速的变化。为了解决这一问题,Shastri及其团队开发了新型的纳米颗粒,通过生物物理学途径靶向内皮细胞。“在这种递送方案中,纳米颗粒不需要生物学邮编来确定目标,这是利用纳米颗粒治疗癌症的一个重要进步,”文章的第一作者Julia Voigt说。
癌症是非常饥渴的组织,它们需要通过自己的血管不断获取营养供给。“靶标组成这些血管的内皮细胞,我们就可以攻击或者饿死肿瘤,”文章的共同作者Jon Christensen说。
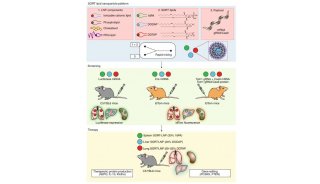
在癌症治疗中,人们往往利用纳米颗粒来运送药物。这些小药片是纳米医学的基础,它们被注射到人体后,可以通过血液到达肿瘤细胞。当它们被目标细胞摄取之后,药物就可以从内部对细胞施加影响。在此之前,纳米颗粒多半是通过受体介导的内吞过程进入细胞。而Shastri及其团队的新方法,利用的是内皮细胞的另一种主要运输过程。
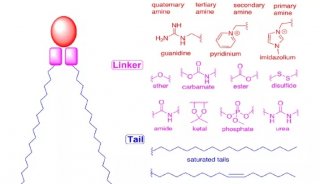
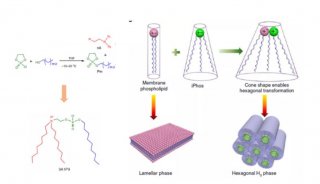
人们知道内皮细胞上存在着大量被称为caveolae的细胞膜内陷结构。Caveolae是一种细胞膜上的“脂筏”,是进入内皮细胞的大门之一。Shastri教授及其团队发现,给由脂质组成的纳米颗粒添加上带负电荷的多聚物,可以使这些颗粒优先进入caveolae的大门。“我们还不清楚这些带电多聚物打开caveolae大门的具体机制,不过我们相信进一步深入研究这一过程,将为人们开辟全新的药物递送途径,”Shastri说。
-
企业风采

-
焦点事件
-
科技前沿

-
项目成果