HDAC5在受伤后诱发再生长相关基因转录的重要作用
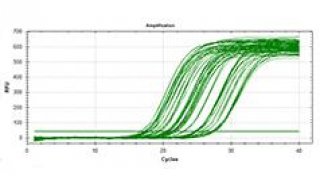
成功的轴突再生长需要细胞核中一个基因表达程序的开始;然而,这一程序是由什么激活的机制却一直没有搞清。Cavalli和同事如今发现,组蛋白去乙酰化酶5(HDAC5)的核输出在受伤后诱发再生长相关基因转录中扮演了一个重要角色。
之前的研究已经表明,培育小鼠的背根神经节(DRG)轴突切开术神经元产生了一个钙波动,从而传播至细胞体;然而,在体细胞中被激活的信号路径却不能被充分分开。在这里,作者在体细胞中观察到活化蛋白激酶Cμ(PKCμ)水平的增加,以及在神经损伤2小时后,从细胞质到细胞核的PKCμ的一个重定位。这种效应被在损伤位点使用钙螯合剂EDTA所抑制,这意味着损伤导致的钙波动在细胞核中造成了PKCμ水平的增加。
之前的研究已经表明,PKCμ在其他制剂中引起了HDAC5的核输出,并且DRG神经轴突切开术导致了HDAC5在损伤位点的积聚。为了调查增加细胞核PKCμ水平的影响,作者监测了损伤后用绿色荧光蛋白(GFP)标记的HDAC5在DRG神经元中的定位。他们发现,轴突切开术或伴随巨大戟二萜醇 3-angelate(I3A)的PKCμ药理学激活导致了从细胞核进入细胞质的依赖钙的GFP标记HDAC重定位,以及在朝向轴突顶端的运动中的一种增加。
HDAC5的重定位有何影响呢?在细胞核中,HDAC5限制了组蛋白乙酰化,并因此调节了基因转录:作者在这里发现,在生物体外或体内的DRG神经元轴突切开术增加了细胞核中乙酰化组蛋白3的水平。通过生成一个被捕捉于细胞核(HDAC5nuc)中的突变HDAC5蛋白,作者进一步研究了HDAC5 核输出的作用。通过比较损伤在野生型以及HDAC5nuc-表达神经元中的作用,他们鉴别出一组基因,它们被损伤以一种取决于HDAC5核输出的方式所激活,包括几种与可再生响应有关的转录因子。
接下来,作者调查了细胞核HDAC5输出对轴突再生的作用。HDAC5nuc的表达在培育的DRG神经元中抑制了轴突再生。相比之下,增加的轴突生长被观察出现于培育的DRG神经元中,这些神经元来自于HDAC5核输出通过在DRG上直接皮下注射I3A而被促进的小鼠中。此外,I3A的使用强化了一种“预处理损伤”在轴突生长中的再生促进作用,并在活体中提高了轴突生长。
与周围神经系统神经元不同,CNS中的神经元在损伤后通常未能成功再生。在这里,作者发现,视网膜神经节细胞(一类CNS神经元)损伤不能导致PKCμ水平的增加或HDAC5的再定位,意味着不能发起这一信号路径,从而可能有助于其再生能力的丧失。
这项研究通过后损伤信号能够触发表观遗传变异从而促进再生相关基因转录,进而证明了一种机制,并强调了外围和中枢神经之间的一些关键差异,从而可能有助于区分它们的再生能力。