北大学者PLoS Pathog发表有趣的“呕吐”机制
来自北京大学的消息,北大生命科学学院王忆平课题组通过生物信息学、分子遗传学及生物化学等手段,对铜绿假单胞菌mexAB-oprM操纵子的表达调控进行了深入研究,发现了一种有趣“呕吐”机制,也就是说当细菌遭到抗生素攻击导致其细胞膜出现威胁生命的异常时,细菌将及时感应到的危机信号传输给CpxR蛋白,激活mexAB-oprM操纵子,启动其“呕吐”机制(外排泵等),将体内的“毒药”(抗生素等)及时排出体外,从而达到细菌对不同药物的广谱耐药性。
这一研究成果公布在PLoS Pathogens杂志在线版上,田哲贤博士和王忆平教授为该论文的共同通讯作者,王忆平课题组的田哲贤博士为该论文的第一作者。
据介绍,自从1928年英国的弗莱明发明了青霉素以来,抗生素的使用将人们的寿命平均延长了24岁。然而,随着新抗生素的发现越来越难、越来越少,及细菌对不同抗生素的广谱的耐药性越来越强(其耐药机制之一是通过相似于人类的“呕吐”行为,即细菌通过非特异性的外排泵对不同化合物的不断外排,导致细胞内很难达到使其致死的药物浓度,达到细菌的多重耐药性;而一般抗生素的给药剂量也是有限的,否则对人体本身也会产生副作用。),耐药细菌的感染已经演变成为当前人类面对的强大威胁之一。因此,揭示病原菌的外排泵表达调控机制具有重要意义。
铜绿假单胞菌之所以被列为人类三大条件性致病菌之一,它的一个重要临床特性就是很容易产生多重耐药,是一种非常难以消除的病原微生物。在2013年的美国疾控中心(US CDC)把多重耐药铜绿假单胞菌列为10大耐药威胁(drug-resistant threats)。铜绿假单胞菌基因组上有12种编码RND(Resistance-Nodulation-Division)家族多药外排泵(multidrug efflux pump)的操纵子,铜绿假单胞菌通过调控这些操纵子的表达,使其拥有广谱的耐药性。在这12种多药外排泵中,mexAB-oprM操纵子编码的外排泵在其临床分离菌株中起主要的多重耐药功能。
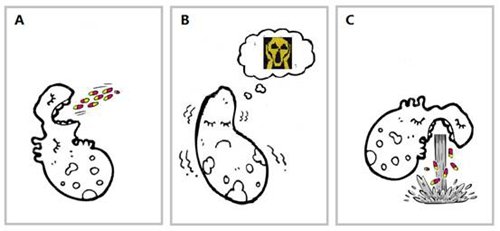
最新研究通过生物信息学、分子遗传学及生物化学等手段,对铜绿假单胞菌mexAB-oprM操纵子的表达调控进行了深入研究,发现在大肠杆菌等很多其它细菌中主管响应细胞膜胁迫信号的调节因子CpxR直接参与了mexAB-oprM操纵子的表达调控。体外研究结果证明,只有磷酸化的CpxR蛋白才可以结合mexAB-oprM启动子上游的靶位点;CpxR蛋白上的天冬氨酸磷酸化保守位点对其体内激活mexAB-oprM启动子至关重要。由于抗生素对细菌细胞的杀灭作用中也包括对细胞膜的直接或间接的胁迫作用,这暗示着当细菌遭到抗生素攻击导致其细胞膜出现威胁生命的异常时,细菌将及时感应到的危机信号传输给CpxR蛋白,激活mexAB-oprM操纵子,启动其“呕吐”机制(外排泵等),将体内的“毒药”(抗生素等)及时排出体外,从而达到细菌对不同药物的广谱耐药性(卡通表述见图一)。
图一:细菌广谱耐药产生过程的工作模型。A.细菌“吃进”抗生素;B.细菌“感应到”细胞膜胁迫等异常信号后,通过CpxR激活MexAB-OprM外排泵的表达;C.细菌通过“呕吐”把体内的抗生素排到体外,达到其耐药的目的。
这一研究通过在铜绿假单胞菌的实验室模式菌株PA14中开展研究,揭示了CpxR激活蛋白与mexAB-oprM操纵子之间的调控偶联。为了探索其临床意义,研究还对医院临床分离菌株进行系统分析,发现CpxR蛋白通过激活MexAB-OprM外排泵的表达,参与了其中部分耐药临床分离菌株的高耐药能力。因此,揭示CpxR对铜绿假单胞菌MexAB-OprM外排泵的表达调控机制,不单对研究细菌耐药性产生机制具有重要的理论意义,而且对防治日益严重的细菌耐药性问题具有重要的现实意义。
作者简介:
王忆平
教育经历
1984年获得中国科技大学生物系分子生物学专业学士学位;1992年获得爱尔兰国立大学科克学院微生物学系博士学位;
工作经历
1984年-1985年在中科院植物研究所固氮研究室做实习研究员;1986年在德国比勒费尔德大学遗传学系做访问学者;
1991年-1992年,爱尔兰Bio-Research Ireland Food Biotechnology Center,Research Scientist;
1993年在法国巴斯德研究所分子生物学部做博士后;
1994年8月-1999年6月北京大学生命科学学院副教授;
1999年7月至今北京大学生命科学学院教授。
社会服务工作
1995年10月-2002年8月,北京大学生命科学学院副院长;
2002年–2006年,国家“973”重大基础研究计划生物固氮项目首席科学家;
2004年,第十四届国际固氮大会主席;
2010年–2014年,国家“973”重大基础研究计划生物固氮项目首席科学家;
荣誉奖励
1999年国家杰出青年基金获得者
科研领域描述
本实验室主要兴趣在于:
多年来,本实验室的工作得到国际同行的认可。主要得到国家自然科学基金、国家科技部“863”、“973”项目基金、国家教育部基金资助、中法先进合作项目、Human Frontier Science Program等项目资助。主要工作包括:大肠杆菌及相关细菌中的基因调控网络,尤其是碳代谢和氮代谢的调控偶联;大肠杆菌及相关细菌中的基因调控机理;植物与微生物相互作用的分子生物学及功能基因组学研究;生物修复领域的研究(功能基因的分离);合成生物学及生物固氮;大肠杆菌定量生物学研究等。取得的主要成就有,发现原核基因表达调控中碳代谢及氮代谢之间的新的偶联作用及其分子机理;发现DNA物理特性参与基因表达调控(该成果被国际知名学术网站Faculty of 1000 推荐);提出了激活蛋白-启动子DNA-σ54-RNA聚合酶所形成的激活复合体的“三明治”结构模型(该成果被国际知名学术网站Faculty of 1000 推荐;使用合成生物学方法,我们使用T7 RNA聚合酶表达系统替代原有的σ54 RNA聚合酶对固氮基因簇的转录调控,绕开了原有固氮基因簇对转录调控系统中14种调控蛋白的依赖,为最终实现固氮基因向真核系统的转移打下坚实的基础;以肺炎克氏杆菌钼铁固氮基因簇为底盘,成功的在大肠杆菌中构建了杂合的铁铁固氮酶体系,从而在不损失酶活的前提下,成功构建了杂合的只含有10个结构基因的最小铁铁固氮酶体系。这一体系的建立,成功的绕开了我国缺乏钼元素,及植物学界关于线粒体、叶绿体内钼元素缺乏等问题,为最终实现固氮基因向真核系统的转移打下坚实的基础。
-
焦点事件
-
项目成果