Biolink——生物医药在中国的政策以及在欧美的发展
分析测试百科网讯 2015年12月1日,BioLink——第二届生物医药创新发展峰会在北京新世纪日航饭店举办。(详见本网报道:BioLink——第二届生物医药创新发展峰会在京召开)会议由中国医药保健品进出口商会、上海博华国际展览有限公司主办,中国外商投资企业协会药品研制和开发行业委员会和世易科技协办。会议吸引来自中国以及全球各地的200多位生物制药领域决策者参加,涵盖生物制剂、生命科技、生物制药、生物器材、分析仪器、CRO等领域。分析测试百科网作为支持媒体参加了此次会议。
美国强生集团的资深总监夏明德
大会由美国强生集团的资深总监夏明德主持。 会议分为六大模块:生物医药需要怎样的政策土壤;生物医药如何在欧美茁壮成长;揭开精准医学的神秘面纱;生物医药之最新研发与生产工艺;资本助力生物医药腾飞;生命科学产业投融资和技术转移合作项目路演专场。
生物医药需要怎样的政策土壤
上午的报告为政策相关,中国外商投资企业协会药品研制和开发行业委员会(RDPAC)执行总裁卓永清、中欧国际工商学院/中欧卫生管理和政策中心主任蔡江南、国家药典委员会生物制品标准处处长郭中平、美国康德乐公司法规科学副总裁/总经理Trey Putnam、BioCentury 首席执行官David Flores、新加坡交易所北京代表处副代表李晶主要介绍了生物医药方面的政策。
RDPAC执行总裁卓永清
第一位报告人是来自RDPAC的执行总裁卓永清。卓永清给大家介绍了《构建中国创新型生物医药产业生态系统》。
卓永清说加速生物技术药物产业发展对于患者、医药产业以及中国经济,都具有非常重要的战略意义。对于患者来说,生物技术药物解决了许多曾难以被攻克的重大疾病难题,改善了患者的生活。对于医药产业来说,生物技术医药是全球医药产业未来增长的重要推动力。而对中国经济来说,到2020年生物产业有望成为中国知识密集型经济模式的支柱产业之一。
但是,卓永清也强调,中国生物技术医药市场仍处在起步阶段,发展亟待提速,现在绝大部分已上市或在研的创新型生物药源自欧美。依照全球的经验来说,生物技术药物产业的发展需要依靠需求侧和供给侧双向激励政策体系。但是若缺乏有效可行的政策来培育和提升产业能力,仅靠市场需求拉动也很难促进产业快速发展。目前,中国的生物技术药物产业的发展正面临着诸多需求政策的障碍和挑战。
生物药有其独特的特点,异质性、结构复杂不稳定、受生产流程的影响、免疫原性,这些特性决定了生物类似物与其参照物不可能完全一样。低质量的生物药会严重威胁到病人的健康。中国需要确保相关监管政策一致性和上市后的监测体系以确保生物药的质量和病人的安全。
最后,卓永清对中国的生物医药产业提出了几个建议:1、希望完善监管机制;2、建立科学性的监管审批要求,加快生物技术药在中国的获批速度;3、改善市场准入,并提供强有力的知识产权保护。
中欧国际商学院中欧卫生管理和政策中心主任蔡江南
来自中欧国际商学院中欧卫生管理和政策中心主任蔡江南带来报告《中国卫生政策和健康产业创新动态》。
蔡江南说现代医疗资源行政化垄断较为严重,只占50%左右的公立医院,拥有的临床资源却占80%-90%,并且医疗资源和服务继续向大医院聚集。在中国有大量的医学毕业生没有当医生,这是为什么呢?
蔡江南介绍了卫生政策的发展状况。政策制定的速度和频率加快,药品仍然是聚集点,政府定价开始松动,医疗服务政策改革绕多元化办医、医生多点职业、补偿机制、改革步子还不够大。
关于健康行业创新发展状况,蔡江南说,创新活动遍布健康行业的各个子行业,创新方式也呈现多样化。聚集点主要围绕着消费者获得的价值,提供全方面解决方案。信息化方面的创新活动丰富多彩。民营机构和跨国公司的创新都很活跃,药品领域的创新相对较为薄弱。
国家药典委员会生物制品标准处处长郭中平
来自国家药典委员会生物制品标准处处长郭中平作报告《从新版药典看生物医药监管方向》。
郭中平首先介绍了新版药典的三部概况。新版药典整体的框架和标准体系分为凡例、生物制品通则、总论、通则(检测方法)、各论。并介绍了通则和各论的一个具体的内容和要求。与国外的标准比较,中国药典收载的生物制品总数多,各论及整体水平与欧美和日本药典日趋一致。通用性技术要求也与国际先进水平逐渐趋于一致,但仍需改善等。
生物医药产业的特点是高技术、高投入、周期长、高风险和高收益。我国的生物医药产业发展趋势正呈现高速发展的态势,新版药典的颁布与实施,将加快推动生物制品注册标准与国家标准的对接,全面提升生物制品注册标准和产品质量。
郭中平说,新版药典与生物药监管,2015版中国药典三部新增尼妥株单抗注射液,首次使用WHOINN英文音译名称。随着国内外生物技术和产业快速发展,中国药典生物制品国家标准收载内容及品种范围已不能满足相应需求。
美国康德乐公司法规科学副总裁、总经理Trey Putnam
来自美国康德乐公司法规科学副总裁、总经理Trey Putnam的报告题目是《Overview of the USBiologicals Market and Ensuring Regulatory/Commercial Success》,对美国生物制品发展现状及商业成功的保障进行了介绍。
BioCentury首席执行官David Flores
来自BioCentury首席执行官David Flores的报告题目是《Looking into 2016:Bio-Link: 2nd Biopharm Innovation & Development Summit》,对2016年金融市场全球化对生物医药行业的影响进行了展望。
新加坡上市平台的北京代表处副代表李晶
上午的最后一位演讲者是来自新加坡上市平台的北京代表处副代表李晶,向大家介绍了新加坡的上市平台。
生物医药如何在欧美茁壮成长
下午的报告中,Accord Research首席执行官Petri Janda、美国FDA驻华办公室副主任辛强、美国药典委员会中华区总部副总裁兼总经理冯兵兵对生物医药如何在欧美茁壮成长进行了解读。
Accord Research首席执行官Petri Janda
Accord Research首席执行官Petri Janda的报告题目是《BIOSIMILARS:REGULATION IN EUACCORD RESEARCH》,为大家解读欧盟生物类似物临床审批。
美国FDA驻华办公室副主任辛强
美国FDA驻华办公室副主任辛强的报告题目是《Biological Product Review》,介绍了FDA生物制品审评要点,并进行案例分享。
药典委员会中华区总部副总裁兼总经理冯兵兵
美国药典委员会中华区总部副总裁兼总经理冯兵兵带来了题为《Overview of Biologics Standard Developmentat United States Pharmacopeia》的精彩报告,对美国药典生物制品标准进行概述。
汤森路透产品与解决方案专家周峰
来自汤森路透产品与解决方案专家周峰带来报告《全球生物药市场和进展概览》。
2013年是Biosimilar最风光的一年,Celltrion公司和Hospira公司的英夫利昔单抗Biosimilar在欧洲上市。
全球生物药合作及许可项目正在增加,2014年和2010年相比有了很大的增长。生物药领域并购非常频繁。在2014年,前10销售的药物中,有7个是生物药。到2020年,前十药物中生物药仍占六席。
中国也是生物药研发的大国,居全球第二。国内企业交易不断,海普瑞和精华加入肿瘤免疫抗体合作。国内过半抗体药物为进口单抗。并介绍了肿瘤领域、免疫领域等项目的进展情况。
周峰向大家介绍了全球Biosimilar主要的开发公司,排名第一的是Amega Biotech,美国公司AXXO Im und Export GmbH排名第二。中国目前是拥有Biosimilar研发数量最多的国家。抗体是生物药的重点发展领域。
-
政策法规

-
企业风采

-
焦点事件

-
政策法规

-
标准

-
焦点事件

-
焦点事件

-
实验室动态

-
焦点事件

-
焦点事件

-
焦点事件

-
标准

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件

-
焦点事件

-
会议会展

-
标准

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
企业风采

-
焦点事件
-
焦点事件

-
标准

-
焦点事件

-
综述
-
焦点事件

-
市场商机

-
政策法规
-
会议会展

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
政策法规

-
焦点事件
-
焦点事件

-
焦点事件
-
焦点事件

-
招标采购

-
标准
-
标准
-
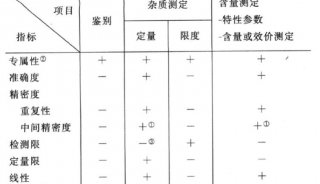
标准
-
焦点事件

-
精英视角

-
焦点事件

-
标准

-
焦点事件

-
焦点事件

-
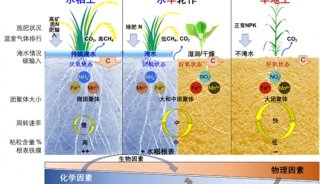
科技前沿
-
焦点事件

-
会议会展

-
企业风采

-
焦点事件

-
焦点事件
-
焦点事件
-
科技前沿

-
科技前沿

-
招标采购

-
财报

-
焦点事件

-
焦点事件

-
政策法规
-
焦点事件

-
项目成果
-
标准

-
企业风采

-
焦点事件

-
招标采购

-
焦点事件
-
项目成果
-
焦点事件

-
焦点事件

-
政策法规

-
焦点事件

-
标准

-
标准

-
标准

-
标准

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
标准

-
焦点事件

-
企业风采

-
焦点事件

-
会议会展
-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
科技前沿

-
政策法规

-
焦点事件

-
会议会展

-
焦点事件