第一章有机化学基本原理是可以质疑的 -专著连载(2)
Book Title: Question the Fundamental Principles of Organic Chemistry
Chapter First: The Fundamental Principles of Organic Chemistry Seem to Be Questionable.
----------------------------------------
第一章的下述章节已经在连载(1)中发表:
1. 有机化学中的基本原理
2. 氮桥双共轭体系的交替竞争共轭
2.1. 课题的设计
2.2. 紫外光谱法
2.3. 同系线性规律法
(由于博文带格式和博客软件的问题,所以排版很困难。如果阅读博文有困难,
可以下载PDF文件后,再阅读)
下面是本章的继续,本连载(2)的内容如下:
第一章的全部内容可以下载阅读下述PDF文件:第一章有机化学基本原理是可以质疑的
---------------------------------------------------------------
3.有机化学的基本原理是可以质疑的
在1-2-(m,n)系列化合物的合成方法中,有的涉及到氨基上的活泼氢与炔醛的加成反应,12因此成系列地合成化合物1-5-(m,n)是很困难. 所以, 实验部分只能选择化合物1-2-(m,n).
大概由于N-甲基的空间位阻效应,在1-2-(1,n) ( n = 0, 1, 2)分子的几何优化构象中,扭角q = C13-N11-C3-C2很大,分别是38.5o,39.7o和39.2o(图1-5到图1-7). 在化合物 1-2-(1,1)和1-2-(1,2)的晶体结中,对应的两面角分别是26.9o和28.0o,萘环平面与氨基平面的两面角分别是33.6o和31.4o. 关于分子内大扭角的驱动力,这将在《二苯乙烯类分子的构像和分子的扭曲驱动力》一章中详细地讨论. 在本章中,为了研究共轭效应与构象之间的因果关系,也为了尽可能地排除空间效应对分子构象的影响,我们优化了三个分子1-5-(1,n) ( n = 0, 1, 2)的几何构象(图1-8), 还优化了分子1-5-(1,0)的q = 0o构象(图18-a-2)和全平面构象(图1-8-a-3). 化合物1-5-(1,0)的q = 0o构象的优化受下属条件的限制:在优化过程中,两面角C13-N11-C3-C2 = 0o, H12-N11-C3-C2 = 180o始终保持不变, 其他键长,键角,两面角的优化不受限制.
从化合物1-5-(1,0),1-5-(1,1)到1-5-(1,2), 氮的孤对电子由主要与萘环共轭转向主要与戊二烯醛共轭. 根据共轭稳定的原理,N11-C3的键长rN11-C3应该增长,扭角q = C13-N11-C3-C2应该增大. 非常有趣的是,下述的几何优化数据的变化恰恰与预期的相反:(i)从化合物 1-5-(1,0)到1-5-(1,2), 键长rN11-C3变化是,1.419 Å (1-5-(1,0)) > 1.404 Å (1-5-(1,1)) > 1.401(1-5-(1,2)) Å; (ii) 扭角q的大小顺序是,28.0o (1-5-(1,0)) > 9.6o (1-5-(1,1)) > 7.3o (1-5-(1,2)). 这似乎意味着,氮的孤对电子与萘环的共轭效应不是使分子稳定的,而是失稳定的。 在1-5-(1,0)分子中,为了减弱共轭效应的失稳定的作用,萘环就必须离开分子平面,它的扭角q =28.0o. 同时, 萘环中所有的原子不再在同一个平面上(见附件1-3)。但是,在由B3LYP/6-31G*优化得到萘分子中,所有的原子是共平面的(附件1-4). 在分子1-5-(1,2) 中,由于氮的孤对电子已经转向与丙烯醛共轭,所以孤对电子与萘环的失稳定作用减弱。结果,扭角就下降到7.3o. 晶体结构的测定也表明,在化合物 1-2-(1,1) 和1-2-(1,2)中, 萘环与氨基氮平面的两面角分别为33.6o和31.4o (由于氨基不是一个平面构象,所以氨基平面与萘环平面的夹角不等于与两面角C13-N11-C3-C2), 这个变的化趋势与上述两面角的变化是一致的.
尤其是, B3LYP/6-31G*的计算表明,在分子1-5-(1,0)中,核排斥能EN,总电子能Ee和分子总能量E分别是:(i) 在能量最优的q =28.0o构象中,EN(28.0o) = 693.53676 hartree, Ee(28.0o) = -1248.12130 hartree, E(28.0o) = -554.58454 hartree (图1-8a-1); (ii) 在q =0o优化构象中,EN(0o) = 693.12877 hartree, Ee(0o) = -1247.71304 hartree, E(0o) = -554.58426 hartree. 两个构象的能差 DEN = EN(28.0o) – EN(0o) = 256.02 kcal/mol, DEe = Ee(28.0o) – Ee(0o) = -256.19 kcal/mol,DE = E(28.0o) – E(0o) = -0.17 kcal/mol. 尤其是,在q =28.0o和q =0.0o的构象中,C6-O14之间的距离rC6-O14(28o) = 8.376 Å < rC6-O14(0o) = 8.393 Å,rC6-C3(28o) = 4.872 Å < rC6-C3(0o) = 4.875 , rC3-O14(28o) = 3.606 Å < rC3-O14(0o) = 3.613. 对应的芳环和甲酰氨之间的排斥ENAB(28.0o) = 184.23370 hartree > ENAB(0o) = 183.77753 hartree. 这就是说,一个空间拥挤的q =28.0o构像,是一个能量最优的构象. 这样,有机化学中的构象和共轭效应强度之间的因果关系就应该被质疑了.
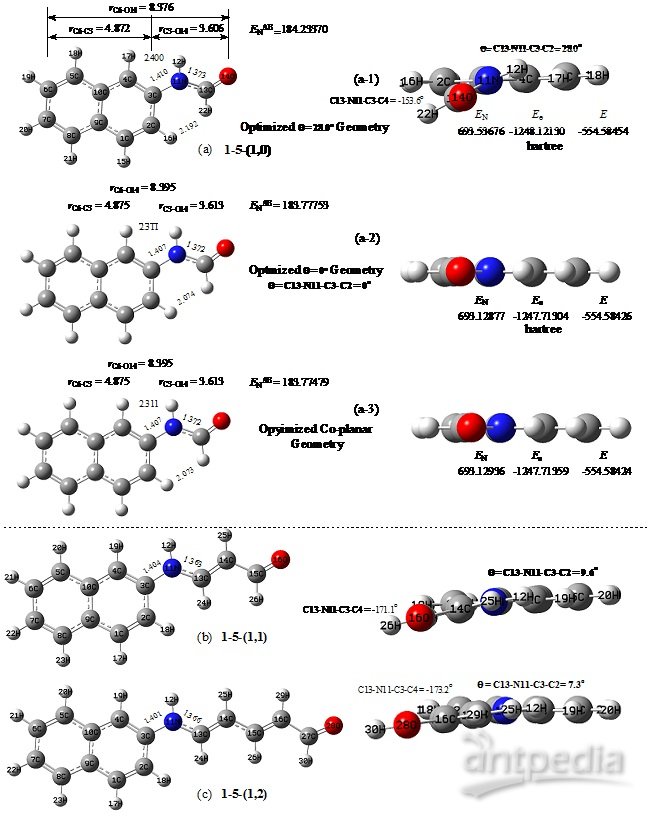
Figure
1-8 Optimized geometries of molecules 1-5-(1,0), 1-5-(1,1) 1-5-(1,2) at
B3LYP/6-31G* level. (a-2) Optimized planar geometry of molecular
1-5-(1,0). EN, Ee and E are the nuclear repulsion , total electron, and molecular energies ( hartree), ENAB is the nuclear repulsion energy between naphthenyl and formamido. The unit of the bond lengths is in angstrom.
4. 结论
上述讨论得到三个矛盾的结果。第一个矛盾的结果是,在同系分子1-5-(1,n) (n = 0, 1, 2)内,随着烯醛链链长n的增长, 氮的孤对电子转向主要与烯醛链共轭,键长rC3-N11 却由1.410 Å是逐渐缩短到1.401Å,同时扭角q由28o减小到7.3o。 这与共轭稳定的原理是矛盾的。第二个是, 根据有机化学基本原理和基本的因果关系,全平面构象是共轭效应最强的构象,空间效应是分子扭曲的驱动力。 但是,能量最优的构象(q =28o)是却一个最拥挤的构象. 空间效应成了分子扭曲的阻力,它的扭曲驱动力却来自分子内的轨道作用。第三,共轭效应应该有利于分子的共平面,但是在分子1-5-(m,n) 中,萘环本身也发生扭曲,萘环中的原子不再共平面. 因此,共轭稳定的基本原理和基本的因果关系式可以质疑的。为此,有必要全面地研究分子构象和它的扭曲驱动力,有必要重新认识共轭效应与分子构象之间的因果关系。
其实,早在20世纪70年, Epiotis就指出,7a
“molecules which exist preferentially in a “crowded” geometry are not
mere aberrations of an order dominated by “steric effect”. Indeed, in
some classes of molecules, preference for “crowdedness” seems to be the
rule rather than the exception. 也正如Epiotis 所说的,这种现象促进了他对几何异构体的研究. 同样,也促进了我对有机化学基本理论问题的研究. 最终,我建立了新的s-p能量分解的方法,在有机化学基本理论问题的研究中,提出了新的观念.
附件1-3 (Appendix 1-2).
The Geometrical Data for 1-5-(1,0) Optimized at B3LYP/6-31G*

附件1-4 (Appendix 1-2)
Geometrical Data for Naphthene Optimized at B3LYP/6-31G*

(第二章. 二苯乙烯类分子的构像和分子的扭曲驱动力,待续)
参考文献
1.(a) Ingold, C. K. Structure and Mechanism in Organic Chemistry, Cornell University Press, New York, 1953.
2.Vollhardt,
K. P. C.; Schore, N. E. Organic Chemistry, third Edition, W. H. Freeman
and Company, New York, 1999; (b) Neckers, D. C.; Doyle, M. P. Organic Chemistry, John Wiley & Sons, Inc. New York, 1977.
3.Bally, T.; Haselbach, E.; Lanyiova, S.; Marschne, F.; Rossi, M. Helv. Chim. Acta 1976,59,486.
4.(a)
Burgi, H. B.; Dunitz, J. D. Helv. Chim. Acta, 1971, 54, 1255; (b) Choi,
C. H.; Kertesz, M. J. Phys. Chem. A, 1997, 101, 3823; (c) Kuze, N.;
Ebizuka, M.;Fujiwara, H.; Takeuchi,H., Egawa, T.; Konaka, S. J. Phys. Chem. A, 1998, 102, 2080.)
5.Gould,E. S.Structure and mechanism in Organic Chemistry,Holt-Dryden Book-Henry Holt Co.New York,1960; (b) March, J. Advanced Organic Chemistry, John Wiley & sons Inc. , New York, 1992.
6.Dewar, M. J.S.The PMO Theory of Organic Chemistry,McGra-Hill,New York,1969.
7.(a) Epiotis, N. D.; Cherry, W. R.; Shaik, S.; Yates, R.; Bernardi, F. Topics in Current Chemistry; Springer: New York, 1977; Vol. 70; (b) Epiotis, N. D. Lecture Notes in Chemistry,Vol. 34,Spinger-Verlag,New York,1983,p.360; (c) Eplods, N. D.Deciphering the Chemical Code,New York:VCH Publishers lnc 1996:263-284.
8.(a) Woodward, R. B.; Hoffmann, R. Acc. Chem. Res., 1968, 1 (1), pp 17–22;(b) Woodward, R. B.; Hoffmann, R. The Conservation of Orbital Symmetry, Academic press Inc,1970.
9.(a)蒋明谦,有机化合物的同系线性规律,科学出版社, 北京,1984;(b) 蒋明谦,共轭基团结合效应, 科学出版社,北京,1987.
10. (a)蒋明谦,虞忠衡, 结构化学,1981,2,121.;(b) 蒋明谦,虞忠衡, 分子科学与化学研究,
1982, 65.
11. Doller, E.; Forster, T.; Renner, H. Z. Physik. Chem. (Frankjurt), 1958, 15, 34.
12. 蒋明谦, 虞忠衡, 戴萃辰,中国科学B辑,1989,19,566.
13. (a) Bai, C. L.; Yu, Z. H.; Fu, H.; Tan, Y. Q. J. Struct. Chem. 1984, 1, 65; (b) Bai C. L, Yu, Z. H.; Fu, H.; Tan, Y. Q. J. Struct. Chem. 1984, 1, 69.
14. Houk,K. N.; Domelsmith.L. N.; Strogier, R.; Patterson, R. T. J. Am. Chem.Soc.1978,100,6531.




