在生物监测中用HPLC-HG-AAS和HPLC-ICP-MS测定砷和锑
在过去的20年中,环境和生命科学领域物种的活性研究重点集中在一些有机消解化合物及氧化态上,其中研究最多的是砷类。尽管U.S.EPA指出锑及其化合物是主要的污染物之一,但在环境和生物监测方面没有引起足够的重视。本文比较了从生物基体中提取砷类和锑类的提取效率,并且从环境和生物监测角度描述了两种与高效液相色谱在线联用方法进行砷类和锑类在物种成长过程中的形态检测的步骤。
In the last 20 years, speciation activities in environmental and life sciences have been focused mainly on the analysis of a few organometallic compounds and oxidation states, one of the most widely studied being arsenic. Even though antimony and its compounds have been listed by the U.S. EPA as priority pollutants, Sb speciation analysis in the environment and biomonitoring has received relatively little attention. This article presents a comparison of the extractability of As and Sb species from biological matrices. Also covered are two different detection principles that have been coupled on-line with HPLC separations of As and Sb species for the purpose of determining speciation patterns in specimens arising from environmental and human biomonitoring.
对环境和人类工作场所采取现代监测措施包括了合适的生物指示剂的系统分析。在环境监测过程中,能够获得从非生物的环境样品如空气、水、沉积物或土壤的检查中不能推断出的环境状态及其随时间变化的信息。对生物圈的分析也允许研究人为污染物转移到植物、动物,最后转移到人体的情况。在生物监测中,选择生物有机体,称作生物指示剂,通过对现象结果的观测(针状植物减少,植物叶颜色消失等),或者通过己成为标本的化学组分的测量来监测污染物。后面提到的方法在生物监测中是基于对合适的生物指示剂的化学分析以及在分析人体样品(主要是血和尿)过程中发现它的配对物。用于环境监测的标本在组成上具有非常多的种类。显然对这么复杂生物样品的痕量和次痕量分析要求可靠的分析程序应有重大的发展。此外,由于需要评价走向信息,总元素浓度(像金属和非金属)的测定是不完全的。人们重视目标化合物的特性,如转移和分配行为、生物有效性、化学活性和毒性。这些都是基于元素的氧化态、键合形式以及键合对,也就是基于它们的物种形成。
最近几年里,在痕量元素分析领域中,许多分析方法已指向物种形成。最近,国际理论化学和应用化学学会(IUPAC)对物种形成分析的定义是“鉴别和测量一种或多种特殊化学物种量的分析活动”,后面解释为“一种元素的特殊形态被定义为分子、络合物、核结构或氧化态”[1]。
近20年来,环境和生命科学中物种形成活性研究主要集中在分析一些有机非生物化合物和氧化态上。最多的是对元素砷的研究,主要感兴趣的是砷(m)和砷(v)的无机络合物、甲基砷酸(MMA)、二甲基砷酸(DMA)。根据现有的毒理学知识可知,对这些化合物的分析程序和对应的化学标准物是可靠的。最近,对生物样品中砷类研究方法的很大发展,主要是通过多种色谱分离技术与电感锅合等离子体-质谱(ICP-MS)检测联用[2]取得的。
美国EPA把锑及其化合物列为主要污染物。尽管如此,在环境和人类生物监测样品中,对Sb物种形成的分析几乎无报道。最近报道了一篇关于当前对锑物种形成分析的综述文章[3]。大多数的研究进展是通过在线色谱和ICP-MS联用分析得到的。但是这种分析的主要问题是将实际样品转化成分析用的溶液,这就是主要成分的提取步骤。此外,分析结果依赖于定量程序的可靠性。同全元素测定方法相比,进行元素物种形成分析不仅缺少合适的参考资料”[4],也缺少独立的分析方法。
为此本文给出了从生物基体中提取砷和锑的比较;同时,为了测定样本中由于环境和人类生物监测而产生的不同型式,本文也给出了两种不同的在线HPIC分离As和Sb的测定方法。
1实验部分
1.1仪器
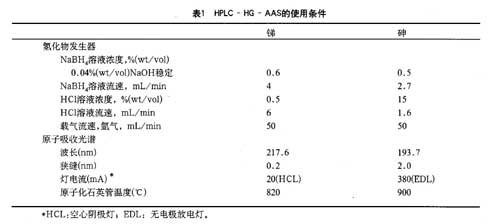
HPLC系统:一个不合金属的L-6220型智能泵(Merck KGaA,Darmstadt,Gennany)和一个不合金属的六通进样阀(Rheodyne,Rohnert Park,CA)以及用聚醚醚酮(PEEK)材料制作的20μL或100μL的进样环。两根阴离子交换柱(PRP?X100,250×4.1mm i.,Hamilton,Reno,NV;ION-120,120×4.6mm i.d.,CetacTechnologies Inc.,Omaha,NE)及一根阳离子交换柱(Nucleosil 5SA,250×4.0mm i.d.,Machery-Nagel,Duerell,Germany)用于色谱分离,流速在1.0mL/min到1.5mL/min之间。每个柱子都与它相应的保护柱同时使用。所有与流动相接触的色谱仪器管路都填充PEEK材料。用一个横向气流喷雾器,一个带有膜去溶剂化作用的超声波喷雾器(U-6000AT+,CetacTechnoIogies Inc.),一个液力高压喷雾器(HHPN),把色谱系统的洗脱液吸入ICP。MS(Elan 5000, PerkinElmer, Shelton, CT)等离子区,或者让其流过氢化物发生器。对于高效液相色谱?氢化物发生器。原子吸收光谱(HPLC-HG-AAS),把HPLC在线连接到原子吸收光谱仪(PerhnElmer 4100)上,以前已有报道[5]。75As和121Sb的质谱仪信号用ICP-MS的时间。分辨率软件以1 point/sec的速率记录。为了区分40Ar35Cl对75As信号的影响,需要附加测量质荷比为77的40Ar37Cl。由HPLC-ICP-MS测量得到的色谱数据用Origin 5.0(Microcal Software,Inc.,Northampton,MA)处理,由HPLC-HG-AAS测得的时间。分辨率数据用Turbochrom® 4.12软件(PerkinElmer)来评价。 HPLC-ICP-MS和HPlC-HG-AAS所用的详细条件分别如表1和表2所示。
1.2试剂和标准样品
用于分离的溶液都用MilliQ(Millipore,Milford,MA)水配制。分离Sb(Ⅲ)和Sb(Ⅴ)的流动相为乙烯基二胺?四乙酸(pull朋.p.a?,FIuka,Neu-Ulm,Switzerland),分离TMSbCL2和Sb(Ⅴ)用碳酸氢氨(Fluka,Mlcroselect)和酒石酸(Fluka,Microselect)作为流动相。根据文献[7],分离尿中的砷化合物用8mmol/L的磷酸氢钠-二水分子(Merck KGaA)和8mmol/L的磷酸二氢钠?单水分子(Merck KGaA)作为流动相,用正磷酸(85%,分析纯,Merck KGaA)调节pH为6.0。HPLC-ICP-MS分离砷用2%(vol/vol)的甲醇和30mmol/L的吡啶(analytical reagent grade,Merck KGaA)作为流动相,用甲酸调节pH为3.0。
将适量的酒石酸砷钾(Sigma Aldrich Chemie,Steinheim,Germany)和六氢氧化砷钾(FIuka)分别溶于高纯水中,配制为l00mg/L的储备液。TMSB是Hans J.Breuning博士(University of Bremen,Bremen,Germany)捐赠,将它用水溶解配制成100mg/L的标准储备液。
砷储备液中应含有1000mg砷/L,对于每种化合物的配制如下:砷(Ⅲ)是将0.264g As2O3(sigma Aldrich)溶解在200mL 0.2%NaOH(Suprapur ®,Merck中;砷(Ⅴ)来自于Titrisol ®安瓿(As2O5溶于水中,Merck);DMA是将0.286g的二甲基砷酸(Na-salt, dihydrate,>99%, FIuka)溶解于100mL MUhQ水中。储备液(每一份均为1000mg/L)的偶砷甜菜碱(AB)、四甲钾离子(Tetra)和MMA是Walter Goessler博士(Institute of Chemistry,Karl-Franzens University,Graz,Austria)捐赠的。所有的储备液均用聚乙烯瓶存放在冰箱中,温度为6℃。这些溶液至少在6个月内是稳定的。砷(m)溶液每两个月需重新配制。用于测量的溶液根据需要每天要用适量的MilliQ水溶解。
1.3样品和提取步骤
尿样品是来自两位未接触电池的和两位职业生产电池的工人(捐赠者为Karl-HeLnz Schaller,University of Erlangen-Numberg, Erlangen,Germany),把它们收集到无Sb的聚乙烯试管中。此外,分析了两种冻干的尿样参考样品SRM 2670(NIST,Gaithersburg,MD)和Seronorm Bakh No.403125(NyCOm劝,Oslo,Norway)。根据样品加工人员的推荐,两种冻干的尿样参考样品用高纯水重新配制。分析前,所有的尿样都要保存在4℃。
尿样进色谱柱前需要稀释和过滤两步预处理。根据尿样中砷和锑的浓度,用流动相将样品从l+1稀释到l+49。样品在进色谱柱前经过0.2μm Minisart RC 25过滤器(Sartorius,Gottingen,Germany)过滤。
研磨成粉(0.1?1g)的冻干样品(极地树叶,松干,云杉干来自Environmental Specimen Bank of the Research Center Juelich,Juelich,Germany)在聚乙烯的试管中用9mL 0.2mol/L的乙酸提取,在室温下振荡24h。提取液在室温下以3000r/min的速度离心,然后取上层清夜4mL,根据以前报道的方法[8]进行矿化。在处理液中砷和锑的总浓度由流动注射(F1)-HG-AAS检测。大约2.2g的常见蚌类和马尾样品用20mL的甲醇/水(9:1,vol/vo1)、CHCl3或者离子化表面活性剂十二烷基硫酸钠(SDS,1%vol/vol)在室温下提取24h。用含有蛋白酶固体(Sigma,酶的活性:0.7?1.0单位/mg固体;100mg蛋白酶/mL NH4HCO3缓冲液,pH为7.5)或者纤维素酶(Sigma,酶的活性:最低为0.3单位/mg固体)的溶液在37℃提取锑24h。对所有的提取混合物都进行振荡。提取液以17000r/min的速度进行超离心,进行FI-HG-AAS检测总的锑样品前上层清液需要过滤。
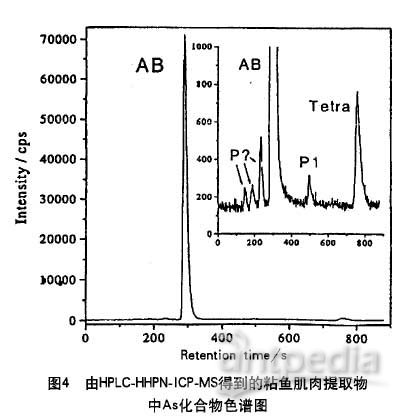
HPLC-ICP-MS进行定量分析新的砷样品(约5g)是用30mL甲醇/水(9:1,vol/v01)从粘鱼肌肉中提取的,然后以17000r/min的速度离心[9]。进一步清洗和甲醇挥发后,进色谱柱前提取物用高纯水配制到10mL。
2 结果和讨论
2.1 砷和锑的提取效率
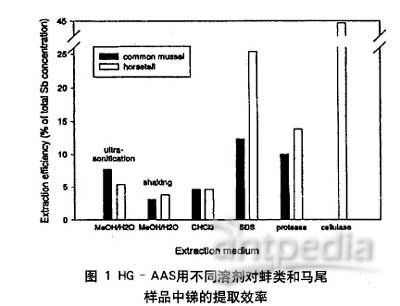
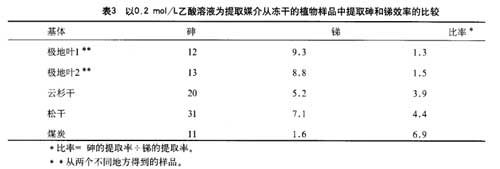
从蚌类和马尾样品中提取锑的效率如图l所示,表3列出了用0.2mol/L的乙酸从不同的植物基体中能提取总的砷和总的锑的百分比[10]。结果显示出从植物基体中提取锑比提取砷要困难得多。用有机溶剂或乙酸提取砷的效率小于10%,而用甲醇/水(9:1,vol/vol)从蚌类和其它海产品样品中提取砷的效率可达到90%[11],并且用同样的步骤从植物基体中提取砷的效率也高于锑(表3)。从冻干的极地叶子中提取砷的效率比锑约高40%,在松干、云杉干中提取砷的效率比锑高4倍。从煤中提取砷的效率比锑高7倍。用SDS能够提高锑的提取效率,特别是从马尾中提取(图1)。用纤维素酶提取能使提取效率高43%,对不用纤维素酶提取的蚌类样品也进行了实验。到目前,关于锑和酶之间的反应机理没人知道。例如,用酶打断Sb-C键,能将锑从基体中脱离出来,但可能改变了物种信息。因此,在生物领域,用酶提取锑的研究需要进行更深入的实验。
对于锑的物种形成研究来说,锑的提取效率差是当前的一个主要问题,因为大部分有关锑的信息都保留在样品内。但通过进一步优化酶的提取步骤可以帮助解决这一问题。
2.2 HPLC-HG-AAS检测砷和锑化合物
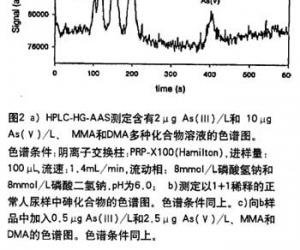
HPLC分离了含有多种砷类的溶液,其中包括2μg As(Ⅲ)/L,10 LtgAs(Ⅴ)/L,MMA和DMA,结果见图2a。对一位未接触电池的人的尿样以l+1的比例稀释后进行分离,结果见图2b。在这个尿样中DMA为主要的砷化合物,另一种主要砷类化合物是氧化三甲肿(TMAO), As(Ⅲ)和MMA都是痕量。在图2c,已向尿样中加人了一定量被检测的砷化合物。色谱不能将四甲基砷离子与As(m)完全分离,并且几乎接近方法的检测限。ICP-MS是非常适合检测特殊元素的检测器,能够提供低的检测限(表4)。HG-AAS作为低消费的特殊元素的检测器,可用来检测砷感染的工人的尿样。用HG-AAS非常适合,由于感染的工人尿样中砷浓度明显高于正常尿中砷(约l0μg总As/L)。用HPLC-HG-AAS检测化合物已有详细的报道[5],其中包括色谱图和基本的仪器优化参数。

2.3 用HPLC-ICP-MS测定砷和锑化台物
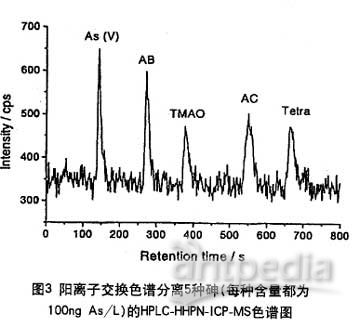
ICP-MS特殊元素检测器明显地改善了检测限,特别是使用超声波喷雾器(USN)或HHPN这种高效导入样品的仪器的时候。另外,还能够检测不能形成氢化物的化合物(例如偶砷甜菜碱),这一点可由图3证实。图3说明HPLC-HHPN-ICP-MS能够在非常低的浓度时检测到砷。
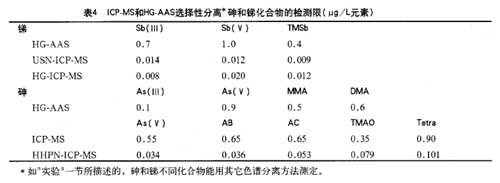
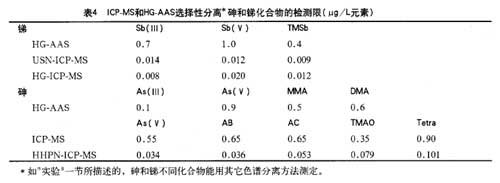
各种仪器对砷和锑的检测限(μg/L)如表4所示。HPLC-HG-AAS的检测限在μ/L范围,从As(Ⅲ)的0.11μg/L到Sb(Ⅴ)的1.0μg/L。还可由HPLC-HG-AAS和HPLC-ICP-MS的比较看出,如果在液相分离柱之后连接USN-ICP-MS,测定锑化合物的检测限大约降低l00倍。对砷而言,这些改善是非常小的,使用HHPN对HPLC-ICP-MS测量仅能使砷(Ⅴ)的信号强度提高26倍。如果ICP?MS使用横向气流喷雾器,测定砷类化合物的检测限与HPLC-IPC-MS及HPLC-HG-AAS就具有可比性。具有高的离子传送量及低的检测噪音的新型ICP-MS仪器检测砷能使ICP。MS优于HG-AAS,特别是使用Meinhard或横向气流喷雾器时。
在作者实验室中,用阳离子交换色谱分离As(Ⅴ)、DMA、AB、偶砷胆碱(AC)、氧化三甲肿(TMAO)和用阴离子交换色谱分离As(V)、As(Ⅲ)、AB、DMA、MMA都有很大的进展。反相色谱用来分离偶砷糖。这些步骤用于从海产品(贝类,粘鱼肌肉,海鸥蛋,泡叶藻)中提取砷化合物。检测结果说明贝类、粘鱼肌肉、海鸥蛋中AB是砷的主要化合物。泡叶藻中主要含有偶砷糖。
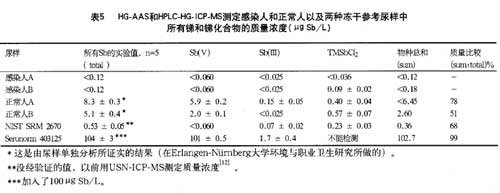
用最近发展起来的HPLC-HG-ICP。MS方法来分离检测尿样中的Sb(Ⅲ)、sb(Ⅴ)、TMSbCl2,结果如表5所示。具体的检测过程已有描述[13]。直接接触电池的人的尿样中锑的总含量几乎比正常人高100倍。他们主要接触三氧化锑和SbH、。令人惊奇的是,两位工人的尿样中主要的锑化合物是TMSbCl2和Sb(V),而非Sb(Ⅲ),sb(Ⅲ)的含量非常低(表5)。众所周知,Sb(m)形成氧化物的几率比Sb(Ⅴ)高10倍,说明在人体中可能是通过氧化作用将Sb(Ⅲ)转化成Sb(Ⅴ)或通过生物甲基化作用将其转化为TMSbCl2。Sb(Ⅴ)和Sb(Ⅲ)的生物作用及短柄帚霉的真菌作用方法最近已经建立[14]。
3结论
测定生物监测样品中的砷和铅化合物需要一系列有力的分析方法。根据我们感兴趣的问题,即以样品中的所有元素的含量为出发点,选择和设计了分离和检测联用技术。生物监测很重要的一个方面是由在有机物研究中不同的非金属种类的影响水平所决定。另外,分析物的稳定性以及它们在整个分析过程中可能出现的变化都应该考虑[15]。分析方法的特殊要求也有一定的影响,例如,在HG-AAS检测中形成氢化物的效率和完全程度或者在ICP-MS检测中色谱流动相组成对喷雾器的适合性。
目前,锑化合物的提取效率一般都低于砷化合物的提取效率。用酶可明显提高锑化合物的提取效率,今后应该对它进行深入的研究。HPLC-HG-AAS对砷和锑化合物的检测限为ng/L级。而对生物基体中砷和锑化合物需要更低的检测限。ICP-MS能够满足这个要求,特别是使用高效率喷雾器时。此外,对物种研究来说,HPLC-ICP-MS能够检测不能形成氢化物的元素类。
参考文献:
- Templeton DM, Ariese F, Comelis R, et al. Guidelines for terms related to chemical speciation and fractionation of elements. Pure Appl Chem 2000; 72: 1453-70.
- Caruso JA, sunon KL, Ackley KL, eds. Elemental speciation.Amsterdam: Elsevier, 2000.
- Krachler M, Emons H, Zheng J. Speciation of antimony for the 21st century: promises and pitfalls. Trends Anal Chem 2001 ; 20:79-90.
- Emons H. Challenges from speciation analysis for the development of biological reference materials. Fresenius J Anal Chem 2001; 370:115-19.
- Krachlet M, Emons H. Potential of high performance liquid chromatography coupled to now injection hydride generation atomic absorption spectrometry for the speciation of inorganic and organic antimony compounds. J Anal At Spectrom 2000; 15:281-5.
- Jabukowski N, Feldmann I, Stuewer D, Bemdt H. Hydraulic high-pressure nebulization-Applicatibn of a new nebulization system for inductively coupled plasma mass spectrometry. Spectrochim Acta B 1992; 47: l 19-29.
- Begerow J, Dunemann L, Snr R. In: Angerer J, Schaller KH, eds. Analyses of hazardous substances in biological materials, vol. 7. Deutsche Forschungsgemeinschafi (DFG).Weinheim, Germany: Wiley-VCH, 2001 :97-l 17.
- Krachler M, Burow M, Emons H. Development and evalnation of an analytical procedure for the determination of antimony in plant materials by hydride generation atomic absorption spectrometry. Analyst 1999; 124:777-S2.
- Falk K, Emons H. Speciation of arsenic compounds by ion-exchange HPLC-ICP-MS with different nebulizers. J Anal At Spectrom 2000; 15:643-9.
- KracNer M, Emons H. Extraction of antimony and arsenic from fresh and freeze-dried plant samples as determined by HG-AAS. Fresenius J Anal Chem 2000; 368:702-7.
- Fath K. Arsenic speciation in biological environmental samples of aquatic ecosystems by using HPLC-ICP-MS.Ph.D. thesis. University of Essen, Germany, 1999. ISSN 0944-2952.
- Krachler M, Alimonti A, Petrucci F, Forastiere F, Caroli S. Innuence of sample pre-treatment on the determination of trace elements in urine by inductively coupled plasma mass spectrometry. J Anal At Spectrom 1998; 13:701-5.
- Krachler M, Emons H. Urinary antimony speciation by HPLC-ICP-MS. J Anal At Spectrom 2001; 16:20-5.
- Andrewes P, Cullen WR, Feldmann J, Koch I, Polishchuk E, Reimer E. The production of medlylated organoantimony compounds by Scopulariopsis brevicaulis. Appl Organomet Chem 1998; 12:827-42.
- Emons H. Speciation in the frame. of environmental biomonitoring-challenges for analytical and environmental sciences. In: Ebdon L, PiHs L, Comelis R., Crews H, Donard OFX, Quevauviller P, eds. Trace element speciation for environment, food & health. Cambridge: Royal Society of Chemistry, 2001 : IS8-95.
TAG: 生物监测砷锑hplc-hg-aashplc-icp-ms