气相色谱- 质谱联用系统分析食品中的丙烯酰胺
摘要:最近,科学家们在油炸和烤制的食品中检测到了丙烯酰胺,其含量比水中的允许含量高出很多倍,这一问题引起了卫生保健团体的广泛关注。研究表明当氨基酸和糖一起被加热到水的沸点以上时,即可能生成丙烯酰胺。本文介绍了一种用于检测食品中丙烯酰胺的分析方法。
GC-MS Approaches to the Analysis of Acrylamide in Foods
Berngard Rothweiler, Eberhardt Kuhn and Harry Prest
Abstract: The recent discovery of acrylamide in fried and baked foods at levels many times higher than those permitted in water, was a concern in the healthcare community. It appears that acrylamide is formed when amino acids and sugars are heated together at higher temperatures than boiling water. This paper describes an analytical method that can be used to study the occurrence of acrylamide in a wide variety of food.
2002年4月,瑞典国家食品监督局的科学家们宣称,他们在油炸和烤制的食品中检测到丙烯酰胺,其含量比水中的允许含量高出很多倍,这一结果表明实际情况甚至比预计情况还要严重[1-3]。众所周知,丙烯酰胺是一种神经毒素,并有潜在的致癌作用。世界卫生组织(日内瓦,瑞士)规定:水中丙烯酰胺的允许最高含量为0.5μg/kg。然而,一些食品,例如炸薯条,炸土豆片,脆面包片和其他常见的油炸食品中丙烯酰胺的含量高达100-1000 μg/L。虽然食品的原材料中不含有丙烯酰胺,非油炸食品中丙烯酰胺的含量也低于检测限。最近的研究表明加热过程中氨基酸和糖会发生Maillard 反应生成丙烯酰胺[4]。对于相对高含量丙烯酰胺这一问题的关注引发了各种食品中丙烯酰胺含量的研究。
1 分析方法
许多仪器分析的方法已经被用于丙烯酰胺的研究。近来,采用液相色谱- 串联质谱技术的丙烯酰胺检测限可以达到50 μg/kg (ppb),利用75-55 m/z 转化能够得到更好的效果,这一技术能够简化了样品的前处理过程。以电子轰击质谱为检测器的气相色谱方法只能分析相对分子量较低的分子,因此需要对样品作衍生化处理。本文探讨了一种选择性气相色谱质谱(GC/MS)方法,不但能够提供准确的定量结果,并且能够进行快速筛选。这是一种用于检测食品中丙烯酰胺的快速、便捷的方法。
1.1 气相色谱-质谱-选择性离子扫描(SIM)正离子化学电离模式下的快速筛选
图1 给出了利用电子轰击质谱得到的丙烯酰胺质谱图。从图中可以看出,有三种粒子的质谱峰- m/z 71,55 和44。这些离子峰的强度说明低于毫微克级的样品可以被检测,但是在分析食品样品时这些离子可能会与基质发生相互干扰。氨正离子化学电离质谱能够提供选择性更好的电离,而且能够在食品分析中发挥比电子轰击质谱更大的作用(见图2)。氨正离子化学电离质谱产生两个离子- m/z72,质子化的分子离子峰,[M+H]+ 和m/z89,复合分子的离子峰,[M+NH4]+。正离子化学电离质谱对于丙烯酰胺的分析具有很好的选择性和灵敏度,皮克级的样品也能够被检测到。定量曲线的线性范围在100pg-10ng 之间。
1.2 样品前处理
用于快速筛选的正离子化学电离质谱具有增强的分析能力,因此采用非常简单,而且快速的样品前处理方法(图3)就可满足要求。食品样品粉碎均匀后,取0.4g 样品放置到离心管中,然后加入1mL 甲醇/水(9:1,体积比)混合溶液,超声提取10min。超声前,1μg13C3 标记的丙烯酰胺加入到1 mL 溶液中。超声提取后,样品经8000rpm 离心5min。将上层清液轻轻倒出,并转移到样品瓶中,作为气相色谱- 质谱- 选择性离子扫描(SIM)的待测样品。
2 筛选方法的结果和讨论
图4 是一种白面包提取物的质谱图。从基线可以看出,由于氨正离子化学电离质谱具有很好的选择性,丙烯酰胺峰附近的基线干扰非常小。丙烯酰胺的定量结果为浓度约34ng/ mL 或84ng。由于丙烯酰胺在氨基酸和糖被一同加热时产生,因此其也有可能在进样口处生成。为了验证这一假设,向白面包提取液中加入100ng 丙烯酰胺后重新分析,得到的结果为135ng(或者185ng/g),这表明由于压力脉冲的存在,较低的温度和短的接触时间减缓了进样过程中丙烯酰胺的形成,或者说进样口处几乎不产生丙烯酰胺。但是,在其他提取物或者分析条件下,也可能不是这种结果。
2.1 气相色谱-质谱联用系统分析丙烯酰胺衍生物
水提,原位衍生加液液萃取[6,7]也是从食品中提取丙烯酰胺的有效手段。这种方法首先用热水按照g:10mL 的比例提取粉碎均匀的样品中的丙烯酰胺,并在提取液中加入强溴代试剂,将丙烯酰胺转化为2,3- 二溴代丙酰胺。添加硫代硫酸盐除去过量的溴代试剂后,对溶液进行离心或者过滤处理。采用乙酸乙酯萃取,2,3- 二溴代丙酰胺通过液液分配被提取到有机相。进一步处理该衍生物的一种选择是生成更稳定的化合物,2- 溴代丙酰胺。化学反应过程如图5 所示。甲基丙烯酰胺,CH2=CH(CH3)CONH2,经常作为测定回收率的标记物,因此也许对其特性加以讨论。具体的实验方案可参考文献[8]。
3 结果和讨论
3.1 电子轰击电离
两种溴代丙烯酰胺衍生物的质谱图很相似。在电子轰击电离模式下,2,3- 二溴代丙酰胺失去一个溴取代基形成C3H5ONBr 离子,这与预测的单溴衍生物同位素丰度相符。三乙基胺(碱)的存在使得分子在溶液中失去HBr基团,形成单溴取代的C3H4ONBr 分子,与二溴代衍生物相比,分子中多一个氢原子,在电子轰击质谱图中显示为一个分子离子峰。在两张质谱图中都能够观察到C2H3Br 离子峰,这也解释了m/z105.9 和107.9 两个碎片峰的形成过程。由于13C3- 丙烯酰胺在质谱图产生C2H3Br m/z107.9,可以将其作为内标,用于丙烯酰胺Bernhard Rothweiler等:气相色谱-质谱联用系统分析食品中的丙烯酰胺的定量测定。与单溴代丙烯酰胺衍生物相比,二溴代丙烯酰胺衍生物在质谱中具有更高的响应值,但是由于广泛存在于溶剂和食品包装中的邻苯二甲酸盐的干扰,使得这类衍生物不显示m/z149 碎片峰。在EI-SIM 中,两类化合物在10-500pg/ μL 范围内都有很好的线性响应,但是二溴代丙烯酰胺衍生物具有更好的质谱检测性能,而且能够在较高的温度下洗脱,因此被更多关注。然而,人们很早就观察到2,3- 二溴代丙酰胺在进样口会分解为2- 溴代丙酰胺,分解过程与进样口的活性存在一定的相关性。可以采用双锥型衬垫进行二溴代丙酰胺的分析,而用木质的锥型衬垫进行单溴代丙酰胺的分析。在二溴代丙酰胺的分析中必须采用13C 标记物以校正其分解,而在单溴代丙酰胺的分析中采用甲基丙烯酰胺可以很好地对回收率加以校正。
3.2正离子化学电离
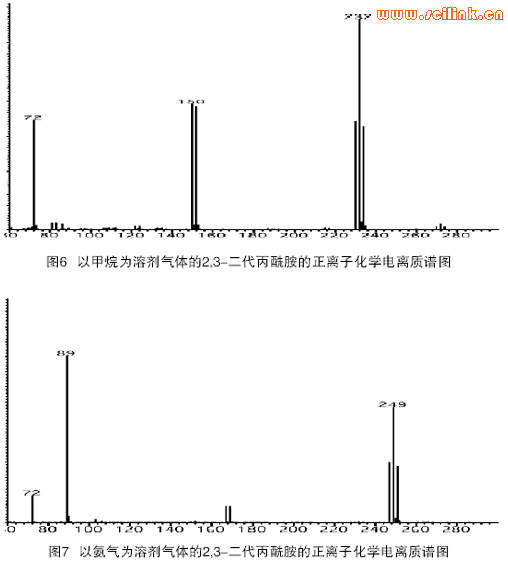
以甲烷和氨气为溶剂气体的2,3 - 二溴代丙酰胺的正离子化学电离质谱图分别在图6和图7中给出。在甲烷中,丰度最高的质谱峰为[M+H]+,而在氨气中,丰度最高的质谱峰为[M+NH4]+。由于以甲烷为溶剂气体可以得到更高的响应,对于一些背景特别复杂的样品中丙烯酰胺的定量测定,采用甲烷可以得到更好的效果。两类溶剂气体的定量线性范围都在10-500pg/ μL(R2>0.998)。在正离子化学电离模式下,较低分子量的碎片峰m/z72(甲烷为溶剂气体)和m/z89(氨气为溶剂气体)不能用于SIM 的定量测定。这些碎片显然来自于溴分子的消去反应,不能反映待测离子的实际状况。
与在电子轰击质谱中的情况类似,在正离子化学电离模式下,以甲烷或氨气为溶剂气体,2,3- 二溴代丙酰胺的响应值比2- 溴代丙酰胺高。以2- 溴代丙酰胺为分析对象,在甲烷中,丰度最高的质谱峰为[M+H]+,而在氨气中,丰度最高的质谱峰为[M+NH4]+。
4 结论
由于在很多食物中发现有丙烯酰胺存在,目前已经出现了很多分析方法。正离子化学电离是一种简单,快速,高灵敏,直接检测和定量丙烯酰胺的方法。以溴代丙酰胺作为标记物,二溴代丙酰胺在鉴定和定量方面表现出比2- 溴代丙酰胺更优越的性能。对于某些不适合电子轰击质谱分析的样品,正离子化学电离质谱是个很好的替代方案。以甲烷为溶剂气体响应值比氨气高两倍。通过添加合适的内标物,可以校正二溴代丙酰胺分解造成的误差。甲基丙烯酰胺内标可以很好应用于回收率的计算。以炸土豆片为对象的实验数据说明了这种方法的特点。
参考文献
-
H ileman B. Swedish researchers report acrylamide found in starchy foods. Chem Eng News 2002:38.
-
Hileman B. Acrylamide worries experts. Chem Eng News 2002;80(27):9.
-
Hileman B. Acrylamide found in cooked foods. Chem Eng News 2002; 80(19):33.
-
Yarnell A. Acrylamide mystery solved. Chem Eng News 2002;80(40):7.
-
Rosen J, Hellenas KE. Analysis of acrylamide in cooked foods by liquid chromatography tandem mass spectrometry. Analyst 2002;127(7): 880-2.
-
Castle L, Campos MJ, Gilbert J. Determination of acrylamide monomer in hydroponically grown
tomato fruits by capillary gas chromatography/ mass spectrometry. J Sci Food Agric 1991;54 (4):549-55. -
Castle L. Determination of acrylamide monomer in mushrooms grown on polyacrylamide gel.
J Agric Food Chem 1993; 41(8):1261-3. -
Rothweiler B, Kuhn E, Prest H. Gas chromatography/mass spectrometry approaches to the
analysis of acrylam ide in foods. Agilent Technologies, appl note 5989-0602EN,2004.
TAG: