Make it EVIDENT
本期推出【FV3000 Makes Yeast Evident】

东南大学电子科学与工程学院 MEMS教育部重点实验室
酿酒酵母与复制寿命检测
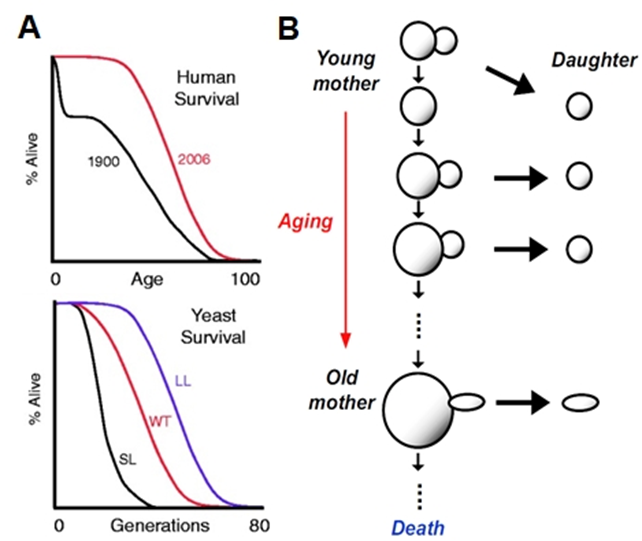
B 酵母细胞复制寿命示意图[2]
酵母细胞复制寿命的传统测量手段是基于1959年提出的微解剖法,即利用微解剖针手动剔除培养板上单个酵母细胞产生的每代子细胞,从而得到复制寿命。该方法具有效率低、周期长、样本量小、对细胞易造成损伤等缺点。
而微流控芯片可利用微结构实现酵母单细胞的捕获,利用流体力剪切去除子细胞,为酿酒酵母自动化高通量单细胞培养和高时空分辨率监测提供可能,但有如下局限:
现有微流控芯片在细胞捕获稳定性、子细胞剪切效率、复制寿命检测精确性等方面都有待于提高;
现有微流控芯片较少关注大体积、随机出芽的双倍体酵母细胞的捕获培养和寿命检测。
显微成像技术在课题研究中的作用
该论文研制的高通量酿酒酵母单细胞捕获-培养-解剖微流控芯片,与奥林巴斯FV3000激光扫描共聚焦显微镜双剑合璧,成功实现对双倍体酿酒酵母母细胞的可靠捕获和子细胞的一致性剪切,进而实现稳定的长期培养和完整的复制寿命检测研究。


 A 微流控芯片沟道实物图
A 微流控芯片沟道实物图针对不同“瓶身”长度,时序图像显示在母细胞较小时,捕获结构容易捕获上游剪切下的细胞。而母细胞接近凋亡时,由于体积增大,子细胞旋转至“瓶颈”的成功率降低,朝向“瓶身”上游生长的子细胞会将母细胞拖拽造成样本丢失。根据统计的母细胞稳定保持的比例,最终确定“瓶身”长度优化值。

A 4小时内微捕获阵列中的空结构实现“自填充”
B 4小时内单细胞捕获效率提升
C 较短“瓶身”的捕获结构,朝向上游的子细胞将母细胞拖拽造成样本丢失
D 较长“瓶身”的捕获结构,易捕获上游剪切下的细胞
接下来,研究人员在高通量单细胞长时间培养过程中,通过视频拍摄观测并验证了母细胞在初始出芽时的动态旋转,并在芽稍大时重新定向至“瓶颈”处,且停止旋转直到胞质分裂完成后被解剖分离。通过时序成像,验证了母细胞在多代子细胞之间,面临随机的出芽位点依然能够实现稳定的“瓶颈”定向和子细胞剪切。
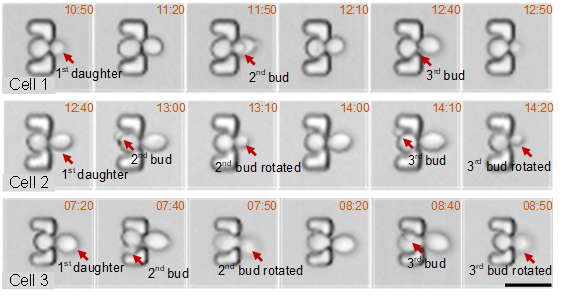 以10分钟时间间隔的时序成像过程中,上一代子细胞被成功剪切后下一代芽随即旋转至“瓶颈”中(三个样本分别为相邻出芽、相对出芽、随机出芽三种模式)。
以10分钟时间间隔的时序成像过程中,上一代子细胞被成功剪切后下一代芽随即旋转至“瓶颈”中(三个样本分别为相邻出芽、相对出芽、随机出芽三种模式)。同时,酿酒酵母的细胞周期在其寿命内的分布也呈现一定规律。细胞在完成第一个细胞周期的用时比接下来5代用时略长,而接下来的复制寿命里,各代周期皆相对平稳,只在临近死亡的最后几代中急剧上升。选取样本并将其每个细胞周期使用不同颜色的长条标出,从而将细胞群体间的异步化结果变得可视化。
结果表明,细胞在前8至10代以内,细胞周期在细胞相互间保持有相对的同步性,随着细胞不断衰老,细胞间的异质化现象逐渐明显。临近细胞死亡时,细胞的周期被拉长,且细胞间差异逐渐扩大。

A 双倍体酿酒酵母细胞的复制寿命曲线
B 不同时间点下,母细胞所产生的子细胞被空捕获结构捕获后的复制寿命
C 酿酒酵母细胞的平均细胞周期(出生对齐)
D 酿酒酵母细胞的平均细胞周期(死亡对齐)
E 细胞周期分布图
该研究后续工作包括利用卷积神经网络深度学习算法实现酵母细胞的复制寿命、细胞周期、生长速率等关键生理指征参数的高效智能分析,成功解决酵母细胞衰老过程中的表型分析问题,为酿酒酵母复制寿命及其衰老相关形态变化完整关联性图谱的构建提供可能,并在杂合性缺失、沉默信息调控等双倍体细胞独有的寿命调控模式研究上具有广泛的前景。
在成像样品制备以及图像采集中的注意事项
参考文献
[1] Smith, J., Wright, J., & Schneider, B. L. (2015). A budding yeast''s perspective on aging: The shape I''m in. Exp Biol Med, 240(6), 701-710.
[2] Lee, S. S., Vizcarra, I. A., Huberts, D. H. E. W., Lee, L. P., & Heinemann, M. (2012). Whole lifespan microscopic observation of budding yeast aging through a microfluidic dissection platform. Proc Natl Acad Sci USA, 109(13), 4916-4920.


