ADC药物开发进度缓慢 新技术有望为其加上一个风火轮
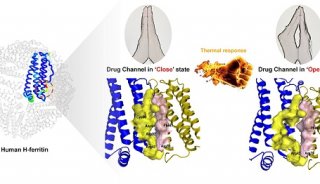
莱布尼茨分子药理研究所(FMP)和慕尼黑路德维希马克西米利安大学(LMU)研究人员在著名期刊Angewandte Chemie 上发表名为Ethynylphosphonamidates for the Rapid and Cysteine‐Selective Generation of Efficacious Antibody–Drug Conjugates最新研究结果,该研究团队为实现更有选择性和更有效地治疗癌症而开发一项创新技术,其将蛋白质和抗体转化为稳定、功能强大的药物转运蛋白,进而更精准检测和杀死肿瘤细胞,使得ADC更安全有效。
ADC药物发展困境
化学药物治疗通常伴有严重的副作用,在多数情况下,能够除去肿瘤的药物剂量对于患者来说毒性太大,随着生物医药技术的发展,为解决类似这样的问题,肿瘤选择性抗体连接的药物组成的抗体-药物偶联物(ADC)应运而生,抗体可以通过细胞表面的变化将癌细胞与健康组织区分开来,它们将细胞毒性分子的高效力与单克隆抗体的肿瘤特异性结合起来,与标准化学疗法相比,ADC具有显着拓宽治疗范围的潜力。
然而,这些ADC在通往癌细胞途中丢失了大部分有毒货物,其一旦被释放到血液中,就会引起危险的副作用,因此,药物和抗体之间的稳定联系是发挥其长期功效的关键因素。
目前批准上市的ADC药物
2000年,由辉瑞开发的第一个抗体偶联药物Mylotarg被FDA批准用于治疗急性粒细胞白血病,但完整的抗体偶联药物因在血液不稳定而导致致死性毒性产生,因此,被迫于2010年撤市,然而,在2017年,Mylotarg获得再度FDA批准,将其用于治疗新确诊的CD33+成人急性髓性白血病和对初始治疗无应答的2岁以上儿童的难治性CD33+成人急性髓性白血病。辉瑞也是同时拥有2款ADC药物的企业。
2011年,武田与Seattle Genetics联合开发的Adcetris获得FDA批准用于治疗霍奇金淋巴瘤。
2013年,罗氏的Kadcyla获得FDA批准用于治HER2阳性转移性乳腺癌患者
2017年,惠氏/辉瑞的Besponsa获得FDA批准用于单药治疗复发或难治性的CD22+成人B细胞前驱急性淋巴细胞白血病。
此外,2019年3月21日,上海医药首次公示恩美曲妥珠单抗B003临床试验方案,该I期临床计划在HER2阳性的乳腺癌患者中展开。
严格来说,自第一个ADC药物上市的以来,目前有4款ADC药物获批上市,偶联技术、靶向性、有效性等受限问题依然是导致开发难度增加的主要原因,不少公司也在研发该类药物上栽了跟头,因此要真正发挥ADC药物的抗癌效力,将药物在体内选择性地输送到作用部位是亟待解决的问题。
突破困境,将有望新生
据该研究人员MarcAndréKasper说道,新的药物转运蛋白能够降低ADC用药剂量、减少其带来严重副作用,我们开发了一项新技术,使天然蛋白质抗体与药物的连接变得更加容易,稳定性也比以往更好。
在该研究中,研究人员发现了不饱和磷化合物在连接抗体与化学药物上的突出特性,膦酰胺酸盐连接了所需的修饰 ,例如,专门针对蛋白质或抗体中的半胱氨酸,半胱氨酸是非常罕见且天然存在的氨基酸,因此可以非常有效地控制每个蛋白质的修饰数量,这对于构建药物缀合物是很关键的,此外,膦酰胺酸盐可以很容易地掺入复杂的化合物中。
Marc-AndréKasper说道:“新方法的最大成就哪怕是在血液循环过程中结合也是稳定的,市场上的ADC无法做到这一点。”
为了测试靶向给药的适用性,研究人员将他们的技术与已被FDA批准的ADC药物Adcetris进行了比较,使用相同的抗体和活性剂尽可能精确地重建药物,其中唯一的不同是新技术应用创新的膦酸酰胺键,当应用于血清时,研究人员观察到他们改良的ADC在一段时间内,活性成分明显减少。
此外,还在小鼠实验中使用这项新技术来对抗霍奇金淋巴瘤,事实证明,这种制剂比传统药物更有效,根据其结果,与酰胺酰胺相关的药物转运蛋白可以以较低的剂量给药,并且可以进一步减少副作用。
结语
该技术在替代现有方法上具有巨大潜力,也有望在未来开发更有效和更安全的ADC,下一步,该研究小组将继续努力开发基于膦酰胺的ADC。
目前这项临床前研究已经开始,此外,去年获得莱布尼茨创业奖的初创公司Tubulis将进一步将其发展为成熟的市场平台。