杨朝勇团队:外周血中循环肿瘤细胞分析检测的新方法
探索发展肿瘤诊断、治疗的新技术、新方法已经成为我国亟待解决的关键科学问题之一。组织活检作为肿瘤诊断的金标准可为病例提供组织学结构判断,然而存在侵入性强、易产生并发症、采样偏差性大、取样难及滞后性等局限。而液体活检具有损伤小、代表全、易取样、快速等优点,可在肿瘤初期诊断、预测复发、监测治疗效果等方面很好地补充组织活检。液体活检目前主要包括:循环肿瘤DNA、循环肿瘤细胞(Circulating Tumor Cell,CTC)、外泌体。CTC是指从原发或转移灶中脱离出进入外周血循环的肿瘤细胞,因CTC能提供完整的细胞生物学信息,相对于其它标志物更能全面系统地反映肿瘤病灶的分子病理信息,已成为目前最具发展潜力的肿瘤无创诊断和实时疗效的监测手段之一。
由于在每毫升外周血中CTC一般是以几个到几十个细胞存在于几亿个血细胞之中,临床进行CTC高效捕获犹如大海捞针、挑战巨大。针对这一瓶颈,杨朝勇教授团队提出了基于流体力学分离与仿生多价识别的微流控芯片多尺度协同捕获富集的新策略。
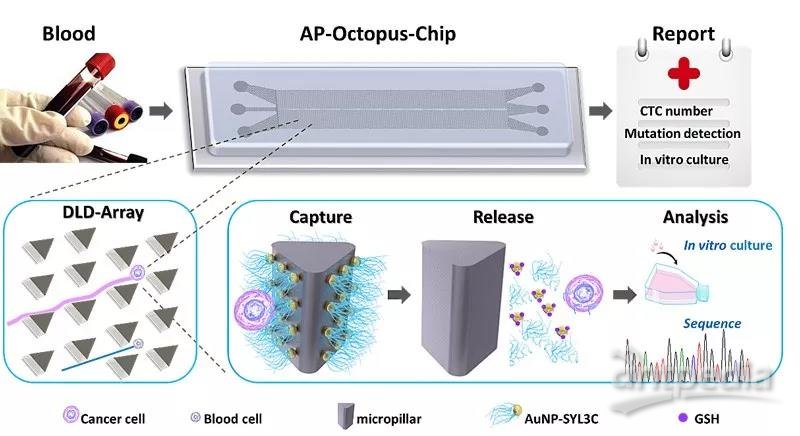
图示:仿生章鱼芯片工作原理图。外周血可直接通入芯片,肿瘤细胞不断与三角形微柱碰撞并被章鱼状探针抓获,而血细胞直接穿过而不被保留。被抓获的肿瘤细胞可被无损释放,用于下游用药筛选、DNA测序分析等,为临床提供精准的分子水平信息。
研究团队设计的仿生章鱼微流控芯片由上万个修饰有可以特异捕获CTC的核酸适体的微柱构成,这些微柱阵列根据确定性侧向位移方式排列,可在微米尺度上实现细胞尺寸选择性流体力学调控。CTC尺寸普遍大于血液细胞,因此CTC可与微柱反复碰撞,从而增加被核酸适体捕获的机率,而血液细胞因尺寸较小沿液流方向运动,从而减少与微柱碰撞而避免被误抓。
在纳米尺度上,每个微柱表面布满了金纳米颗粒,且每个金纳米上修饰了上百条核酸适体分子。相比于单价核酸适体,金纳米上的多条核酸适体由于多价效应,使靶细胞捕获效率提高3倍,解决了单价核酸适体在实际应用中亲和力不足的问题。此外,捕获后的细胞可以通过加入富含巯基且生物相容性好的谷胱甘肽分子进行配体交换反应,破坏核酸适体和金纳米连接的金硫键,从而保证了CTC无损释放。释放后的细胞活性可以达到95.8%,可以实现下游的细胞培养及基因突变检测。
通过对41例正常、前列腺癌、结肠癌临床样本的盲测,该团队验证了所发展的芯片技术,仅需1 mL外周血就可以有效区分肿瘤患者和正常人,对肿瘤患者的检出率可以达到100% (38/38),其中包括T1N0M0分期样本,并且通过谷胱甘肽配体交换释放机制,真实样本中CTC释放相率可达到75%以上。该工作在肿瘤分期诊断、动态监测、疗效评估、药物开发和预后监测等方面具有广阔的应用前景。
这一成果近期以内封面论文发表在Angew. Chem. Int. Ed. 杂志上,文章的第一作者为宋彦龄博士。
该论文作者为:Yanling Song, Yuanzhi Shi, Mengjiao Huang, Wei Wang, Yang Wang, Jie Cheng, Zhichao Lei, Zhi Zhu, Chaoyong Yang