液相色谱-串联质谱法测定强化食品中叶酸的含量
方案优势
该方法在0.05~100 ng/mL 浓度范围内线性关系良好,定量下限为0.01~0.5 mg /kg,回收率为72.0%~109%,相对标准偏差(RSD) 为3.8%~11.8%。该方法简单快速,灵敏度、准确度和精密度均能满足强化食品中叶酸的测定要求。
采用标准
相关标准
方法/原理/步骤
样品前处理(下述提取步骤,均须避光进行。)
1.果汁饮料称取2g试样于10mL容量瓶中,加入40μL 50μg /mL内标液(甲氨蝶呤)和100μL1mg/mL BHT溶液,用水定容至刻度后过膜待测。
2.大米、果冻、饼干称取2g试样于10mL容量瓶中,加入40μL50μg/mL内标液和100μL 1mg/mL BHT溶液,用0.01mol/L盐酸溶液溶解并定容至刻度,涡旋混匀1min,超声15min,4000 r /min离心10 min,过膜待测。
3.含乳饮料称取2g试样于10mL容量瓶中,加入40μL50μg/mL内标液和100μL 1mg/mL BHT溶液,用4%三氯乙酸溶液溶解并定容至刻度,涡旋混匀1min,超声15min,4000 r/min离心10min,过膜待测。
4.奶粉称取5g试样于离心管中,加入200μL50μg/mL内标液和500μL1 mg/mL BHT溶液,用25mL45~50℃水溶解并涡旋混匀1 min,超声15 min。待溶液温度降至室温后,用5 mol/L盐酸溶液调节至pH 1.90±0.5,放置2min,再用5mol/L氢氧化钠溶液调节至pH 4.7±0.5。将溶液转移至50mL容量瓶中,用水定容至50mL,超声10min,4000r/min离心10min,过膜待测。
仪器条件
1.色谱条件
Waters HSS T3色谱柱( 50 mm×2. 1 mm,1.7μm) ;进样量5μL;柱温30℃;流动相:A为10 mmol /L乙酸铵( pH 6. 3)水溶液,B为甲醇;梯度洗脱程序: 0~1 min保持B为1%;1~4min,B从1%升至55%; 4~6 min保持B为55%; 6~6.1 min,B降至1%; 6.1~10 min保持B为1%。
2.质谱条件
大气压电喷雾离子源,正离子电离模式。毛细管电压3.5kV;喷雾压力45psi;气帘气流量5L/min;鞘气流量10L/min;鞘气温度350℃;毛细管温度350℃;定性离子对: m/z442.4→176.9,碰撞能量33eV;定量离子对m/z 442.4→295.1,碰撞能量21eV;甲氨蝶呤m/z 445.0→308.0,碰撞能量20eV。
结果与讨论
1.基质及内标物的选择
依据GB14880-2012《食品安全国家标准食品营养强化剂使用标准》,按照可强化食品的不同类别选择并确立6种代表性食品:果汁、奶粉、含乳饮料、大米、饼干和果冻。
通过大量查阅国内外文献,选取D4-烟酸、D4-烟酰胺、乙酰苯胺、马尿酸、甲氨蝶呤及33C5-叶酸放射性同位素内标等6种内标,对其安全性及定量结果的准确性进行比较,最终选择甲氨蝶呤作为内标物。
2.叶酸的稳定性实验
叶酸在酸性溶液中热不稳定,在碱性溶液中易被氧化,水溶液遇光迅速分解,因此需要通过控制溶液所处的环境改善叶酸储备液的稳定性。分别用水、1%氨水、5mgVc、0.01 mol/LHCl(pH 2.0)、0.01mol/L HCl(pH 5.0)、25μLβ-巯基乙醇、1%BHT、10 mmol /L乙酸铵和3%偏磷酸等不同溶剂配制浓度为100μg/mL的标准溶液,并将配制好的溶液用铝箔做避光保护,4℃冰箱中储存。测试不同溶剂不同时间段的峰面积并进行比较,得到叶酸的稳定性曲线图
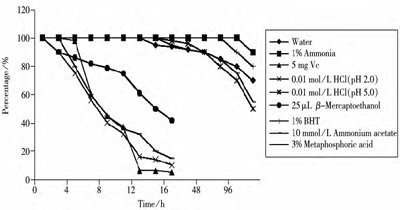
叶酸的稳定性曲线图
由图可知,叶酸在强酸条件下容易分解,当采用0.01 mol/L HCl(pH 2.0)和3%偏磷酸作为溶剂时,叶酸标准溶液分解现象十分明显;采用水、0.01 mol/LHCl(pH =5.0)和10mmol /L乙酸铵作为溶剂时,溶液在16h内稳定性较好,基本无分解,16~48h出现缓慢分解,48h后分解现象十分明显;当采用1%氨水溶解叶酸时,1~4d内无分解,在第5d分解了10%,因此叶酸标准储备液在1~4d内具有良好的稳定性,能够满足定量分析实验要求。同时,比较了Vc、β-巯基乙醇和BHT 3种抗氧化剂的抗氧化效果,发现添加BHT的溶液在72 h内基本无分解,因此样品前处理过程中加入BHT,能够避免叶酸的氧化,有利于稳定性的提高。
二丁基羟基甲苯( BHT)的优化
由于叶酸的不稳定性,实验过程中需要加入BHT避免叶酸的氧化。用0.01 mol/L HCl溶液配制浓度为100μg/mL的储备液,常温下放置12h后,比较了不同质量分数BHT溶液(0.1%,0.5%,0.8%,1.0%,1.2%,1.5%,2.0%)对叶酸稳定性的影响。对新配制的叶酸储备液进行检测,此时得到的峰面积数据认为无损失,记为100%;然后分别取含不同浓度BHT的叶酸溶液进行检测,得到各标准储备液的峰面积,将此峰面积与新配制溶液得到的峰面积进行比较;以BHT含量为横坐标,百分比为纵坐标,得到各标准储备液的稳定性数值如图。结果发现,随着BHT用量的增多,叶酸的分解速度变慢,稳定性提高,但当达到1%时,溶液中的叶酸趋于稳定,因此实验选取加入1%的BHT作为抗氧化剂。

BHT 使用量对反应的影响
仪器设备
高效液相色谱仪
高效液相色谱仪的系统由储液器、泵、进样器、色谱柱、检测器、记录仪等几部分组成。储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱(固定相) 内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中做相对运动时,经过反复多次的吸附- 解吸的分配过程,组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器,样品浓度被转换成电信号传送到记录仪,数据以图谱形式打印出来。