II型糖尿病研究需要使用的动物模型介绍
今天师兄告诉我,如果我们实验室要研究糖尿病,应该主要研究2型糖尿病,这让我听到之后愣在了那里,原来在研究糖尿病上面我还年轻着呢(暗自说道)。
那,2型糖尿病是不是也需要相对应的动物模型来支持研究呢?师兄能帮忙讲讲嘛?(我厚着脸皮问道)。
当然了,研究2型糖尿病怎么能少得了其相关的动物模型呢?你上周已经掌握了1型糖尿病模型的相关知识,下面就来和你说说一些常见的2型糖尿病模型吧。
糖尿病主要分为1型和2型糖尿病,其中2型糖尿病约占90%,已经成为继癌症、心血管疾病之后的第三大严重威胁人类健康的重大疾病,因此对其研究也越发重要,理想的动物模型是研究疾病病理和治疗疾病的关键。
2型糖尿病简介
2型糖尿病(Type 2 diabetes, T2D)主要表现为胰岛素相对不足或胰岛素分泌正常但存在胰岛素抵抗,血糖升高。超重、高血压、血脂异常、年龄增加、工作压力大、高热量饮食等是诱发2型糖尿病的主要因素。
常见2型糖尿病动物模型
建立2型糖尿病的动物模型的主要发生机制是引发胰岛素抵抗和(或)β细胞功能障碍为主,主要包括以下几种模型:
①单基因肥胖模型,如常见的ob/ob和db/db大小鼠,ZDF大鼠;
②多基因肥胖模型;
③饮食诱导模型,主要指高脂饲料诱导型;
④其他非肥胖型模型;
⑤其他β细胞功能障碍模型。
如下表1所示,列举了上述常见的糖尿病模型,诱导机制及应用。接下来我们就经典的糖尿病动物模型作详细介绍。

表1. 2型糖尿病啮齿动物模型
一
单基因肥胖模型
单基因肥胖模型如上表所示主要包括:ob/ob和db/db小鼠,ZDF大鼠,Mc4r KO大小鼠等。其中ob/ob和db/db小鼠目前已经成为应用最为广泛的2型糖尿病模型,下面以它们为主作详细介绍。
1. ob/ob和db/db大小鼠
ob/ob小鼠:即Lepob/ob,是瘦素(Leptin, Lep)基因纯合突变的小鼠。
Leptin为肥胖基因(ob)编码产物,是脂肪细胞分泌的蛋白质类激素,在调节能量平衡、摄食行为起重要作用。若ob基因突变,食欲大增,体重剧增,产生严重的肥胖特征,多用于肥胖症的研究。
db/db小鼠:即Leprdb/db,代表瘦素受体(Leptin receptor, Lepr)基因纯合突变的小鼠。Lepr,又名OBR,是由db基因编码产物,为Leptin受体。若Lepr缺失,导致高血糖症和胰岛素抵抗症,有类似ob/ob小鼠症状,现已广泛用于肥胖和2型糖尿病的研究。
模型特征:2周时,超重和食欲大增,开始出现高胰岛素血症;
4周时,明显高血糖,血糖浓度继续上升,峰值在3-5个月;
期间伴随代谢异常包括高脂血症,严重肥胖、多食、易渴、多尿、体温调节紊乱和活动能力下降。
注意:该纯合子小鼠是不育的。
模型判定:4周龄后检测血糖,空腹血糖>7mmol/L,餐后血糖>11.1~16.7mmol/L。
数据展示:如下图所示为邦耀实验室构建的Lepr基因点突变大鼠数据[1]。
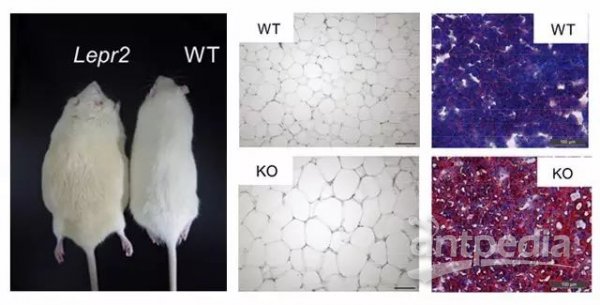
图1. Lepr点突变大鼠表型特征。 左:突变鼠和野生鼠的体型特征;右:在组织学水平对脂肪组织和肝组织染色的结果[1]
应用范围
① 肥胖症:抑制食欲,能量消耗研究;
② 糖脂代谢:如高血脂症,2型糖尿病的胰岛素抵抗的治疗;
③ 肝肾疾病:肝硬化,脂肪肝,糖尿病肾病;
④ 生殖发育,如不孕不育症;
⑤ 免疫炎症,肥胖和糖尿病都伴随着炎症的加剧;
⑥ 代谢综合征;
⑦ 糖尿病的并发症治疗。
2. MC3R、MC4R大小鼠模型
基因功能
黑皮质素受体3(Melanocortin-3 receptor, MC3R)和黑皮质素受体4(Melanocortin-4 receptor, MC4R)属于视紫红质样G蛋白偶联受体家族。
MC3R主要表达在中枢神经系统,调节能量平衡;
MC4R广泛表达于整个中枢神经系统,也表达于外周组织,如脂肪组织,MC4R参与调节摄食行为和能量消耗,并且MC4R基因的突变是单基因肥胖的人类最常见的原因。Mc4r和Mc3r敲除(KO)大鼠小鼠模型现已作为糖尿病和肥胖的动物模型,广泛应用在疾病病理研究和药物开发中。
模型特征
如表2所示, Mc3r KO大鼠食欲增加,脂肪量增加,体重却减轻,没有糖尿病症状;Mc3r KO小鼠基本与大鼠表型一致。Mc4r KO小鼠显示出肥胖,饮食过多,高血糖和高胰岛素血症;
Mc4r和Mc3r-Mc4r双敲除(DKO)大鼠和Lepr大鼠一样,均食欲过强,在4周开始出现肥胖症、胰岛素抵抗,血糖和瘦蛋白水平升高,诱发糖脂代谢紊乱和糖尿病并发症。
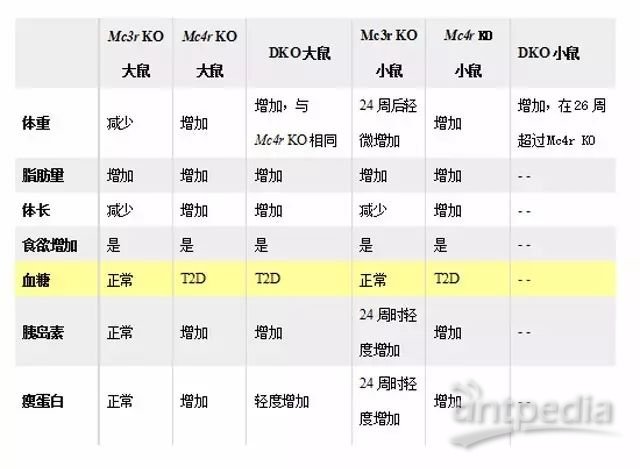 表2. 黑皮质素受体敲除大小鼠的表型比较
表2. 黑皮质素受体敲除大小鼠的表型比较
邦耀实验室技术团队首次利用CRISPR-Cas9技术敲除SD大鼠,并繁殖得到三种基因敲除大鼠(Mc3r KO、Mc4r KO 和双KO Mc3r Mc4r),并通过确定其各自的表型,比较了他们之间表型的异同。
其中Mc3r-/-为中心型肥胖的动物模型,Mc4r-/-是模拟2型糖尿病及全身性肥胖的代谢综合征,而Mc3r/Mc4r双基因敲除模拟重度2型糖尿病兼全身性肥胖的代谢综合征。如图2所示,相关报道发表在并在《Scientific Reports》[2]。

图2. Mc3r-/-,Mc4r-/-和Mc3r-/-Mc4r-/-大鼠体型和餐后血糖比较示意图[2]
应用范围
② 糖脂代谢,如2型糖尿病的胰岛素抵抗的机制研究和治疗;
② 肥胖症,增加能量消耗,影响脂肪合成,开发减肥产品;
③ 中枢神经系统调节机制研究,尤其黑皮质受体家族系统研究;
④ 代谢综合征的研究与治疗;
⑤ 肝肾疾病:肝硬化,脂肪肝,慢性肝炎;
⑥ 糖尿病并发症的预防与治疗,如糖尿病肾病,糖尿病足等;
⑦ 免疫炎症;
⑧ 药物研究与开发。
3. ZDF大鼠
ZDF (Zucker Diabetic fatty) 大鼠是被广泛认可的先天遗传性2型糖尿病和肥胖病的动物模型,来源于Zucker肥胖大鼠(Zucker fatty rats, ZF),ZDF大鼠没有ZF大鼠肥胖,但具有更严重的胰岛素抵抗和β细胞凋亡。
应用范围
① 2型糖尿病、葡萄糖不耐症、高胰岛素血症,如雄性瘦素受体缺失ZDF大鼠(ZDF/CrlCrlj);
② 心血管疾病,如早期微血管病变;高血脂症;肥胖症。
除了上述常用到的基因突变的大小鼠,饮食诱导的糖尿病模型,也同样广泛应用于2型糖尿病的研究。
二
饮食诱导肥胖模型
特点:需要制备或者购买高脂饲料,饲料代价昂贵,造模需要周期较长,但造模相对简单。
1. 单纯高脂饲料诱导
高脂饲料诱导肥胖模型在模拟人类2型糖尿病发病病因独具优势,尤其模拟了肥胖合并糖尿病病人的发病特点,不会由于化学药物诱导导致体内重要器官受损,广泛用于各种病因病理研究(肥胖症、非酒精性脂肪肝、高血脂症、心血管等疾病),特别是营养过剩和肥胖的2型糖尿病研究中。
2. 高脂饲料+STZ
高脂饲料+STZ诱导模型与单纯高脂饲料诱导模型相比,造模周期缩短,成模率高,多用于2型糖尿病药物筛选和评价的动物模型。
下面以高脂饲料+STZ诱导型模型为例介绍其构建方法(以ICR小鼠为例):
① 8-10W小鼠喂养Research Diets 公司的60%高脂饲料(high fat diet,HFD)至少3周,诱导胰岛素抵抗;
② 小鼠饥饿5~12h后,腹腔注射 80 mg/kg(其他相似剂量也可以)的STZ(Sigma)诱导部分胰岛素分泌障碍;
③ 一般2~3天检测空腹血糖水平和餐后血糖水平,衡量血糖是否升高;
③ 体重相同、符合标准的糖尿病小鼠即可用于下一步实验。
如图3所示,邦耀实验室已成功建立该模型并用于药物筛选评价[3]
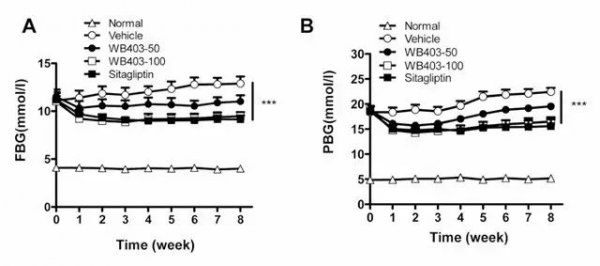
图3. 成功构建HFD/STZ小鼠并用于药物筛选。 A,B分别是药物治疗8周内的空腹血糖(FBG)和餐后血糖(PBG) [3]
三
糖尿病其他药物靶点模型
除了我们上述提到的动物模型外,另外陆续报道也发现了一些潜在的糖尿病药物靶点[4-8],目前我们实验室已成功构建了部分相关小鼠模型,如G蛋白偶联受体家族:GPR35、GPR40、GPR119、GPR120、GPR131(TGR5)、GPR146、GPR162等,均有研究表明,它们与糖尿病的发生发展有着密切关系。现以TGR5举例说明:
TGR5与肥胖、糖尿病以及代谢综合症相关,目前已确定为潜在糖尿病药物靶点,而且TGR5激动剂已成为潜在的抗糖尿病治疗药物,如我们实验室发表文章《A Novel TGR5 Activator WB403 Promotes GLP-1Secretion and Preserves Pancreatic β-cells in Type 2 Diabetic Mice》结果显示TGR5激动剂可以刺激TGR5使肠内皮细胞分泌GLP-1控制血糖水平,增加能量消耗,改善β细胞功能,达到降低血糖的功能,如图4所示[3]。
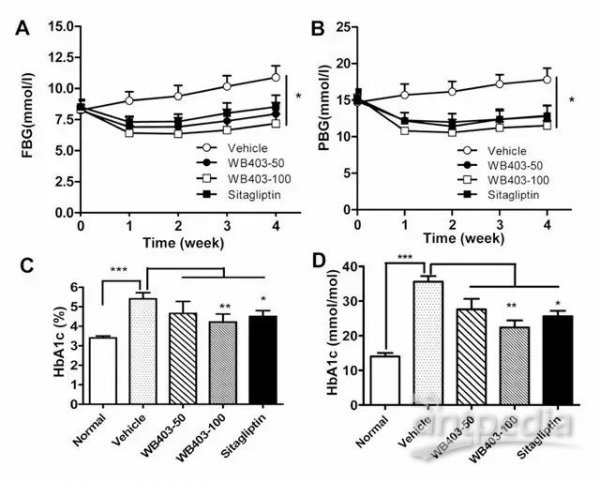
图4. TGR5激动剂在db/db糖尿病小鼠的降糖效果。A,B分别是治疗4周的空腹血糖(FBG)和餐后血糖(PBG),C,D是血清的糖化血红蛋白(HbA1c)水平[3]
综上所述为2型糖尿病研究中应用最广泛的几类动物模型,回顾一下主要包括基因突变类(ob/ob和db/db小鼠,Mc4r KO大小鼠及ZDF大鼠等)及高脂饲料诱导的模型等。
目前邦耀实验室利用CRISPR/Cas9技术已经成功构建上述几类基因突变和高脂饲料诱导的2型糖尿病模型,并发表了高影响力的文章[1-3],如果您的实验室从事糖尿病相关研究,您对糖尿病研究有任何疑问或者需要相关模型,可以与我们联系,我们竭诚为您提供最准确的动物模型,为您的研究助力!
参考文献
[1] Chen Y, Lu W, Gao N, et al. Generation of obese rat model by transcription activator-like effector nucleases targeting the leptin receptor gene[J]. Science China Life Sciences, 2016: 1-6.
[2] You P, Hu H, Chen Y, et al. Effects of Melanocortin 3 and 4 Receptor Deficiency on Energy Homeostasis in Rats[J]. Scientific Reports, 2016, 6.
[3] Zheng C, Zhou W, Wang T, et al. A novel TGR5 activator WB403 promotes GLP-1 secretion and preserves pancreatic β-cells in type 2 diabetic mice[J]. PloS one, 2015, 10(7): e0134051.
[4] Divorty N, Mackenzie A E, Nicklin S A, et al. G protein-coupled receptor 35: an emerging target in inflammatory and cardiovascular disease[J]. Frontiers in Pharmacology, 2015: 41-41.
[5] Steneberg P, Rubins N, Bartoovshifman R, et al. The FFA receptor GPR40 links hyperinsulinemia, hepatic steatosis, and impaired glucose homeostasis in mouse[J]. Cell Metabolism, 2005, 1(4): 245-258.
[6] Rayasam G V, Tulasi V K, Davis J A, et al. Fatty acid receptors as new therapeutic targets for diabetes[J]. Expert Opinion on Therapeutic Targets, 2007, 11(5): 661-671.
[7] Kolar G R, Grote S, Yosten G L, et al. Targeting orphan G protein-coupled receptors for the treatment of diabetes and its complications: C-peptide and GPR146.[J]. Journal of Internal Medicine, 2016.
[8] H A R, Hong E, Sanchezmunoz F, et al. Expression of the orphan receptors GPR22, GPR162, GPR27 and GPR17 in cardiovascular tissues of diabetic rats (1051.7)[J]. The FASEB Journal, 2014.