食用植物油中溶剂残留的测定方法(顶空进样器)
摘 要
关键词 溶剂残留, 顶空进样, 气相色谱,氢火焰电离检测器。
1.前言
食用油的加工生产通常有精炼、压榨、浸出3种方法, 其中利用适当的有机溶剂将植物组织中的油脂提取出来, 然后脱去溶剂并回收溶剂, 这种浸出法较先进, 出油率比压榨法高出3%或更高, 故倍受生产企业的青睐。目前, 国内多数食用油生产厂家已采用此种工艺过程。此种工艺虽然优点多, 但也有局限性。生产的油脂虽然虽经脱去溶剂处理, 但仍有少量溶剂残留在油脂中。我国浸出油生产使用的溶剂是石油的低沸点馏分, 是一种以六碳烷烃为主要成分的烷烃、环烷烃、芳香烃的混合物, 故统称六号溶剂。其主要成分正己烷是一种麻醉呼吸中枢的溶剂。因此, 从毒理学及生产工艺水平两方面综合考虑, 国家标准规定浸出油中溶剂残留量不得超过50m gökg, 并且同时规定了标准的检测方法。
本文采用顶空进样, 毛细管气相色谱分离, 氢火焰电离检测器(FID)检测, 以正己烷为标准溶液定量的方法, 对食用油中溶剂残留量的检测进行了研究。通过气2质联用仪, 分析出食用油中溶剂残留主要的六碳烷烃除正己烷外, 还有甲基环戊烷(见图1), 2-甲基戊烷(见图2), 3-甲基戊烷(见图3), 因此本文还比较了这3种六碳烷烃在定量分析中与正己烷的相对标准偏差。
2. 实验部分
2.1试剂
正己烷, 分析纯;N,N2二甲基己酰胺(简称DM A), 分析纯; 空白植物油: 置于70℃烘箱中烘
24h。
2.2 仪器
广州国创分析仪器有限公司GC6890气相色谱仪, DK300顶空进样器.
2. 3 顶空分析条件
平衡温度: 50℃, 定量环温度: 60℃, 传输温度: 70℃, 循环时间: 10m in, 平衡时间: 30m in, 加压时间: 0. 05m in, 定量环充满时间: 0. 15m in, 定量环平衡时间: 0. 10m in, 进样时间: 1. 00m in, 进样体积: 1mL。
2. 4 气相色谱分析条件
柱温180℃, 进样口温度: 200℃, 氢火焰电离(F ID)检测器, 检测器温度: 250℃, H P-5(30m×0. 25mm×0. 25Lm)弹性石英毛细管柱, 载气为高纯氮气, 流速为4. 4mL/m in, 氢气50mLöm in, 空气流速为450mL/m in, 尾吹气: 15mL/m in, 分流比: 1∶1。
图1 正己烷的色谱图
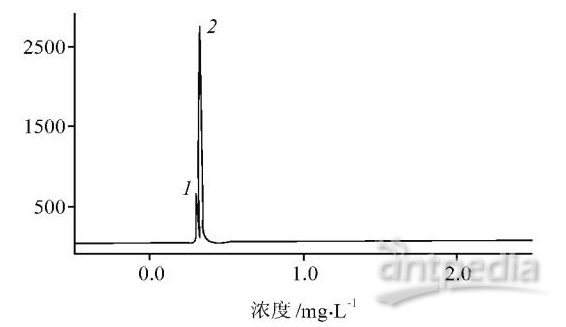
1——正己烷; 2——N,N2二甲基己酰胺(DM A)。
2. 5 标准溶液的配制
用移液管取1mL正己烷于100mL容量瓶中,以DM A定容, 摇匀备用, 作为标准贮备液。取5mL空白植物油到5个平衡瓶中, 用微量注射器分别取10、20、30、40、50LL标准贮备液到5个平衡瓶中, 放入顶空进样器中, 以2. 3 中的分析条件进行测定。然后, 以 浓 度 对 峰 面 积 绘 制 校 准 曲 线 如 下y =5. 9128x, r2= 0. 9982;其气相色谱图见图1。
2. 6 残留量测定
准确量取5. 00mL待测植物油到顶空平衡瓶中, 称重质量为m(g), 以2-4中气相色谱分析条件进行测定, 得到其浓度为n(mg/L), 则待测植物油中溶剂残留量n′(mg/kg)为: n′=5·n/m。
3 实验结果与讨论
3. 1 气相色谱条件的选择
因为本文采用DM A作为正己烷的溶剂, 而DM A在F ID检测器上也有响应, 所以选择的柱温不能过高; 但要使正己烷和其他3种六碳烷烃保留时间一致, 柱温也不能过低。本文比较了3种柱温: 80、180℃和250℃, 结果表明, 180℃柱温时正己烷和其他3种六碳烷烃的保留时间均为0. 807m in, 并且和DM A分离良好, 是合适的柱温。
3. 2 检出限的确定
在本实验的条件下, 正己烷的检出限为0. 001m g/L, 符合溶剂残留量检测的要求。






















