先天性糖蛋白糖基化缺陷导致的疾病
先天性糖蛋白糖基化缺陷(congenital disorders of glycosylation, CDG)是一组由常染色体隐性遗传引起的糖蛋白合成缺陷而导致的疾病,可引起一系 列临床表现[1]。糖蛋白的蛋白糖基化修饰是一个极 其复杂的过程,参与其中的酶种类繁多。糖蛋白糖 基化缺陷可累及多个脏器,如神经、造血、消化和生 殖系统等,从而引起多种多样的临床表现。该病最 早由比利时儿科医师Jaeken等于1980年首次报 道。迄今根据缺陷的酶、缺陷部位已报道有19型, 见表1。
CDG的分型
糖蛋白由糖链和多肽链组成,其糖链又有O-糖 苷键连接的糖链和N-糖苷键连接的糖链2种。CDG 患者的缺陷发生在N-糖苷键连接的糖蛋白形成过 程。根据缺陷发生的环节可分为两类:CDGI型为糖 链合成过程中及已合成的糖链与蛋白质多肽链结 合过程中发生缺陷而引起的疾病;而CDGII型为发 生在已与多肽链结合的糖链的延伸、修饰过程的缺 陷[3]。因缺陷的酶不同,两型中又各自有一些亚型, 如CDGI型内目前发现的有CDG -I a至CDG -I l, CDGII 型中有 CDG -II a 至 CDG -IIg(表 1)。由于 参与蛋白糖基化修饰的酶种类繁多,随着科学的发 展将会不断发现更多的类型。
CDG的诊断临床表现
CDG的诊断首先基于临床表现。CDG无特异性 临床表现,患者任何器官(系统)均可受累,最常见 的是神经系统。不明原因的多脏器损害,特别是合 并智力运动发育落后、斜视、小脑萎缩和凝血功能障碍时均应考虑该病可能,对患者进行详细的病史 调查与体格检查,借助实验室技术进行进一步的诊 断。以CDG -Ib型为例,致病病因为磷酸甘露糖异 构酶(phosphomannose isomerase)缺陷,患者婴儿期主要表现为反复呕吐和慢性腹泻等胃肠道症状及 肝纤维化,一些患儿由于高胰岛素血症导致低血 糖,多不伴有畸形及智力运动发育障碍。
CDG可导致的临床症状与体征:①胎儿水肿、 体重不增、小头畸形和反复感染;②皮肤损害:乳头 内陷、异常脂肪堆积、橘皮样皮肤或鱼鳞样皮肤;③ 视觉器官损害:斜视、色素性视网膜炎、视神经萎 缩、眼组织缺损、白内障;④激素水平失衡:生长落 后、性腺发育不良、青春期延迟或无、高胰岛素血 症;⑤骨骼系统:骨质疏松、挛缩性关节炎和外生骨 疣;⑥凝血障碍:血栓形成、出血倾向和静脉炎;⑦ 心脏损害:心肌病、心包积液和新生儿期心包炎;⑧ 胃肠系统异常:腹水、周期性呕吐、慢性腹泻、失蛋 白性肠病、肝脾肿大、肝炎样表现、肝脏病理检查可 见肝硬化及脂质、糖原空泡;⑨泌尿系统损害:蛋白 尿、先天性肾病综合征、微囊变和新生儿期近端肾 小管病。
实验室检查
一般实验室检查借助常规化验、影像学检 查技术,对疑似患者进行系统检查,以了解有无多 脏器受累以及受累的程度。①广泛的神经系统检 查,包括形体的发育和IQ的测定;②矫形医师的评 估;③头颅磁共振扫描(NMR);④电生理检测;⑤肾脏超声波;⑥肝脏超声波;⑦空腹血糖;⑧肾功能; ⑨肝功能;⑩内分泌系统的检测,特别是甲状腺素 (包括甲状腺球蛋白)和促性腺激素;©凝血功能检 测,包括因子K、因子XI、蛋白C、蛋白S,抗凝血因子III (ATIII)、肝素辅助因子II和补体系统;⑫全血 细胞计数,包括网状细胞;⑬基因分析。其中①、②、 ④、⑤、⑥、⑦、⑧、⑨、⑩项应定期复查,如每年或隔1年1次。
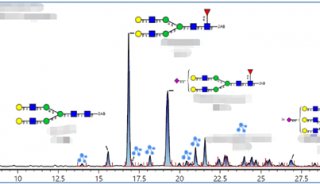
2.2.2特殊实验室检查①血液转铁蛋白(trans¬ferrins, TF)电泳:米用等电聚焦电泳(isoelectric fo¬cussing, IEF)技术进行血液转铁蛋白分析,通过免疫 固定后进行银染,可清楚地显示转铁蛋白的糖基化 不完全的条带分布,进行诊断(图1)。由于缺陷部位 的不同,患者血液转铁蛋白IEF图谱不同,因此,IEF 技术不仅有助于CDG诊断,也可对患者进行初步分 型。需要注意的是出生后1周内血液标本可能出现 假阴性。因此,IEF分析技术不能用于产前诊断。对于高危患者,应在出生后2〜3个月复查,避免误 诊。另外,酗酒、半乳糖血症和果糖不耐受症等其他 原因也可引起继发性的糖蛋白糖基化异常,患者血 液TF的IEF条带类似CDG,需进行鉴别诊断。在迄 今发现的19个型别的CDG中,CDG-IIc患者血液 TF的IEF条带与正常人相同,采用IEF不能进行诊 断。对于疑似病例,应进行其他糖蛋白(如过-抗胰 蛋白酶)分析以协助诊断[4]。②酶学分析和分子生物 学诊断:随着对CDG的认识和医学诊断技术的提 高,CDG的病因、缺陷蛋白与基因逐步明确,应用酶 学分析和分子生物学诊断技术可对患者的确诊、产 前诊断、相关家系的遗传咨询提供更多的支持。

注:脑脊液作为标准以显示转铁蛋白的各条带:正常人血清的转铁蛋白条带显示为以带4个唾液酸转铁蛋白含量最高的高 斯分布;CDGI型患儿的血清转铁蛋白则表现为带2个唾液酸和无唾液酸转铁蛋白强度增高,带4个唾液酸转铁蛋白强度减低; CDGII型患儿的血清转铁蛋白显示为除了带2个唾液酸和无唾液酸转铁蛋白含量增高外,带1个唾液酸和带3个唾液酸转铁蛋 白的含量也增高。非常清晰的条带含量分布差异可用于CDG的诊断及初步分型
3 CDG 患者的管理
多数CDG患者尚无特殊治疗方法,对症治疗颇 为复杂,需要对其病理生理有透彻的了解。CDG为 慢性进行性遗传性疾病,累及多个器官,常引起患 者及其家族心理障碍,需要综合、细致的管理。对于 智力、运动障碍的患者应给予物理治疗、语言训练; 对于合并畸形的患儿可进行矫形;随访中应定期进 行全身检查,以了解疾病进展情况并及时实施妥当 的治疗措施。
对伴有凝血障碍的CDG患者应格外加以重视, 其出血倾向和血栓形成常随病程而加重。患儿如有 中风样发作,应给予小剂量的乙酰水杨酸,剂量为 1 mg/(kg-d)。对于间歇性发病者,应注意预防脱水, 特别是伴有肠道感染者应及时静脉补液,除监测血 气、电解质和血糖外,还应测定凝血因子、蛋白C、蛋 白S和AT III。对于需要进行全身麻醉和外科手术 的患者,应注意避免禁食和脱水,通过持续静脉输 注能量合剂,尽可能缩短禁食时间。术前即使凝血 功能正常,亦应检测其他凝血因子,特别是凝血因 子K和XI,以及蛋白C、蛋白S、AT III和肝素辅助因子II。
总之,由于缺少特殊治疗方法,CDG的治疗管理是一个综合、细致的过程。可喜的是,CDG -Ib患者经口服甘露糖[1 g/(kg-d),分5次服用]治疗,可获得良好的疗效[5]。对CDG发病机制的进一步研究, 将有助于探讨疾病的治疗。
参考文献
1.Schachter H. Congenital disorders involving defective N -glyco¬sylation of proteins. Cell Mfol Life Sci, 2001, 58(8): 1085¬1104.
2.Jaeken J, Vanderschueren -Lodeweyckx M, Caesar P, et al. Familial psychomotor retardation with markedly fluctuating serum prolactin, FSH and GH levels, partial TBG deficiency. increased serum arysulfatase A and increased CSF protein: a new syndromeUPediatr Res, 1980, 14( Suppl): 179.
3Jaeken J, Carchon H. What’s newin congenital disorders of glycosylation? Eur J Paediatr Neurol, 2000, 4(4): 163 -167.
4.
Fang
J, Peters V, Assmann B, et al. Improvement of CDG diagnosis by combined examination of several glycoproteins. JInherMfetabDis, 2004, 27(5):581-590.
5.
Niehues
R, Hasilik M, Alton G, et al. Carbohydrate deficient glycoprotein syndrome type I b. Phosphomannose isomerase deficiency and mannose therapy. J Clin Invest, 1998, 101(7): 1414-1420.