SMAD2/3与TGF-β通路协同影响转录因子发生m6A RNA甲基化调...
SMAD2/3与TGF-β通路协同影响转录因子发生m6A RNA甲基化调控干细胞发育
文章导读:
胚胎干细胞作为一种全能性细胞,通过增殖和分化,产生动物体所有组织和器官的细胞。已有研究表明,胚胎干细胞发生m6A
RNA甲基化,大多与细胞增殖[1-2],免疫应答[4]关系密切。然而,对于m6A修饰在胚胎干细胞向神经内胚层细胞分化过程中的分子机制目前并没有相关报道。今天,分享一篇英国剑桥大学研究团队于2018年8月发表在Nature(影响因子:40.14)文章,聊一聊RNA甲基化在调控胚胎干细胞分化过程中的作用机制。这篇文章的开头很直接,首先通过阅读文献确定了感兴趣的基因SMAD2/3,对其进行Co-IP和质谱后,结果显示其能够与甲基化转移酶METTL3,METTL14和WTAP直接互作。他们是明星,和他们结合的分子也是明星分子,这不,在胚胎干细胞当中有研究者就发现SMAD2/3就和METTL3,METTL14结合,不出所料,这一结合在胚胎干细胞当中起到了重要作用。

欲知详情,让我们接着往下看。
文章内容:
1.SMAD2/3蛋白与METTL3-METTL14-WTAP复合物结合
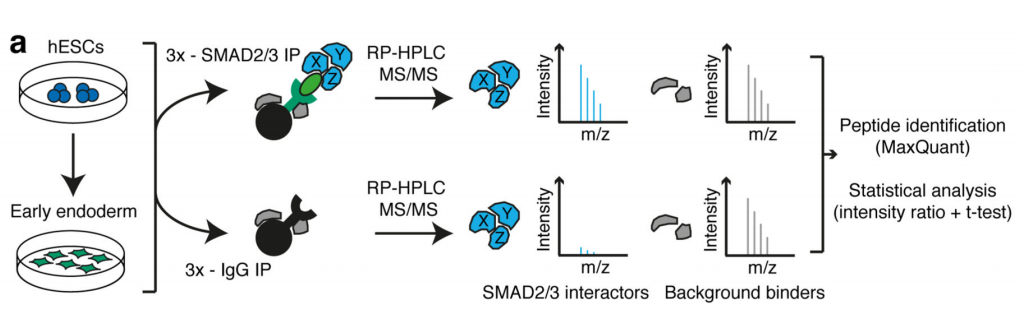
作者首先通过体外刺激,诱导人类胚胎干细胞分化为神经外胚层细胞,并通过Co-IP技术联合质谱(云序生物提供此项实验)技术,对比两种细胞中,能够与SMAD2/3抗体直接结合的蛋白。结果显示,一共找到89个蛋白,取交集后,得到78个共有蛋白,绘制成网络图,发现这些蛋白除参与TGF-β信号通路,mRNA生物学过程之外,还与国自然大热点RNA甲基化中的甲基化转移酶-------METTL3-METTL14-WTAP复合物直接互作。此结果与后期WB验证和抑制SMAD2/3磷酸化位点后Co-IP结果吻合。PLA实验证实两者间的结合主要发生在细胞核内,并且受Activin刺激后,影响核内转录因子NANOG表达。
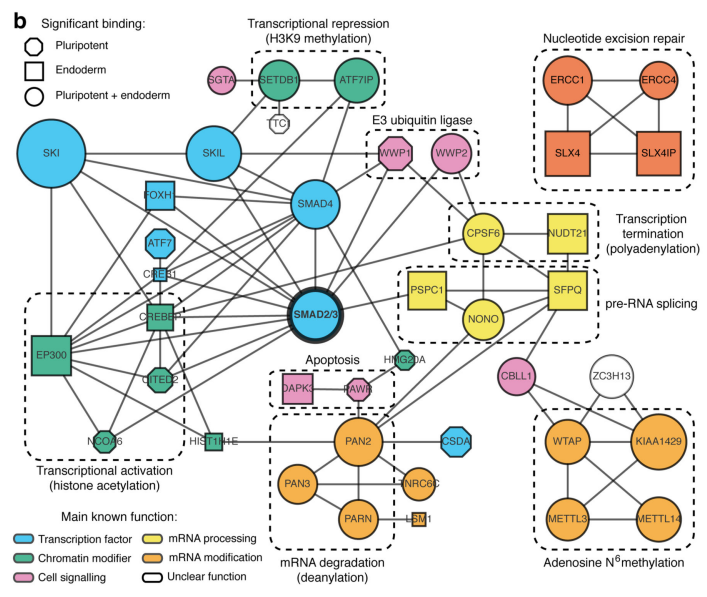
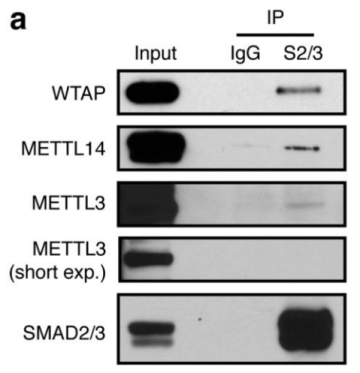
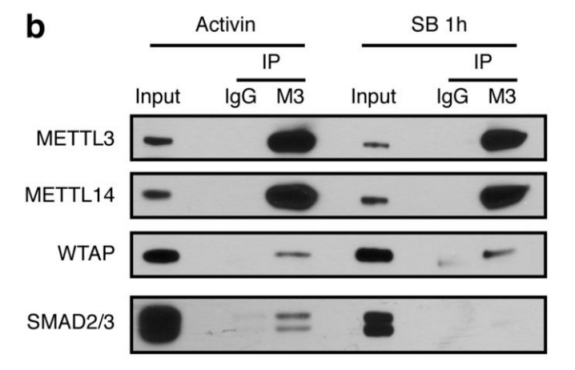
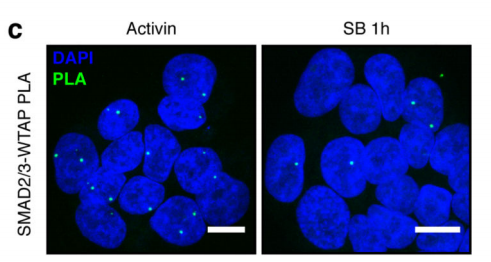
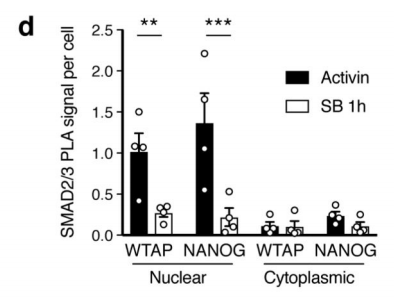
2.Activin/Nodal影响SMAD2/3下游转录因子甲基化
作者以Activin/Nodal敲降组胚胎干细胞为实验组,未敲降组为对照,每组三个生物学重复,进行m6A RNA甲基化测序(云序生物提供此项实验)。结果显示,motif区域保守序列为GGAC,且大多在转录起始区和转录终止区富集,Activin/Nodal特有甲基化位点在转录起始区低富集。可视化结果显示,NANOG和LEFTY1的mRNA分子上存在m6A甲基化信号(如红框所示),并且通过SMAD2/3的ChIP测序(云序生物提供此项实验)结果,有一部分区域与甲基化信号重叠(如绿框所示)。WTAP或SMAD2/3蛋白RIP实验(云序生物提供此项实验)证实,在受Actin分子刺激下,WTAP与NANOG,LEFT,FZD8和NOC2L结合增强,而在SMAD2/3分子刺激下,能够促进其降解。
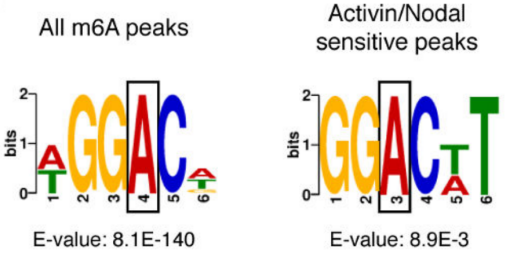
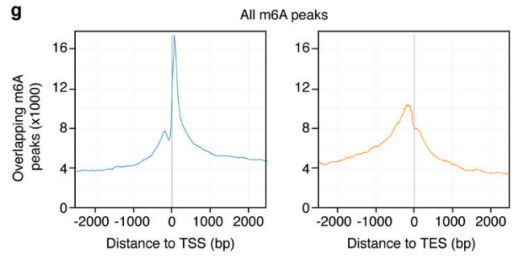
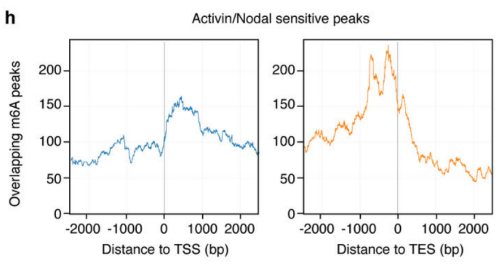
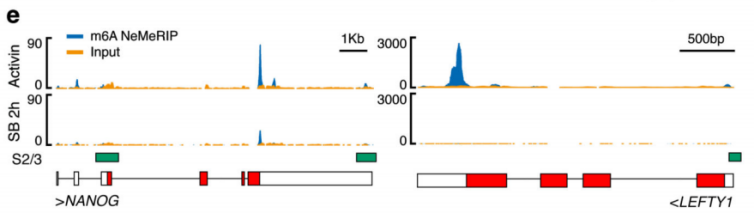
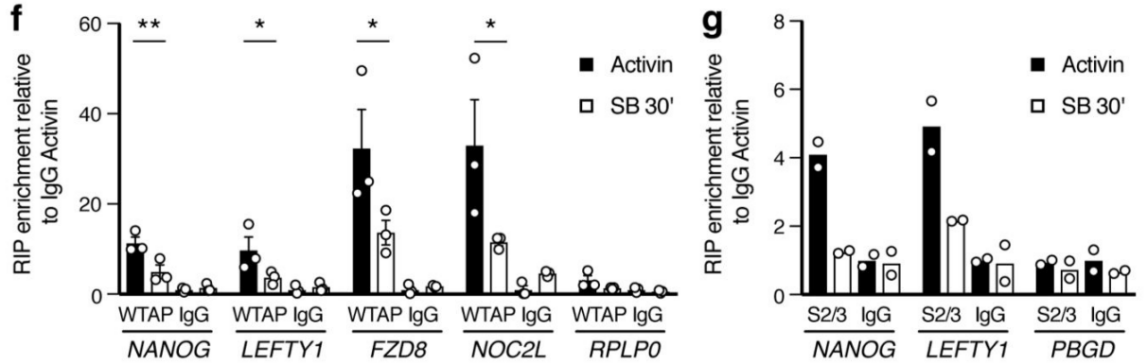
3.Activin/Nodal促进SMAD2/3结合蛋白与下游转录因子结合
前人研究证实m6A多在细胞核内促进pre-RNA的合成,由于本实验的SMAD2/3通过与m6A 甲基化酶复合物结合,影响靶基因合成的位置同样也在核内,并且SMAD2/3的转录和甲基化受Activin/Nodal调控,因此,作者猜测SMAD2/3可能参与pre-mRNA的合成。通过抑制Activin/Nodal后检测m6A RNA甲基化水平,发现差异甲基化的情况不单单在外显子上下调,同时在外显子和内含子交界处受抑制。综上,Actin通过促进磷酸化的SMAD2/3蛋白与下游转录因子结合,调控靶基因发生m6A RNA甲基化。
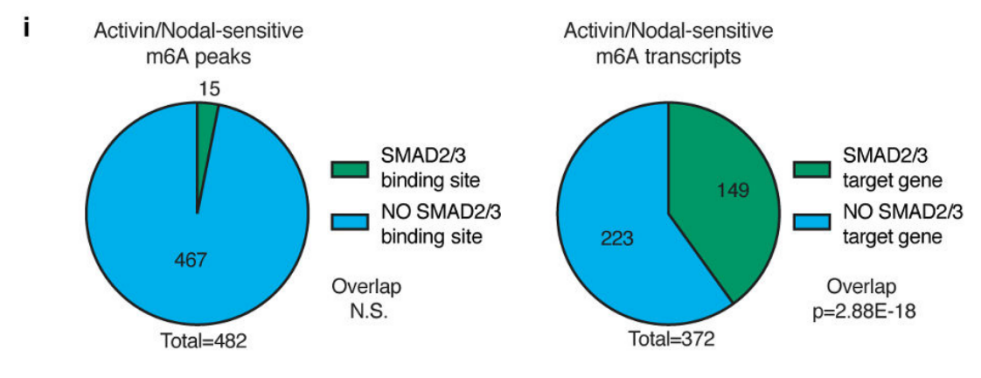
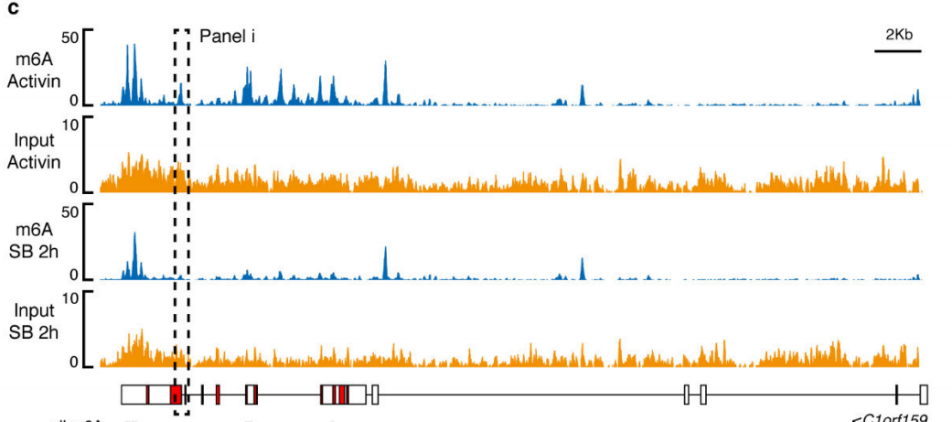
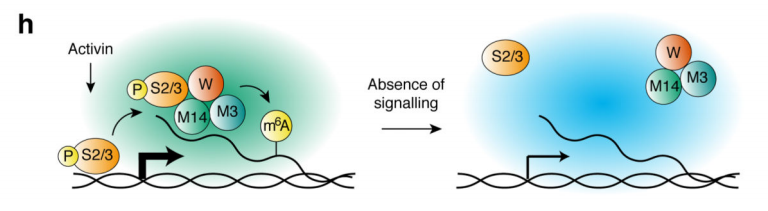
4.转录因子mRNA甲基化负调控干细胞增殖
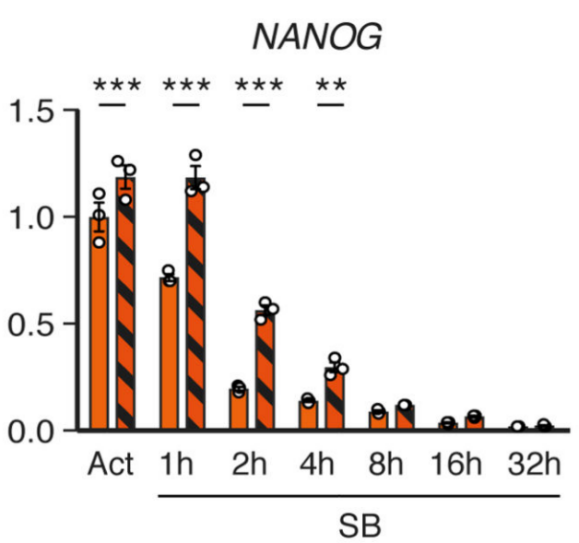
通常来说,RNA甲基化与基因的表达关系密切。作者接下来分析了甲基化与转录水平的两组学联合分析,发现下调Activin/Nodal通路后,NNANOG上的m6A甲基化水平与表达量成反比,并对神经内胚层分化起促进作用。
总结
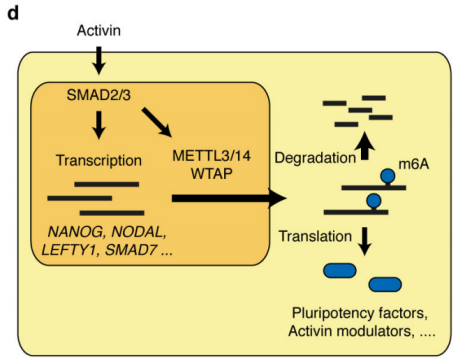
本篇文章首次研究了SMAD2/3蛋白与TGF-β通路间复杂的细胞内生物学过程。本文结果展示了SMAD2/3在mRNA上发挥了调控,凋亡,DNA修复和转录后调控的生物学功能,并阐述了此过程受Activin/Nodal的m6A甲基化调控,并与甲基化转移酶间的关联。本文为以后研究RNA甲基化非经典机制,如与染色质表观遗传、转录和表位调控奠定基础。
全文链接
https://www.nature.com/articles/nature25784
参考文献
1.Yang D, Qiao J, Wang G, et al. N6-Methyladenosine modification of
lincRNA 1281 is critically required for mESC differentiation
potential[J]. Nucleic Acids Research, 2018, 46. 影响因子:11.561
2.Wen J, Lv R, Ma H, et al. Zc3h13 Regulates Nuclear RNA m6A Methylation
and Mouse Embryonic Stem Cell Self-Renewal.[J]. Molecular Cell, 2018,
69(6):1028. ?影响因子: 14.248
3.Li H B, Tong J, Zhu S, et al. m6A mRNA methylation controls T cell
homeostasis by targeting the IL-7/STAT5/SOCS pathways[J]. Nature, 2017,
548(7667):338-342. 影响因子: 41.577?