CDD | 浙江大学郑敏/赵永超发现了肝癌的潜在治疗新靶点
TRAF2 (肿瘤坏死因子受体相关因子2)是一种具有双重功能的蛋白,作为衔接蛋白和泛素E3连接酶,在介导TNFα-NFκB信号通路中发挥重要作用。据报道,在多种人类癌症中,TRAF2表达失调。但是TRAF2是否以及如何调节肝癌细胞的生长仍然是一个谜。
2023年4月20日,浙江大学郑敏及赵永超团队在Cell Death & Differentiation(IF=12)在线发表了题为“The TRAF2-p62 axis promotes proliferation and survival of liver cancer by activating mTORC1 pathway”的研究论文,该研究的目的是检查肝癌中TRAF2的潜在失调及其生物学功能,并阐明其潜在机制,从而验证TRAF2是一个有吸引力的肝癌靶点。该研究发现TRAF2在人肝癌细胞系和组织中上调,并且TRAF2的高表达与HCC患者预后不良相关。蛋白质组学分析和共免疫沉淀分析表明p62是TRAF2的一个新的底物,它通过K420残基上的K63连锁受到TRAF2诱导的多泛素化。
该研究结果显示在人类HCC样本中发现p62蛋白水平与TRAF2呈显著负相关。TRAF2缺失通过引起p62积累抑制肝癌细胞体外和体内的生长和存活,而p62的同时敲低可以部分地挽救p62的积累。机制上,TRAF2介导的p62多泛素化通过形成p62-mTORC1 -rag复合物激活mTORC1,促进mTORC1溶酶体定位。TRAF2缺失通过破坏p62与mTORC1复合物之间的相互作用来抑制mTORC1活性。总之,该研究提供了概念验证证据,证明TRAF2是肝癌的有效靶点。

肝细胞癌(HCC)是全球第四大癌症死亡原因。导致HCC发生发展的确切机制尚不清楚。研究表明,几种重要的细胞信号通路,包括泛素-蛋白酶体系统、核因子κB (NF-κB)通路、自噬通路等都参与了HCC的发生发展。对这些信号通路中关键分子的研究可能有助于阐明肝脏肿瘤发生的机制,从而发现、验证并最终开发出有效治疗HCC的靶向治疗方法。
肿瘤坏死因子受体相关因子2 (TRAF2)是研究最多的TRAF家族成员之一,因其在NF-κB信号通路中的支架功能而闻名。因此,TRAF2在多种生物过程中发挥重要作用,包括细胞增殖、分化和凋亡。除了作为信号中枢,TRAF2也是一种泛素E3连接酶。TRAF2介导底物的K63和K48多泛素链,导致下游信号的激活。TRAF2在15%的上皮性肿瘤(包括HCC)中经常扩增和重排,并被确定为致癌基因。此外,TRAF2在血液恶性肿瘤中也起着特殊的作用。
尽管TRAF2参与多种肿瘤,但其在肝癌中的作用尚不明确。然而,最近的一项研究报道,肝实质细胞中受体相互作用丝氨酸/苏氨酸蛋白激酶1 (RIPK1)和TRAF2的联合基因缺失促进了HCC的发展,表明TRAF2具有积极作用。该研究试图鉴定与TRAF2相互作用的潜在蛋白,以阐明TRAF2调节肝癌细胞生长和存活的机制。这一努力导致了p62作为候选物质的发现。
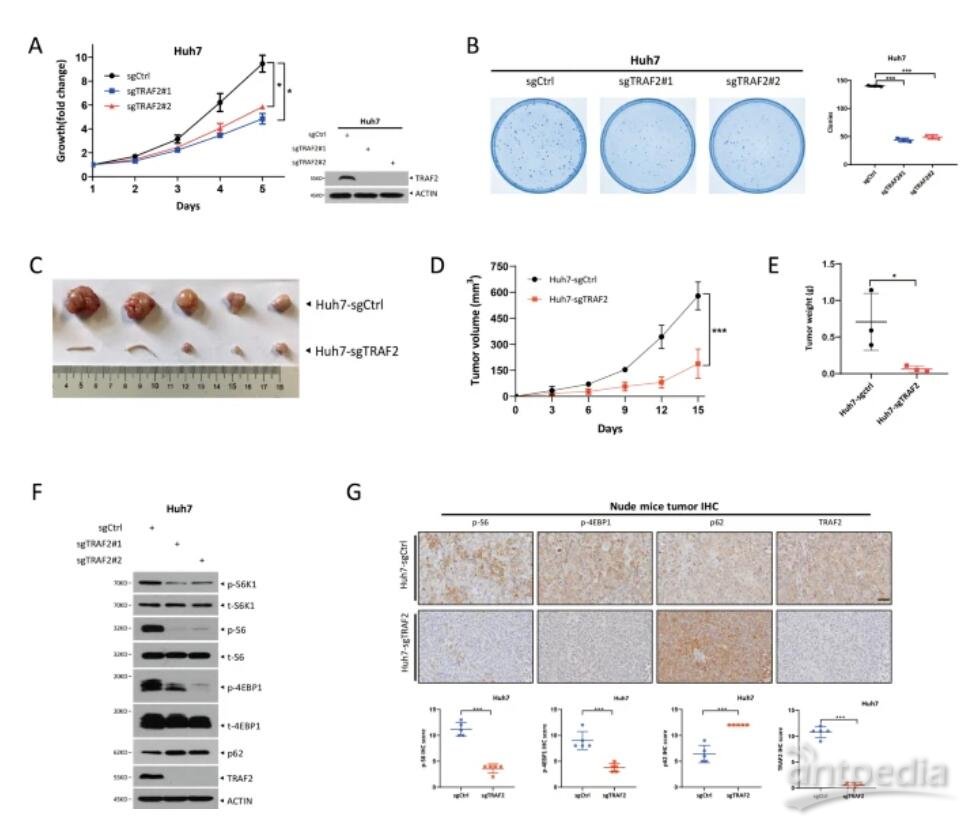
敲除TRAF2表达可移植HCC肿瘤生长(图源自Cell Death & Differentiation )
p62/SQSTM1 (sequestosome 1)通过与微管相关蛋白轻链3 (LC3)相互作用,是一个重要的自噬底物和适配体。除了在自噬通路中发挥作用外,p62也是一个参与细胞死亡、增殖和氧化应激反应的多功能信号调节因子。越来越多的证据表明,p62通过激活NF-κB信号,调节Keap1-NRF2和mTOR信号通路,以及自噬,在肝脏肿瘤发生中起着至关重要的促进作用。与其致癌作用相反,研究发现肝细胞中p62的缺失可增强二乙基亚硝胺(DEN)与高脂饮食(HFD)联合诱导的肝脏肿瘤发生。因此,p62似乎在HCC的发展中以一种环境依赖的方式发挥着复杂的作用。
该研究发现TRAF2在人HCC组织中蛋白和mRNA水平的表达均显著升高,这与HCC进展和患者生存不良呈正相关。TRAF2在体内和体外均能促进肝癌细胞的生长。该研究结果表明p62是TRAF2的一个新的底物,它通过K420残基上的K63连锁受到TRAF2诱导的多泛素化。泛素化后的p62通过增强mTORC1的溶酶体位置激活mTORC1信号。因此,该研究提出了一种靶向TRAF2/p62/mTOR轴治疗HCC的潜在策略。