默沙东Keytruda(可瑞达)获美国FDA批准2个新适应症
肿瘤免疫治疗巨头默沙东(Merck & Co)近日在美国监管方面迎来喜讯!美国FDA已批准Keytruda(可瑞达,通用名:pembrolizumab,帕博利珠单抗)2个新的适应症,一线治疗转移性或不可切除性复发性头颈部鳞状细胞癌(HNSCC)患者,具体为:(1)作为一种单药疗法,用于肿瘤表达PD-L1(合并阳性评分[CPS]≥1)的患者;(2)联合一种常用的化疗方案(铂+氟尿嘧啶[FU]),无论患者肿瘤PD-L1表达状态如何。
此次批准,使Keytruda成为首个获批一线治疗转移性或不可切除性复发性HNSCC患者的抗PD-1疗法,同时也是首个在这类患者中使总生存期(OS)在统计学上显著改善的抗PD-1疗法。
此次新适应症批准,基于关键性III期临床研究KEYNOTE-048(NCT02358031)的数据:与标准护理方案EXTREME相比,Keytruda作为单药疗法在CPS≥1的患者群体中显著延长了OS、Keytruda联合化疗在整个研究患者群体中显著延长了OS。
KEYNOTE-048也作为Ib期研究KEYNOTE-012的验证性研究,后者的总缓解率数据支持了2016年FDA加速批准Keytruda作为单药疗法治疗接受含铂护理期间或化疗后病情进展的复发性或转移性HNSCC患者。根据加速审批程序,进一步的完全批准取决于临床疗效的验证和描述,目前已在KEYNOTE-048研究中得到证实,并导致FDA将加速批准转为完全批准。
耶鲁医学院医学教授、耶鲁癌症中心开发治疗研究项目所长Barbara Burtness博士表示:“此次批准,对于头颈癌临床治疗是一个非常激动人心的里程碑,并有潜力通过提供重要的新治疗方案来改变临床医生治疗这种致衰性疾病患者的方式。转移性或复发性头颈癌一直是一个尚未得到满足的重要领域,因此在一线治疗中为患者提供免疫治疗方案非常令人鼓舞。”
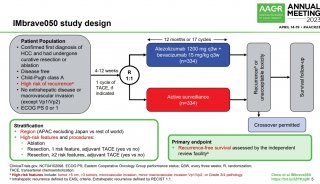
KEYNOTE-048是一项随机、开放标签研究,旨在评估Keytruda作为单药疗法或与铂(顺铂或卡铂)及5-氟尿嘧啶化疗联合疗法相对于目前HNSCC一线治疗标准护理方案EXTREME(Erbitux[cetuximab,西妥昔单抗]+铂[顺铂或卡铂]+5-氟尿嘧啶联合疗法)的疗效和安全性。该研究的共同主要终点是总生存期(OS)和无进展生存期(PFS)。次要终点包括:第6个月或第12个月的PFS生存率,客观缓解率(ORR),生命总体健康状态质量/欧洲癌症研究和治疗组织(EORTC)生活质量问卷生活量表质量发生恶化的时间。研究中825例被随机分配接受:(1)Keytruda单药疗法(200mg,3周一个疗程,每个疗程的第1天静脉输注,持续治疗24个月);(2)Keytruda+铂+5-氟尿嘧啶联合疗法;(3)EXTREME(Erbitux+铂+5-氟尿嘧啶组合疗法)。
截止数据分析时,Keytruda单药组、Keytruda+化疗组、EXTREME方案组中位随访时间分别为11.7个月、13.0个月、10.7个月。数据显示:
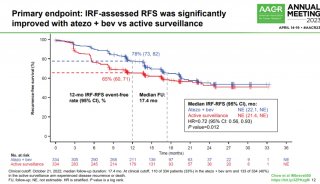
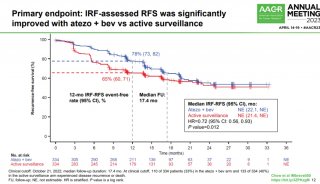
(1)在CPS≥20患者群体中:与EXTREME方案相比,Keytruda单药疗法显著延长了OS(14.9个月 vs 10.7个月;HR=0.61[95%CI:0.45-0.83],p=0.0015);PFS无差异(HR=0.99[95%CI:0.75-1.29]);Keytruda单药疗法和EXTREME方案的ORR分别为23.3%和36.1%、中位DOR分别为20.9个月和4.2个月。
(2)在CPS≥1患者群体中:与EXTREME方案相比,Keytruda单药疗法显著延长了OS(12.3个月 vs 10.3个月;HR=0.78[95%CI:0.64-0.96],p=0.0171);PFS无差异(HR=1.15[95%CI:0.96-1.38]);Keytruda单药疗法和EXTREME方案的ORR分别为19.1%和34.9%、中位DOR分别为20.9个月和4.5个月。
(3)在整个患者群体中:与EXTREME方案相比,Keytruda+化疗组合疗法显著延长了OS(13.0个月 vs 10.7个月;HR=0.77[95%CI:0.63-0.93],p=0.0067);PFS无差异(HR=0.92[95%CI:0.77-1.10]);Keytruda+化疗组合疗法和EXTREME方案的ORR分别为35.6%和36.3%、中位DOR分别为6.7个月和4.3个月。
该研究中,Keytruda的安全性与先前报道的涉及HNSCC患者的研究中一致。