指示抗癌药进程的纳米粒子
癌症是世界上最难治疗的疾病之一,科学家们一直都在孜孜不懈的寻找最佳的癌症治疗方法。2015年10月,Cell出版社旗下新子刊《Trends in Cancer》,邀请世界领先的癌症研究学者,列出了目前癌症研究领域所面临的八大问题。
目前,已有超过100种药物被批准用于治疗癌症,但如何因人施药以取得最佳疗效,仍是个难题。常规治疗手段下,治疗癌症的药物往往具有毒副作用,药物进入体内,大部分被肝脏、肾脏代谢,极少量药物进入肿瘤。2015年,美国总统奥巴马提出的“精准医学计划”,引发全球关注。精准医学的其中一个目标就是,了解不同的人为什么对同一种癌症疗法的反应不同,实现精准用药。
最近,来自美国俄亥俄州立大学的研究人员,基于自然发生的绿色荧光蛋白,设计了一种纳米粒子,可以穿过人体细胞,跟踪抗肿瘤药物的踪迹。这些纳米颗粒在可见光范围内具有光学活性、生物相容性和耐光性,在初步研究中,研究人员用MUC1核酸适体——阿霉素(DOX),对这些纳米粒子进行了功能化处理,可将化疗剂DOX带到癌细胞,表明他们能够实时监测药物在人类上皮癌细胞中的释放。他们这一研究成果发表在最近的《Nature Nanotechnology》。
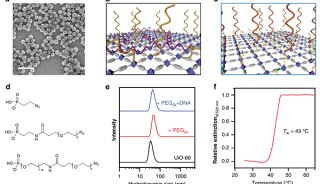
本文通讯作者是俄亥俄州立大学的华人学者Mingjun Zhang教授,他本硕博毕业于浙江大学,后在斯坦福大学获电气工程学硕士学位,2000年在华盛顿大学获科学博士学位,现就职于俄亥俄州立大学生物医学工程系。Zhang教授带领的研究小组,模仿黄色荧光蛋白制备了他们的二肽纳米粒子(DNP),黄色荧光蛋白的光活性是由于介子堆和BFPms1,一种突变的绿色荧光蛋白,其协同Zn(II)复合物,促进更大的荧光强度。他们调查了三种芳香肽——色氨酸、苯丙氨酸和酪氨酸的各种组合,发现Zn(II)可调节Trp-Phe复合物很容易地自组装成纳米颗粒,并在一个狭窄的可见光范围内具有光学活性。
Zhen等人用碱和碱金属离子调查了类似复合物的光学活性之后证实,过渡金属可形成最佳的配位结构。此外,他们调查了他们DNP的最好光信号的最佳浓度、温度和pH范围。荧光研究表明,DNPS会发出明亮的蓝色,并与Trp-Phe单体相比有一个较窄的光谱带宽。与用有机荧光染料(若丹明6G)的研究进行比较后证实,DNPs是耐光的,用NIH-3T3细胞的体外研究表明,与CdSe量子点相比,DNPs是生物相容性的。
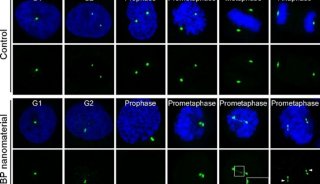
Zhen等人用MUC1核酸适配体——是靶定某些MUC1蛋白过表达的癌细胞的寡核苷酸,对DNPs进行了功能化处理。然后,他们将小鼠成纤维细胞(MUC1阴性)中MUC1核酸适配体功能化的DNP,与MUC1阳性的人类癌细胞进行了比较,以判断它对MUC1阳性细胞是否是选择性的。他们发现,人类细胞显示出明显的荧光,而小鼠细胞则没有。
最后,DOX——一种化疗药物,往往与芳香DNPS堆叠在一起。Dox与Trp-Phe DNP是共轭的,并且研究发现,当是共轭的时候,复合物就表现出荧光猝灭和吸收减少。人癌细胞的研究表明,随着DOX释放到靶细胞中,DNP的荧光信号增强,从而为抗癌药物的释放提供了一种实时的光学指示器。
精准医学的目标之一就是,了解不同的人为什么对同一种癌症疗法的反应不同。这项研究提供了一种方法,当一种众所周知的癌症药物在靶细胞内释放时,实时监测它的路径。研究人员希望,这将最终帮助医生对每名患者的治疗策略进行优化。
-
政策法规
-
企业风采

-
技术原理
-
会议会展

-
企业风采

-
焦点事件

-
焦点事件



































