自噬在肿瘤中的双面作用
这个夏天,复联 3 的上映是漫威迷的狂欢。说起复联系列,除却超级英雄的连番炫技,「亦正亦邪」的反派洛基也凭其独特的魅力吸粉无数。
细胞内的「清道夫」自噬,在肿瘤领域中也扮演着这样的双面角色。一方面通过控制肿瘤细胞增殖,抑制血管生成来实现抑癌作用,另一方面自噬可提高肿瘤细胞的应激能力助其死里逃生。在大多数情况下,自噬被认为是抑制早期肿瘤发生,促进已形成的肿瘤发展。
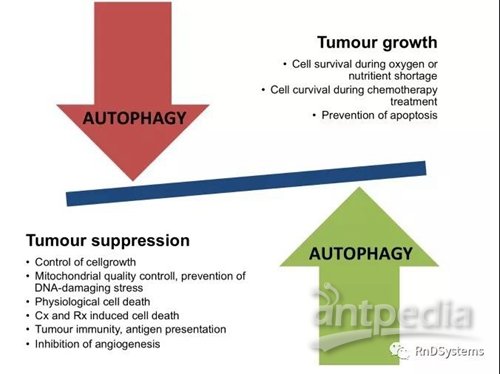
自噬在肿瘤中的双面作用
过往对肿瘤的研究和治疗,简单粗暴的针对于肿瘤细胞本身,而越来越多的研究聚焦在肿瘤及其微环境,自噬也不例外。在肿瘤的发展过程中,自噬、肿瘤、微环境有着怎样的恩仇录呢?
种子与土壤
早在 1889 年,英国医生 Stephen Paget 就提出了「种子与土壤」学说,「种子」是指肿瘤细胞,「土壤」是适合肿瘤细胞生长的微环境。肿瘤的生长与转移与微环境息息相关,橘生淮南为橘,生淮北为枳,一些特定的靶器官能够提供适宜肿瘤细胞生长的,从而备受「青睐」,而在另一部分器官中却不会形成肿瘤。

「种子与土壤」学说提出者 Stephen Paget,图片来自于 Bing
「土壤」具体有哪些元素呢?肿瘤微环境包括肿瘤细胞周围的血管,成纤维细胞、内皮细胞、免疫细胞、骨髓来源的间充质干细胞等各种正常细胞,以及细胞外基质(ECM)等。肿瘤细胞可以通过释放细胞外信号影响周边的微环境,促进肿瘤血管增生和抑制周边的免疫细胞,而肿瘤微环境中的免疫细胞及因子又可以影响肿瘤细胞的生长。
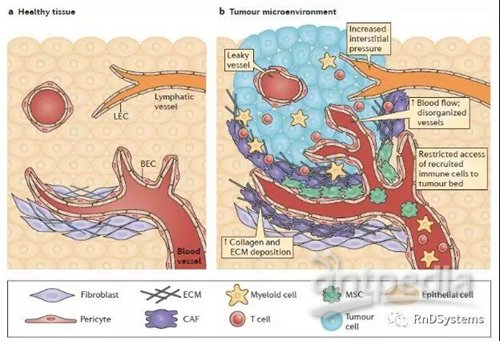
肿瘤细胞与肿瘤微环境间的相互关系(右图)远比正常组织中细胞和其周边的微环境复杂的多(左图)
肿瘤细胞中的自噬——调控微环境
肿瘤细胞中的自噬通过调控细胞因子、生长因子来影响细胞间的交流,包括临近的肿瘤细胞和其它肿瘤微环境中的正常细胞。研究表明,自噬可以阻碍肿瘤微环境的抗肿瘤免疫,肿瘤细胞从而实现「免疫逃避」。采用遗传手段抑制自噬,不仅可以抑制荷瘤小鼠内的肿瘤生长,而且可增强免疫监视,加强 CD8+ T 细胞介导的细胞毒性作用,最终杀伤肿瘤。
例如,在 ATG4B 显性负性的胰腺导管腺癌(PDAC)小鼠模型中,自噬受到限制,观察到肿瘤生长的显著抑制。当在裸鼠中注射自噬功能正常的细胞后,肿瘤「卷土重来」,而 ATG4BCA+(自噬缺陷)细胞则未出现这一现象。最近一项 PDAC 的研究表明,抑制自噬,能够引起抗肿瘤 T 细胞和 CD68+ 巨噬细胞的募集及渗透。
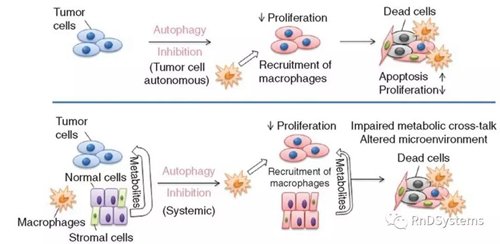
抑制自噬可影响 PDAC 的生长
微环境中的自噬——调控肿瘤细胞
肿瘤微环境中的自噬对肿瘤细胞也具有深远的影响,胰腺癌的一项研究表明,抑制微环境中的胰腺星形细胞自噬,减少了肿瘤细胞丙氨酸的摄入,进而限制其代谢及生长。
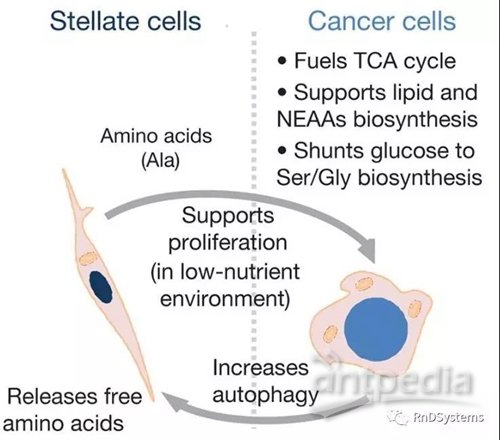
肿瘤-基质代谢相互作用模型
Nature 的一项研究使用一种带有恶性肿瘤的果蝇模型,其肿瘤可以被自噬抑制剂类药物控制,前期肿瘤生长和自噬主要依赖于其所处的肿瘤微环境。当把处于休眠状态的自噬缺陷肿瘤细胞移植到自噬活跃的机体中时,就会重新激活肿瘤的生长活力。
总之,肿瘤细胞及其微环境中的自噬可作为肿瘤研究的靶标,因此,自噬抑制剂(查看Tocris 自噬抑制剂)具有成为抗肿瘤药物的潜能。
检测自噬的正确打开方式
传统方法利用电子显微镜对自噬过程进行研究,理想情况下,应该使用组合测量方法,包括自噬形成的稳态监测和自噬流测定等不同体系来评估自噬活动。
• 稳态监测:自噬小体数量
自噬小体的数量分析试验通常测定的是 LC3 蛋白。LC3 可能存在于胞质和胞核中。脂化型 LC3 或 LC3 -II 是已知的唯一与自噬小体的内膜相关的蛋白。通过免疫荧光(ICC/IHC/IF)和免疫印记(WB)可以检测 LC3-II 水平,通过它可以较好的评估自噬小体的数量。
• 自噬流测定
自噬流是指从自噬小体的形成到底物降解,再将基本组分回收到胞质的整个过程。免疫荧光或免疫印迹分析中增强的 LC3-II 信号可能由自噬引起,也可能是自噬流阻断所致。因此,为了清楚地区分这两种机制,经常需要设置正确的对照,添加自噬诱导剂和溶酶体抑制剂,将自噬流测定与稳态监测相结合。
Bio-Techne 凭借超强的实力,俨然成为自噬研究领域的领导者。旗下子品牌 Novus 的 LC3B 抗体(目录编号# NB100-2220)被 CiteAb 认可,确定为自噬市场上引用最多的抗体,目前引用数已近 700 篇!
参考文献:
[1] Aunan JR, et al. The Biology of Aging and Cancer: A Brief Overview of Shared and Divergent Molecular Hallmarks. Aging Dis. 2017 Oct 1;8(5):628-642.
[2] Narita M, et al. Spatial coupling of mTOR and autophagy augments secretory phenotypes. Science. 2011;332(6032):966-70.
[3] Noman MZ, et al. Blocking hypoxia-induced autophagy in tumors restores cytotoxic T-cell activity and promotes regression. Cancer Res. 2011;71(18):5976-86.
[4] Garg AD, et al. ROS-induced autophagy in cancer cells assists in evasion from determinants of immunogenic cell death. Autophagy. 2013;9(9):1292-307.
[5] Maes H, et al. Autophagy: shaping the tumor microenvironment and therapeutic response. Trends Mol Med. 2013;19(7):428-46.
[6] Yang A, et al. Autophagy sustains pancreatic cancer growth through both cell autonomous and non-autonomous mechanisms. Cancer Discov. 2018.
[7] Sousa CM, et al. Pancreatic stellate cells support tumour metabolism through autophagic alanine secretion. Nature. 2016;536(7617):479-83.
[8] Katheder NS, et al. Microenvironmental autophagy promotes tumour growth. Nature. 2017;541(7637):417-20.




















