ACE HILIC色谱柱方法开发指南Ⅲ - HILIC法色谱条件
HILIC流动相
HILIC模式中用作流动相的溶剂类似于RPLC模式下所用的溶剂。
流动相条件是各种HILIC保留机制的关键因素。
通过改变洗脱液中有机组分和水组分的比例,可以改变分析的保留率。
在HILIC模式下,保留因子建议保持在1.5-10之间。
有机改性剂
HILIC中最常用的有机改性剂是非质子溶剂乙腈。
乙腈作为较弱的洗脱溶剂与水结合使用(见图5)。
与RPLC不同,增加流动相中的有机物含量百分比,可增大分析物的保留率。
乙腈具有粘度(粘度低)和紫外线切断(截止波长)较低等优点。

由于能够干扰固定相周围的水层,所以散装(主体)溶剂中通常要避免甲醇等质子溶剂。
这些溶剂可以形成氢键,从而破坏分析物分散(分配能力)。
但是,也存在极性溶剂(如甲醇和2-异丙醇(IPA))与水性部分结合使用以影响分离选择性的各种情况。
如果所有其它参数不能实现足够的分离[6],这通常作为最后的方法来使用。
洗脱剂pH值
洗脱剂的pH值对于方法开发来说是一个有用的参数。
如果pH值高于或低于可电离物质的pKa,则分析物的电离状态会发生改变,反过来会影响它的亲水性。
因此,这会影响(影响可电离分析物)与固定相的潜在相互作用,并且还会影响保留。
此外,pH值也会影响固定相表面的极性,进而影响到保留机制。
了解分析物的pKa非常有助于pH选择。若可能的话,建议与pKa相差2个pH单位,以达到特定的方法稳定性。对于酸性物质,低于pKa将使分析物主要以非电离状态存在。
在酸性分析物pKa的2个pH单位以上将使大部分分析物电离。对于碱性物质,正好相反。
为了进行方法开发,建议对(在)三种不同pH值条件下各种(用三款)ACE HILIC色谱柱的(对)混合分析物进行评估:
pH 3.0、4.7和6.0。这种方法探索了不同洗脱剂pH值条件下使用不同固定相时的选择性差异,而且经证明对HILIC方法开发是有效的。
例如,ACE HILIC-A相中,在pH为3.0、4.7和6.0的等度条件下,分析了包含酸性物质和中性物质的混合物(见图6)。所有其它条件都相同。
保留和洗脱顺序的差异(即选择性差异)可清楚地看出,这一单个HILIC相的pH值不同。

图6
ACE HILIC-A相中,不同流动相pH值下六种极性分析物的分析中性物-绿色酸-红色
色谱柱:150 x 4.6 mm, 5 μm
流动相:10 mM甲酸铵(溶于MeCN/H2O中)(90:10 v/v)
流速:1.5 mL/min
检测:UV, 254 nm
温度:25 °C
进样:5 μL
样本:
1) 4-氨基苯甲酸
2) 4-羟基苯甲酸
3) 烟酰胺
4) 扁桃酸
5) 腺嘌呤
6) 2’-脱氧鸟苷
缓冲液浓度
HILIC中可使用各种缓冲盐,但缓冲盐必须可溶解于高有机物含量的(含有高比例有机物的)洗脱剂中。
这就排除了像磷酸盐这样的无机缓冲盐。
甲酸铵缓冲盐比较适宜,因为它们在低pH范围内具有缓冲能力,并在高乙腈含量的洗脱剂中具有良好的溶解性。
HILIC的缓冲液浓度范围通常为2-18mM。
缓冲液浓度对保留率和选择性的影响取决于分析物和固定相的特性。
例如,图7显示了pH为3.0时,通过ACE HILIC-A固定相,甲酸铵缓冲液的浓度对三(三种)组分(极性的酸性、碱性和中性分析物)混合物分析物保留率(保留)的影响。
洗脱剂浓度低(洗脱剂的低pH)意味着:酸吡哆醛(峰1)以离子抑制或中性的形式存在。胞啶(峰2)是一种极性的中性分析物。
普鲁卡因胺(峰3)是一种带电的极性碱。在ACE HILIC-A相的这些条件下,极性碱的保留率显著下降,而(随着)缓冲液浓度增大(随着缓冲液浓度增大,极性碱的保留率显著下降)。
极性碱很可能主要是通过与带电酸性固定相进行离子交换的方式来保留。
缓冲强度的增加会使(与)碱性分析物形成竞争,并且保留率随后会因离子交换机制的耗尽而减小。

图7
缓冲液强度对分析物保留率的影响
色谱柱:ACE 5 HILIC-A,150 x 4.6 mm
流动相:甲酸铵,pH3.0(溶于MeCN/H2O中)(90:10 v/v)
流速:1.5 mL/min
检测:UV, 254 nm
温度:25 °C
进样:5 μL
样本:
1) 吡哆醛
2) 胞啶
3) 普鲁卡因胺
样品稀释液
HILIC模式下,由于分析物溶解性以及稀释液与HILIC洗脱剂不匹配等问题,通常较难选择合适的样本(样品)稀释液。
选择优化不足的稀释液会大大降低色谱性能和峰形。
通常,样本稀释液对各种分析物的影响不一样,并且这种行为因固定相的选择和洗脱剂的条件而存在差异。
因此,对样本稀释液的优化往往是针对特定应用的研究。
一般来说,建议增量为20%,缓冲比介于20%到80%之间(建议20%的乙腈增量让其处于缓冲比20%-80%之间来探索样品稀释方法)。
例如,图8(第16页)显示了pH为3.0时,三个ACE HILIC相中的每一个相(固定相)上酸性、碱性和中性分析物的峰形,其中研究了样本(在这三个固定相上的研究样品)稀释液乙腈(MeCN)的百分比。
通常,次黄嘌呤(极性中性)的峰形会随着所有ACE HILIC相有机浓度的增大而改善。
然而,分析物未能在100%的乙腈中溶解。
这种分析物最有效的样本(样品)稀释液是60-80%的乙腈。
在样本稀释液中乙腈浓度较低的情况下,酪胺(碱性分析物)显示了ACE HILIC-B相和ACE HILIC-N相的分裂峰。
然而,这种效果对ACE HILIC-A并没有那么明显,峰形仍然很差。
对于60%以上的乙腈,所有ACE HILIC相的峰形都有改善。
扁桃酸的峰形通常不受ACE HILIC-B和ACE HILIC-N的样本(品)稀释液的影响。但是,对于ACE HILIC-A,有机浓度较低时峰形较差。
根据这个数据集,对于该HILIC应用,建议使用60-80%的乙腈样本(样品)稀释液。
对于各HILIC应用,建议进行此类系统研究。
如果可能的话,最好采用较高浓度的分析物和较小的进样量。
这样可尽量减少(尽可能减少)对吸附水层的破坏。
样本(样品)溶解性与样本(样品)浓度之间的平衡(权衡)始终具有挑战,尤其是对于HILIC而言。
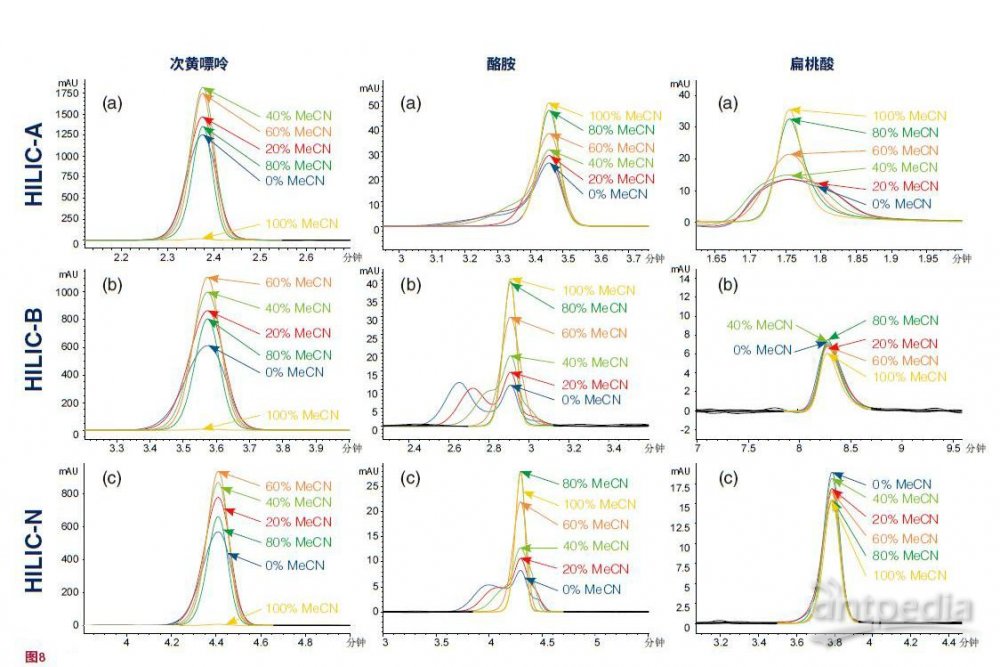
图8
(a)ACE HILIC-A相(b)ACE HILIC-B相和(c)ACE HILIC-N相中样本溶液对次黄嘌呤、酪胺和扁桃酸的色谱峰形的影响。
色谱柱:150 x 4.6 mm, 5μm
流动相:甲酸铵,pH4.7,(溶于MeCN/H2O中)(90:10 v/v)
流速:1.5mL/min
温度:25 °C
检测:UV, 254 nm
进样:5 μL
温度
温度是方法开发中一个很有用的参数。
温度对保留的影响程度取决于固定相和分析物二者。例如,分析物的pKa可能随着温度的变化而变化,从而影响电离和保留的程度。
据记载,对于HILIC,随着温度的升高,保留率有可能同时增加和减少,如图9中所示,分离出极性的酸性、碱性和中性分析物(极性的酸性、碱性和中性分析物的分离)。
在HILIC方法开发中,建议不要将温度作为优化选择性和分离的主要参数。
与色谱柱化学特性、有机物含量百分比或洗脱剂pH值等参数相比,在HILIC模式下它能改变保留率(保留的作用微弱)。

图9
下列相中温度对酸性、碱性和中性分析物混合物的分析物保留率的影响:
(a) ACE 5 HILIC-A
(b) ACE 5 HILIC-N
(c) ACE 5 HILIC-B
色谱柱:150 x 4.6 mm
流动相:10 mM甲酸铵,pH4.7(溶于MeCN/H2O中)(90:10 v/v)
流速:1.5 mL/min
检测:UV, 230 nm
进样:5 μL
样本:
1) 4-羟基苯甲酸
2) 沙丁胺醇
3) 2’-脱氧鸟苷
4) 色氨酸