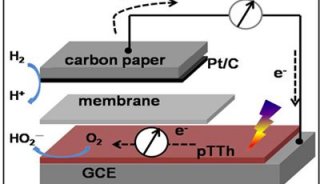
解析:过渡金属氧化物的表面氧还原活性
背景
氧还原反应(ORR)是燃料电池性能的关键瓶颈之一。到目前为止,该反应的最活跃、最稳定的电催化剂是铂族金属元素。而过渡金属氧化物(TMO)是一类在氧化条件下实现运行稳定性的替代材料。不幸的是,人们通常发现TMO的活性远不如Pt。
研究的问题
本文确定了为什么很难找到具有高ORR活性的TMO的两个原因。首先,TMO表面始终比过渡金属更弱地结合氧原子。这使得O-O键的断裂决定了本文研究的各种TMO表面的速率。二是TMO表面的电场效应较强,进一步增加了O-O键断裂的难度。为了验证预测并确定它们对TMO的普适性,本文报道了对7798种独特的TMO组分的实验ORR催化剂筛选,这些TMO组分的活性通常远低于Pt。
图文分析
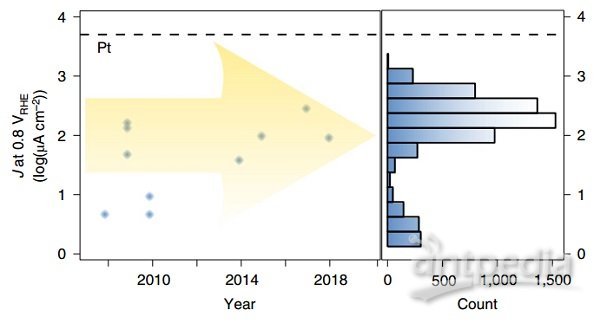
图1|TMO催化剂性能摘要。
要点:
在图1的酸性ORR面板中,展示了过去12年发表的用于酸性ORR的代表性稳定TMO催化剂的性能摘要。
在催化剂运行两小时(以减轻瞬变反应产生的电流)后,测量了基于Mn、Ni和Fe与Ca、Mg、Y、In和La的不同组合的7798种独特的TMO组成的ORR活性,以在图1的碱性ORR面板中展现结果。
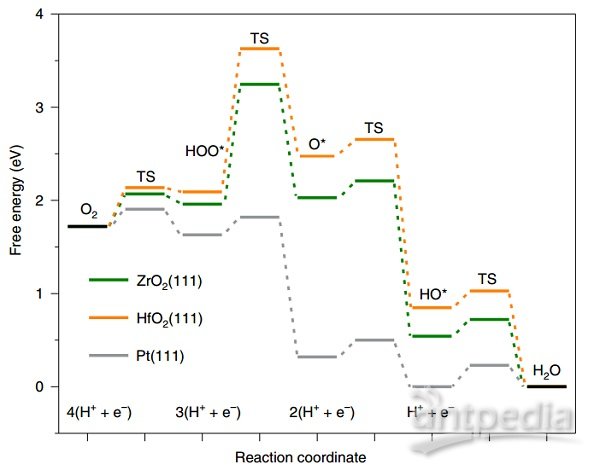
图2|Pt,ZrO2和HfO2(111)上的四电子(4e-)(four-electron)的ORR过程的自由能图。
要点:
在图2中,本文将两个稳定的TMO的计算自由能图与典型的ORR催化剂Pt的自由能图进行了比较(使用Kulkarni等人的数据)。基本步骤的能量势垒估计是基于狄更斯等人的比例关系。表面Pourbaix图计算表明,在酸和碱中,化学计量比的原始TMO表面在ORR电位下是最有利的。
如图2所示,由于O*与HO*和HOO*的结合方式不同,EO*与EHO*在金属上的比例关系因吸附位置而异。在紧密堆积的过渡金属上,O吸附在三重中心,而HO和HOO则偏爱两重或一重中心。如果不是绘制EO*与EHO*的标度与O在首选位置的关系,而是强制O吸附在顶部位置,则可以观察到HO相对O标度线的显著上移(图2)。
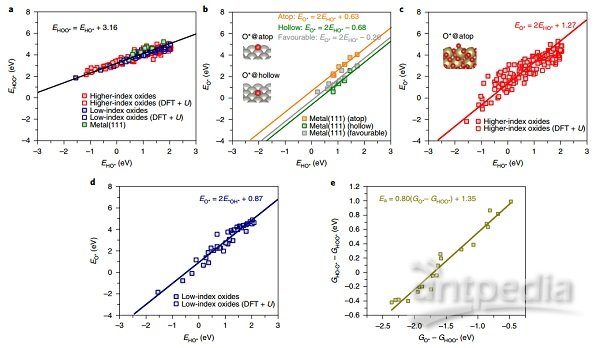
图3|决定ORR活动的线性缩放关系。
要点:
TMOS与Pt的显著区别在于吸附O*的稳定性和O-O键断裂的过渡态。无论反应的pH值如何,两者在TMOS上的稳定性都要差得多。这是一个普遍的现象,如图3所示。本文对ORR中间体在200多个不同的TMO和低指数和高指数表面上的吸附能进行了密度泛函(DFT)计算。在图3中,本文收集了HOO*对HO*和O*对HO*的吸附能之间的标度关系的数据。第一种是通用的-TMO的情况与过渡金属的情况相同(图3a)。然而,后者对于TMO和金属来说是非常不同的(图3b-d)。这是本研究的两个重要理论发现之一。本文注意到,这个结果与是否在计算中包含Hubbard U无关。
总而言之,电场效应可以提供第二个原因的解释,即为什么TMOS在酸性条件下对4e-ORR的性能本质上是有限的。显然,目前的模型,至少在定性上,也解释了为什么TMOS在碱性溶液中似乎比在酸性溶液中更好。本文的模型表明,由于HO与HOO的比例关系不变(图3a),TMO在酸和碱中对2e-ORR的活性都更高,这与许多实验观察结果是一致的。
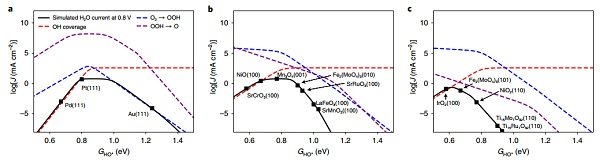
图4:0.8VRHE的4e -ORR过程的动力学火山模型。
要点:
氧的弱成键(大的GO*-GHO*或者HO对HOO比例)导致O-O键断裂形成更大势垒。所有这些都在图4所示的ORR动力学模型中得到证实。
对于过渡金属来说,通常有两个重要的步骤来决定O2的吸附速率和Ho*从表面的去除。这产生了一种火山形状的曲线(图4a)。
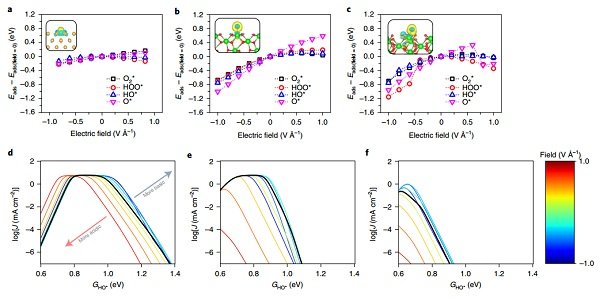
图5|电场效应和pH相关的火山动力学模型
要点:
在酸性溶液中,过渡金属对活火山的影响很小(图5a)。相比之下,火山向左和向下移动,在更酸性的条件下,低指数和高指数TMO的最大速率普遍下降(图5b,c)。这种影响在TMO上比在金属上强,这是因为TMO表面通常有较大的表面偶极和极化率,这是因为在TMO表面,O和其他吸附物在大多数情况下只能吸附在顶部位置,而它们可以在过渡面上找到更稳定的高配位吸附位置。
结语
在这项工作中,基于密度泛函理论(DFT)计算和微观动力学模拟,确定了为什么很难找到具有高ORR催化活性的TMO的两个原因。首先,TMO表面与氧原子的结合比过渡金属更弱。这使得O-O键的断裂率在许多情况下是决定性的,并限制了相对于金属的催化活性。第二个原因是TMO表面的电场效应更强,这进一步增加了O-O键的断裂难度,特别是在酸性条件下。这两种效应协同作用共同影响TMO表面ORR的活性。
本文由SSC供稿。