PCR产物的直接纯化
实验概要
本实验介绍了PCR产物直接纯化的原理及操作步骤。
实验原理
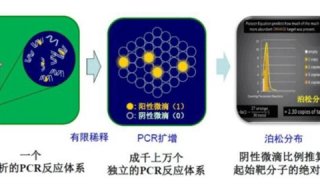
PCR产物一般都含有过量的引物、Taq DNA酶及dNTP,这些成分的存在将直接影响到后续的酶切、双脱氧PCR测序反应等过程,因此有必要除去。目前核酸纯化的方法有很多,商用化试剂盒的出现使得DNA的纯化过程变得更加简便快捷。本实验中,Buffer PCR-A促使大于100bp的DNA片断选择性地吸附到silica膜上。经Buffer W1、Buffer W2洗涤去除残留在silica膜上的小于50-mer的引物、酶蛋白、单核苷酸、荧光染料或放射性同位素标记的单核苷酸后,吸附到silica膜上的 DNA片断经微量水或Eluent洗脱下来,即可用于各种分子生物学的操作。
主要试剂
1. Buffer PCR-A
2. Buffer W1
3. 已加无水乙醇的Buffer W2
4. Eluent或去离子水
主要设备
1. 恒温孵育器(65℃)
2.离心机
3. 移液器
4. 1.5ml 离心管
实验材料
PCR产物
实验步骤
1. 在PCR反应液中加入3倍体积的Buffer PCR-A,若需加入的Buffer PCR-A不足100μl,则加入100μl。
2. 将DNA-prep Tube置于2-ml Microfuge Tube中,将步骤1中的混合液移入DNA-prep Tube中,5500rpm离心1min。
3. 弃滤液,将DNA-prep Tube置回到原2-ml Microfuge Tube中,加入500μl Buffer W1,5500rpm离心1min。
4. 弃滤液,将DNA-prep Tube置回到原2-ml Microfuge Tube 中,加入700μl 已加无水乙醇的Buffer W2,5500rpm离心1min,以同样的方法再用700μl已加无水乙醇的BufferW2洗涤一次。
5. 弃滤液,将DNA-prep Tube置回到原2-ml Microfuge Tube中,14000rpm离心1min。
6. 连滤液一并弃掉收集管,将DNA-prep Tube 置于一新的1.5ml 离心管中,在silica 膜中央加入25-30μl Eluent或去离子水(65℃预热)。
7. 室温静置2min,14000rpm离心1min洗脱DNA。
8. 取5μl样品,1%琼脂糖凝胶电泳检测纯化结果。
注意事项
洗脱液预热后可增大洗脱的DNA量,同时重复洗脱也可增加溶解的DNA量。