药监局加强用于药品的化学活性成分管理 正拟措施
3月16日下午,国家食品药品监督管理局局长邵明立、国家食品药品监督管理局副局长吴浈、国家食品药品监督管理局食品安全协调司司长孙咸泽、国家食品药品监督管理局新闻发言人颜江瑛,就“食品、药品安全”问题接受中外记者集体采访。
就化工企业生产原料药和药品生产企业使用化工企业生产的原料药直接生产药品的问题的监管措施问题,国家食品药品监督管理局副局长吴浈告诉记者,直接用于药品的化学活性成分,在国内是把它作为原料药管理。药品管理法明文规定,生产原料药必须具备生产条件,也就是获得生产许可,必须具备GMP的环境条件,获得认证证书,上市的产品必须符合国家标准,获得批准文号,这才能有资格生产原料药。
吴浈表示,有些化学活性成份,可能在原料药的前一步,还不能称之为原料药,因此这类化学活性成份可能在我们监管之外。这一问题已经引起我们的注意,包括国际社会也对此给予关注。
他指出,我们已经在采取措施加强这方面的管理。措施包括,首先要摸底,摸清楚到底有多少企业在生产这些东西。中国的化工厂较多,直接用于药品的活性成份、品种又很多,我们现已开始了与有关部门共同开展摸底调查。第二,国内明确要求,没有药品标准的其他化学活性成份,如果要用作药品生产,必须要有明确的购进单位,自己还得严格把关,制定相关标准。所以,国内药品生产企业必须按照这个要求来做,要能够溯源。第三,摸清底数之后,要采用登记制、备案制或者许可制,根据不同的情况采取措施。这些措施目前都在拟定之中,今后将向大家通报。
-
焦点事件

-
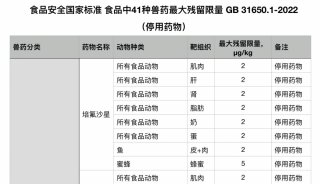
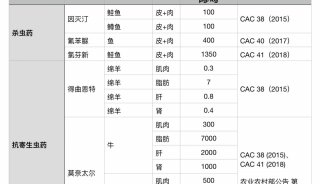
标准
-
焦点事件

-
焦点事件

-
精英视角