细胞溶质LPS感知及其调节和病理生理功能的最新研究进展
通过先天免疫系统监测细胞质室的病原体编码的产物或病原体的活动,往往可以激活caspase的一个子集。在大多数情况下,细胞内的监视通路通过典型的炎症复合体与caspase-1的激活结合。一组相关的caspase,即啮齿动物中的caspase-11和人类中的caspase-4和caspase-5,监测细胞溶质中的细菌脂多糖(LPS)。通过细胞内LPS直接激活caspase-11,caspase-4和caspase-5引发称为“pyroptosis”的溶解性细胞死亡,其发生在多种细胞类型中。通过成孔蛋白GSDMD执行pyroptosis,其由caspase-11,caspase-4或caspase-5介导的切割激活。在单核细胞中,GSDMD孔的形成可以诱导NLRP3炎性体的活化,从而使细胞因子IL-1β和IL-18成熟。响应细胞溶质LPS的Caspase-11介导的pyroptosis对抗菌防御和感染性休克至关重要。
2019年4月8号,北京生命科学研究做邵峰团队等人在Nature immunology上发表了Innate immunity to intracellular LPS的综述性文章。在这里,研究人员回顾了关于细胞溶质LPS感知及其调节和病理生理功能的最新研究进展。

由天然免疫细胞表达的生殖细胞编码的模式识别受体(PRRs)可以识别微生物相关分子模式(MAMPs)或内源性危险相关分子模式(DAMP)。PRRs所识别的MAMP,包括LPS、脂蛋白、碳水化合物、鞭毛素和核酸,在微生物中高度保守和/或常见,这使得宿主能够以有限数量的PRRs感知多种病原体。十多个类Toll受体被认为是细菌、病毒和寄生产物的PRRs。除了TLRs外,PRRs还包括CLRs、RLRs和ALRS,以及特征相对较差的NLRs。在这些PRRs中,TLRs和CLRs被结合在血浆或内小体膜上,而RLRs、ALRS和NLRs是胞浆性的,它们使天然免疫系统能够同时监测细胞外间隙和细胞内间隙,从而获得感染性药物。
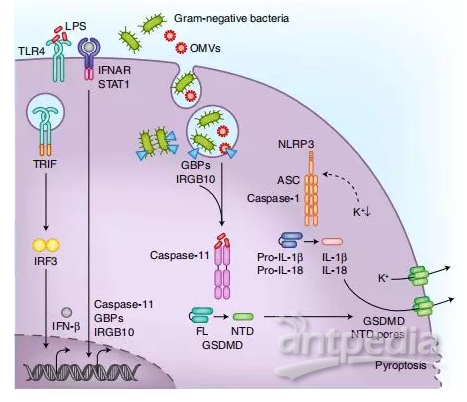
通过非典型炎症体感知细胞溶质LPS
PRRs识别MAMPS和DAMP的下游的一个关键事件是编码各种炎症介质的基因的转录激活。TLRs和CLRs,以及某些细胞质PRRs(如RLRs),刺激依赖转录因子NF-κB和干扰素调节因子(IRF)家族成员的基因转录。由ALR和NLR家族的许多细胞浆PRRs驱动的一种新的、同样重要的反应是促炎细胞死亡,称为“pyroptosis”。从形态学上看,“pyroptosis”的特征是细胞膜完整性丧失,细胞肿胀,质膜破裂,最终导致细胞溶解.“pyroptosis”具有高度的促炎作用,伴随着IL-1β和IL-18等炎性细胞因子的释放,同时还伴有IL-1α和HMGB 13等炎症反应。
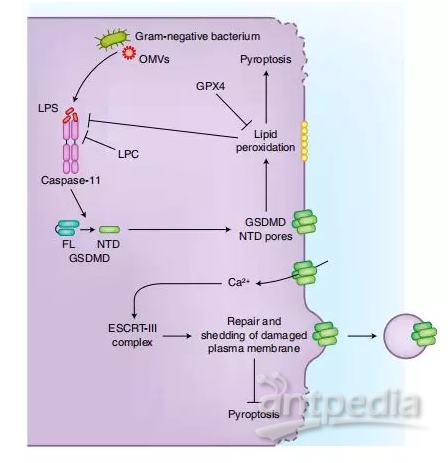
非典型炎症体的负调节
同时,“pyroptosis”是指由某些细菌感染或毒素刺激引起的caspase-1介导的单核细胞死亡。caspase-1的激活目前已知是由一种细胞质多蛋白炎症小体复合体介导的,其中NLR蛋白被认为是中心。在过去十多年的广泛工作中,确定了NLR家族的几个成员(包括NLRP 3、NAIPS和NLRP 1)、AIM 2和pyrin,它们在炎中起作用。这些细胞质PRRs识别多种微生物产物,包括细菌鞭毛素、III型分泌系统的成分和毒素,以及自身或外来双链DNA,以及在特定情况下,细菌毒力活动,以组装各种炎症小体,直接或间接通过适配体ASC或NLRC4激活caspase-1。caspase-1诱导的蛋白水解活性是由多重化介导的自蛋白水解过程产生的,它与IL-1β和IL-18的成熟和“pyroptosis”有关。