新冠口服药物!辉瑞Paxlovid获欧盟CHMP推荐批准!
与安慰剂相比,在症状出现后5天内启动Paxlovid治疗(每天2次,连续5天)可将住院或死亡风险降低88%。
辉瑞(Pfizer)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布一份积极审查意见,建议有条件批准Paxlovid(nirmatrelvir[PF-07321332]片剂和利托那韦片剂),用于治疗COVID-19,具体为:用于治疗不需要补氧、且有高风险发展为严重COVID-19的成人患者。现在,CHMP的意见将递交至欧盟委员会(EC)审查,后者通常会在2个月内做出最终审查决定。如果获得批准,Paxlovid将成为欧盟第一款COVID-19口服药物。
在美国,FDA于2021年12月授予Paxlovid紧急使用授权(EUA):用于治疗直接SARS-CoV-2病毒检测呈阳性、体重至少40公斤(88磅)、有高风险发展为严重COVID-19(包括住院或死亡)的轻度至中度COVID-19成人和儿科(≥12岁,体重≥40公斤[88磅])患者。
截至目前,Paxlovid已在全球10多个国家被批准或授权紧急使用。辉瑞计划在2022年向美国FDA提交Paxlovid的新药申请(NDA),以获得完全监管批准。
Paxlovid是一种复方制剂,由300mg(2片150mg)nirmatrelvir和一片100mg利托那韦组成,每天服药2次,连续服药5天。一盒药物含有5个泡罩包装的Paxlovid,作为nirmatrelvir片剂和利托那韦片剂的联合包装,提供完整5天疗效所需的全部剂量。
欧盟CHMP的积极审查意见以及美国EUA,均基于2/3期EPIC-HR研究的数据:与安慰剂相比,Paxlovid将住院或死亡风险降低89%(症状出现后3天内启动治疗)和88%(症状出现后5天内启动治疗)。
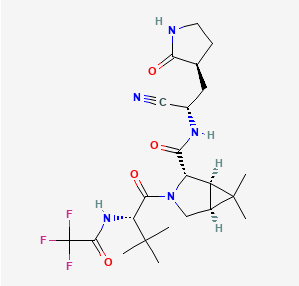
nirmatrelvir(PF-07321332)化学结构式(图片来源:drugapprovalsint.com)
Paxlovid活性药物成分中,nirmatrelvir是一种源于辉瑞实验室的新型主蛋白酶(Mpro,也被称为3CL蛋白酶)抑制剂,专门设计用于阻断SARS-CoV-2 Mpro的活性,这种酶是冠状病毒复制所需要的。低剂量利托那韦有助于减缓nirmatrelvir的代谢或分解,使其在较高浓度下在体内保持较长时间的活性,以帮助对抗病毒。
目前的变异毒株可以抵抗抑制SARS-COV-2病毒表面棘突蛋白的药物,因为该蛋白的突变率高。然而,Paxlovid通过结合SARS-CoV-2病毒的蛋白酶在细胞内发挥作用,从而抑制病毒复制。nirmatrelvir显示在体外针对当前变异毒株(即α、β、δ、γ、λ和μ)具有一致的抗病毒活性。此外,在体外生化分析中,nirmatrelvir可有效抑制与奥密克戎(Omicron)相关的Mpro。这表明nirmatrelvir有潜力针对奥密克戎维持强大的抗病毒活性。关于这种变体的其他体外抗病毒研究正在进行中。
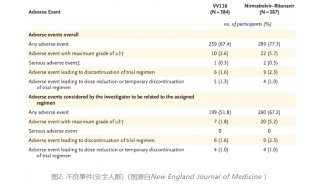
2/3期EPIC-HR试验入组的是18岁及以上确诊为COVID-19的非住院成人患者,这些患者的病情进展到严重疾病的风险增加。数据显示,在症状出现后3天内启动治疗,与安慰剂相比,接受Paxlovid治疗的患者,因任何原因住院或死亡的风险降低了89%(主要终点)。到第28天,Paxlovid治疗组没有患者死亡,而安慰剂组有9例死亡。在症状出现后5天内启动治疗(次要终点)也观察到了类似的结果,与安慰剂相比,接受Paxlovid治疗的患者因任何原因住院或死亡的风险降低88%,未观察到死亡。Paxlovid组(23%)和安慰剂组(24%)的治疗期不良事件(TEAE)具有可比性,其中大多数是轻度。
虽然Paxlovid临床试验不包括18岁以下的患者,但经授权的成人给药方案,预期在12岁及以上体重至少为40kg的儿童患者中的Paxlovid血药浓度水平达到与成人患者同等水平。额外的2/3期临床试验正在进行中,入组的是进展为严重疾病的风险为标准风险(即住院或死亡风险较低)的成人患者,以及COVID-19患者的家庭成员。
-
焦点事件

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件

-
科技前沿

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件

-
焦点事件





















