动物病毒毒力测定实验——TCID50 的测定方法
病毒感染能力测定是评估其毒力的常用方法之一,通常采用测定实验动物的半数致死量(50% lethel dose,LD50)和测定细胞培养物的半数组织(细胞)培养物感染量(50% tissue culture infectious dose,TCID50)来评估病毒的感染能力(毒力)。用细胞培养物测定病毒的 TCID50 较实验动物的 LD50 简便、经济,且易控制实辁条件,加之细胞系的同质性高,敏感性比较一致,沒:有个体间的遗传差异。所以本实验介绍 TCID50 的测定方法。
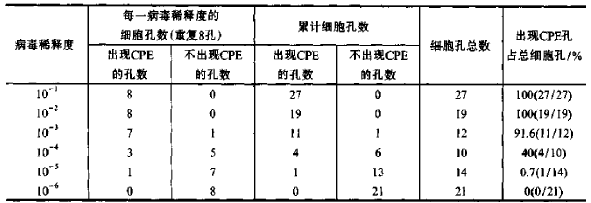
| 实验方法原理 | 溶细胞性病毒的毒力与其致细胞病变的能力直接相关,固可用不同含量的病毒液接种敏感的宿主细胞培养物测定毒力。实验中病毒的毒力以其致细胞病变效应(cytopathic effect CPE)的程度确定,即观察病毒致细胞病变的最高和最低量,以半数细胞病变为病毒感染剂量。然而,实验中所能观察到的是不同稀释病毒致细胞病变的定性结果,需要将结果统计处理,用 Reed-Muench 公式计算,才能获得病毒 TCID50 的相对定量(滴度或效价)。 为了便于理解,以一病毒致细胞病变的观察结果,介绍 Reed-Muench 公式的计算方法。 首先获得表 1 的观察结果: 表 1 病毒 CPE 观察结果 从表中可见,该病毒的 TCID50 在 10-3 和 10-4 稀释度之间。 根据 Reed-Muench 公式 TCID50=高于 50% CPE 百分率病毒稀释度的对数+比距×稀释因子的对数(1)式中,比距=(高于 50% CPE 百分率-低于 50)/(高于 50% CPE 百分率-低于 50%CPE 百分率) (2),将表 1 的数值代(2)式中,则比距=(91.6-50)/(91.6-40) =0.8。再将比距值代入(1)式中,lg10-3+0.8×lg10-1=-3.8,则 lg TCID50=-3.8,即 TCID50=10-3.8。查反对数得 6310,即该病毒 6310 倍稀释液 0.1 ml 等于 1 个 TCID50。 |
|---|---|
| 实验材料 | |
| 试剂、试剂盒 | |
| 仪器、耗材 | |
| 实验步骤 | 1. MDCK 细胞培养 常规复苏液氮冻存的 MDCK 细胞,接种于培养方瓶中,加入 7~10 ml DMEM 培养液,充分混匀,置 37℃ 培养 2~3d,待细胞形成致密单层备用。 2. 细胞悬液制备 MDCK 单层细胞一瓶,弃上清液,加 0.25% 胰酶 1 ml,消化 2~5 min,待细胞完全脱壁后加入 3 ml DMEM 培养液,充分分散细胞取样显微计数,调整细胞浓度为 2×105~5×105 /ml。胰酶消化时间不宜过长,否则对细抱造成损伤。初学者可将细胞培养瓶置显微镜下观察,细跑变圆脱壁即可。 3. 细胞接种 取 96 孔塑料细胞培养板一块,用加样器分别向每孔加入细胞悬浮液 200 ul。 4. 细胞培养增殖 细胞培养板置 37℃,5% CO2 的培养箱中培养 24 h,细胞快速生长,形成 70% 左右的单层可用于病毒接种。 5. 病毒稀释 将病毒液在 5 ml 无菌试管内作连续 10 倍稀释,即用 1 ml 吸管吸取 0.2 ml 病毒液,加到装有 1.8 ml PBS 的第 1 支小试管内(10-1),充分混匀后,更换吸管,吸取 0.2 ml 加入第 2 管中,连续如此操作,继续第 3 支稀释,如此类推,稀释到第 6 管。 病毒液中务必加少量胰酶(2.5 ug/ml),增强病毒的吸附力。 6. 病毒感 染从 CO2 培养箱中取出 96 孔细胞板,弃上清液,用 PBS 洗 2 次,于每孔加入不同稀释度的病毒 100 ul,每稀释度重复 8 孔。对照组以 100 ul PBS 代替病毒液,然后每孔补加新鲜的 DMEM 培养液100 ul,总体积为 200 ul。 7. 观察细胞培养板置 37℃,5% CO2 培养箱中继续培养。逐日用倒置显微镜观察细胞病变情况,至少观察一周。 展开 |