单克隆抗体介绍(二)
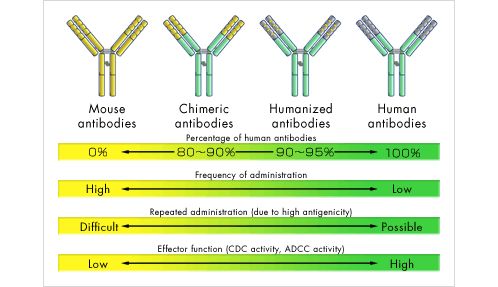
抗体筛选技术:单细胞抗体基因扩增技术2008 年, Tiller 等人发明了一种从人外周血单个核细胞快速制备单克隆抗体的方法。其主要过程包括: 经流式分选出抗原特异性单个B 细胞, 单细胞RT-PCR 与巢式PCR 组合获取抗体重链和轻链的可变区基因信息, 将这些基因克隆并在真核系统中表达。单个B 细胞的分离可以分别通过“随机分选”或者“抗原特异性分选”两种途径进行。“随机选择”的主要方法有基于显微操作的细胞分选、流式细胞分选技术等。“抗原特异性分选”的主要方法有抗原包被的磁珠分离、荧光包被的抗原多参数流式细胞分选等。此外, 近年来快速发展的单细胞测序技术使得研究人员能够更低成本、更大规模地获得B 细胞抗体基因。同时, 细胞微阵列芯片、显微雕刻技术和免疫斑点阵列芯片技术也为高通量筛选单克隆抗体分泌细胞提供了条件。与各种抗体展示技术相比, 单细胞抗体基因扩增技术能快速、直接地获得人源抗体, 特别适合在突发传染病等情况下发现有保护性的单克隆抗体。 人源抗体技术:嵌合抗体和人源化抗体由于通过小鼠杂交瘤技术制备的单克隆抗体是非人源性的, 应用于人体不可避免地会引起人抗鼠抗体反应,导至药物疗效降低, 或者引起过敏反应, 甚至威胁生命,限制了单克隆抗体的临床应用。为了克服这种缺陷, 20世纪80 年代中期, 研究者们寻求以基因工程技术对鼠源性单克隆抗体进行改造优化, 尝试对其进行人源化处理。如将鼠源抗体可变区与人抗体恒定区拼接而形成“嵌合抗体”, 或将鼠抗体可变区的互补决定区(complementarity determiningregion, CDR)与人抗体的互补决定区互换构成“人源化抗体”。“嵌合抗体”的人源程度可达60%, “人源化抗体”可达90%~95%。这虽然在极大程度上保持亲本抗体的特异性和亲和力, 但仍不是真正意义上的人源抗体,仍无法完全避免进入人体后发生排斥反应或超敏反应。
人源抗体技术:抗体基因人源化小鼠虽然各种抗体展示与筛选技术为制备人源单克隆抗体提供了选择, 但是由于展示文库多样性不足或者抗原使用等方面因素的限制, 获得理想抗体特别是高亲和力单克隆抗体的效率仍然偏低。直接由人B 细胞构建抗体基因人源化小鼠, 并通过自然筛选过程产生高亲和力人源抗体是正在发展中的技术变革, 有望成为最具优势的抗体药物研发平台。该技术需要将小鼠抗体基因替换成相应人抗体基因, 并且通过正常的抗体基因重排与克隆选择过程发育出表达人源抗体的B 细胞。目前, 构建这种人源化小鼠的基本方法是在鼠胚胎干细胞(embryonicstem cell, ESC)中进行同源重组使得鼠原有抗体基因缺失,破坏其免疫系统,再通过显微注射、逆转录病毒载体、酵母人工染色体系统或者精子介导外源DNA转移等技术将重建的人源抗体胚系基因位点转入小鼠体内,最终由杂交瘤技术或者抗体库技术筛选出靶向的单克隆抗体。 HuMAb-Mouse 与XenoMouse 是目前最为成熟的转基因小鼠技术平台。由于人源化小鼠的抗体是在体内产生, 经历正常发育和成熟过程, 其产生的抗体相对于其他技术具有较高的靶结合亲和力。但是, 该技术尚存在不足之处, 包括由于仅导入部分人源基因引起的抗体多样性低, 对小分子化合物免疫原性较弱, 不适合针对生物毒素等对机体有害的人源抗体的制备以及所制备的抗体含有鼠糖基化修饰等。
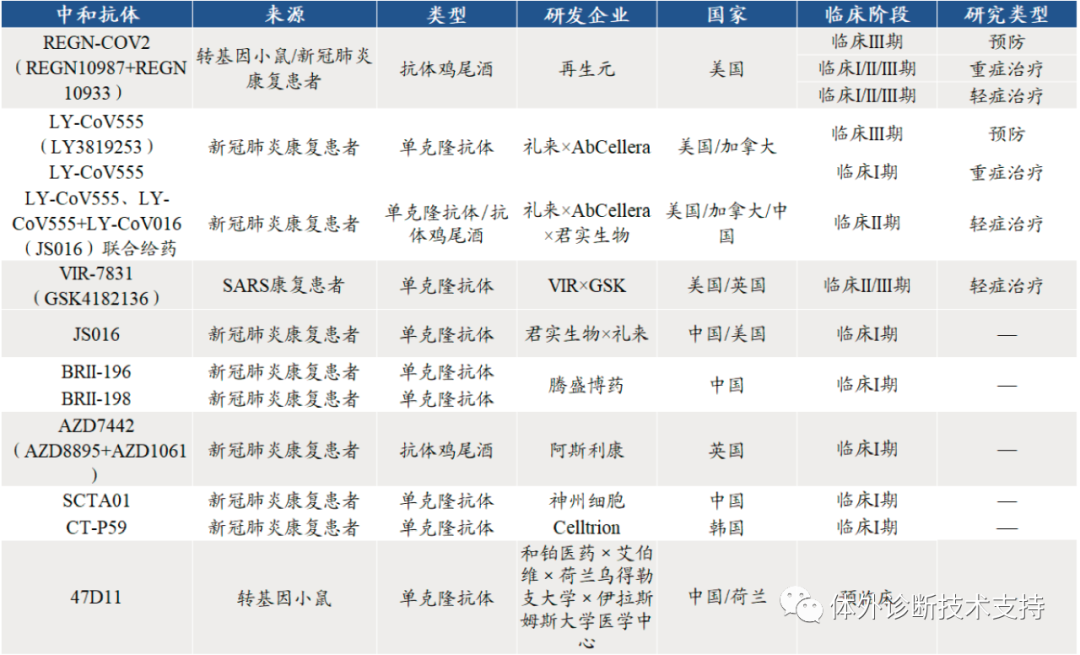
单克隆抗体在基础研究中的应用Köhler 和Milstein 的发现创立了具有划时代意义的单克隆抗体技术, 对生物医学的影响是巨大的。单克隆抗体在研究中主要用于两个方面: 第一,用于研究抗体本身的性质及其产生的机理;第二, 用于生产与特定蛋白质或其他特定分子结合的试剂。 在第一方面,相比之前无法确保同质性和特异性的抗体制备, 使用新技术生产的高纯度、高浓度的单克隆抗体自然对抗体特异性的研究有更大的帮助。此后不久, 人们便发现抗体的可变区(V)和恒定区(C)是由不同的基因片段编码的。 B 细胞将这些基因片段连接在一起, 便形成了识别不同抗原的抗体。其中具有结合抗原能力的抗体可变区,其基因片段会进行高达1012 种可能性的重组, 抗体库的多样性由此产生。另外由于抗原刺激介导的体细胞超突变(somatic hypermutation)使得抗体应答进程中抗体亲和力不断提高, 也就是抗体亲和性成熟(affinity maturation)。单克隆抗体技术推动了在分子层面阐释抗体产生的分子机理。此外, 由于抗体在免疫系统中的核心地位, 单克隆抗体技术的出现, 也让人们对获得性免疫和体液免疫有了更进一步、更深层次的了解。 在第二方面,单克隆抗体技术提供了对生物大分子(主要是蛋白质)进行准确定性、定量、定位的手段, 如今已经渗透到生物医学研究的各个方面, 诸如通过细胞表面蛋白标记对细胞进行分类筛选分析的荧光细胞分选技术、展示细胞内特定蛋白定位的高分辨率荧光显微镜、检测蛋白质混合物中特定蛋白表达量的蛋白印迹法(Western blot)、常用于血清中细胞因子表达量测定的酶联免疫吸附测定(enzyme-linkedimmunosorbnent assay, ELISA)等, 这些技术的特异性和分辨率都离不开高质量的单克隆抗体试剂的助力。值得一提的是, 得益于荧光标记单抗的发展, 我们现在已经能够在单细胞水平对细胞表面的蛋白质标志物表达图谱进行高通量的绘制与分析。 单克隆抗体在医药领域的成功尽管早期对抗体的产生和作用机制了解得并不透彻, 但是自从被发现以来, 抗体就被医学界和工业界应用于早期的血清疗法、疾病诊断等多个方面。单克隆抗体技术的出现, 更为抗体类药物的发展插上了腾飞的翅膀。 1986 年, 仅仅在单克隆抗体制备技术诞生10 年后, 美国FDA 就批准了全球首个治疗性鼠源单抗, 一种名为muromonab-CD3 的抗CD3 抗体, 用于治疗器官移植后同种异体排斥反应。随后几十年, 单克隆抗体类药物在生物医药领域得到了飞跃式发展, 如今已经有约千亿美元的巨大市场, 并且在可预见的未来仍将继续增长, 再加上抗体在疾病诊断上难以替代的地位, 单克隆抗体在医药领域的应用可谓是公认的成功。 最初,把来源于小鼠的单克隆抗体用于人类疾病治疗,但在人体内半衰期短且引发免疫排斥风险等问题, 效果并不好。这是因为人体的免疫系统会把小鼠的抗体蛋白识别为“异己”成分, 并产生针对小鼠抗体的抗体; 但小鼠抗体的恒定区段无法和人类细胞的新生Fc 段受体(FcRn, 也被翻译为滋养层细胞表面相应受体)结合, 从而难以在人体循环系统中稳定存在。为解决这个问题, 1988 年, Greg Winter 团队首先发展了人源化嵌合单克隆抗体。他们将抗体基因中与特异性无关的恒定区替换为人类抗体的同源区段, 在没有丧失特异性的前提下提高了单克隆抗体药物在人体内的稳定性, 这是单抗临床应用领域的重要进步。人源化嵌合单克隆抗体并不完美, 因为对人体的免疫系统来说, 毕竟嵌合的抗体分子中仍有非人源成分, 人体强大的免疫系统依然能够识别它们并产生针对嵌合抗体的抗体。为了进一步减少单克隆抗体中的鼠源成分, 研究者们索性将鼠抗体上的超变区氨基酸结构域直接移植至人源的抗体分子, 从而改良出比嵌合抗体更先进一步的、分子结构同源性达到95%的人源化抗体。即使如此, 鼠源抗体的Frame Region 还是无法彻底的人源化, 但是人类追求卓越的脚步并未停止。随后不久, 借助分子生物学及基因工程技术等的快速进步, 噬菌体抗体库技术、核糖体展示技术、RNA-多肽融合技术和人类抗体库转基因小鼠制备技术的发展最终实现了全人源化抗体的飞跃 。 在肿瘤与自身免疫性疾病治疗方面, 单克隆抗体获得的成功尤其令人瞩目。现在临床上使用的利妥昔单抗(Rituximab)就是一种抗CD20 人-鼠嵌合性单克隆抗体, 也是第一个被批准用于肿瘤治疗的单克隆抗体, 主要应用于B 细胞非霍奇金淋巴瘤。利妥昔单抗能够显著延长肿瘤患者的无进展生存和5 年总生存率, 在肿瘤内科治疗史上具有划时代的意义。而单抗类药物中的“明星产品”——阿达木单抗(Adalimumab/Humira)则是一种抗TNF-α 全人源化单克隆抗体, 自2003 年美国FDA 批准以来已经在全球90多个国家获批治疗类风湿关节炎、幼年特发性关节炎、强直性脊柱炎、银屑病关节炎、克罗恩病等15 个适应证, 相关系列产品的年销售额近200 亿美元, 位列全球抗体类药物销量首位, 其疗效及安全性得到了广泛验证与认可。近年来更是诞生了抗体-偶联药物、双特异性及多特异性抗体、抗体融合蛋白、小分子抗体等多种新型单克隆抗体, 使得单抗类药物具有更大的生命力及发展前途。 针对传染病的单克隆抗体也有其发展前景, 正如百多年前Berhing 和Kitasato 所期待的那样。新临床研究显示,两种治疗埃博拉出血热的单抗类药物MAb114 和REGNEB3可有效降低感染者的死亡率, 其疗效均优于既往被寄予厚望的其他药物。 MAb114 是一种从1995 年刚果埃博拉幸存者的血液中提取筛选的单克隆抗体。 REGN-EB3 则是再生元公司开发的3 个全人源化抗埃博拉病毒单克隆抗体组合而成的“鸡尾酒”。这两种单抗类药物为战胜埃博拉病毒带来了新的希望和曙光。同时, MAb114 的成功也再次将康复病人血清抗体的治疗作用推向了研究的“风口浪尖”,更让人们想起了2003 年SARS(severe acute respiratory syndrome)时期, 将病愈个体的血清注入SARS 患者体内从而治愈病患的情况。 当前新型冠状病毒正在全球横行肆虐, 其传染性之强、致病率之高让人措手不及, 而常规临床“特效药”的缺乏更是阻碍了疫情的防控及治疗。那么此时新型冠状病毒病愈患者的血清抗体是否可以成为临床治疗的一种选择,研究者们是否能够从康复患者血清抗体中筛选出如MAb114 一样有治疗前途的抗新型冠状病毒单克隆抗体呢?为了寻找新冠肺炎(COVID-19)的有效疗法,中和抗体具有预防与治疗的双重作用,有望成为新冠“特效药”。目前全球共有12 个中和抗体项目进入临床,其中进展较快的中和抗体研发项目包括由再生元(Regeneron)公司开发的中和抗体鸡尾酒疗法REGN-COV2,礼来和加拿大AbCellera 公司联合开发的中和抗体LY-CoV555,Vir Biotechnology 和GSK 联合开发的VIR-7831。REGN-COV2和LY-CoV555 已进入以预防为目的的III 期临床试验阶段,三者均已进入以治疗为目的的II/III 期临床试验阶段。国内公司中,君实生物和中科院微生物所合作开发的JS016 领跑,成为中国第一个、全球第二个进入临床试验的新冠病毒中和抗体疗法。
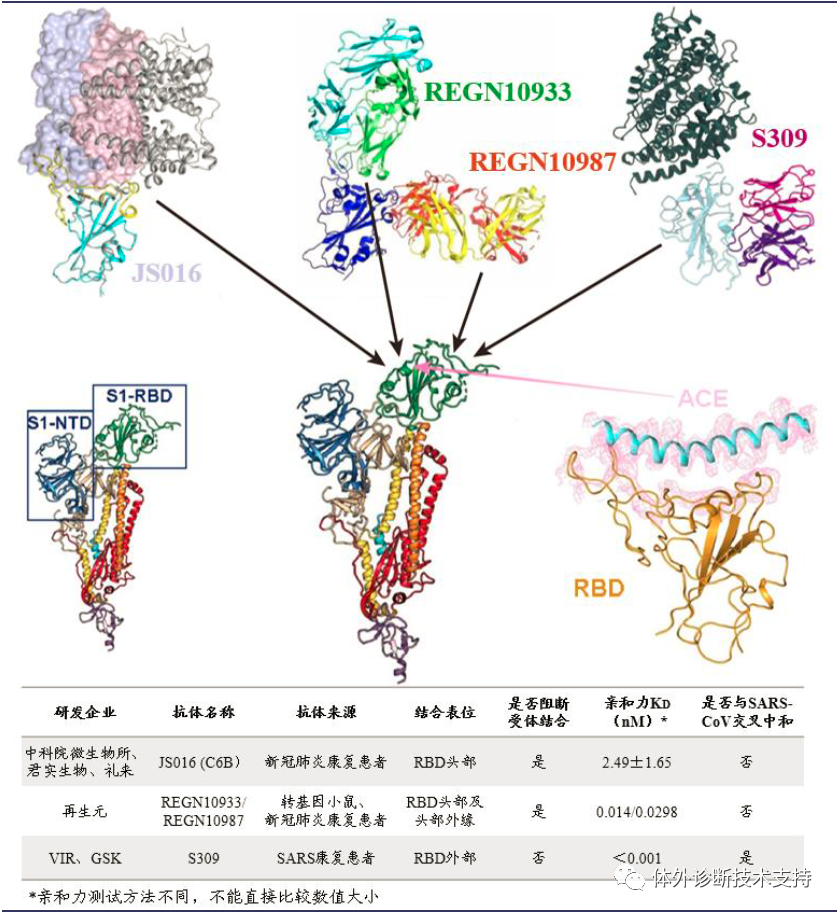
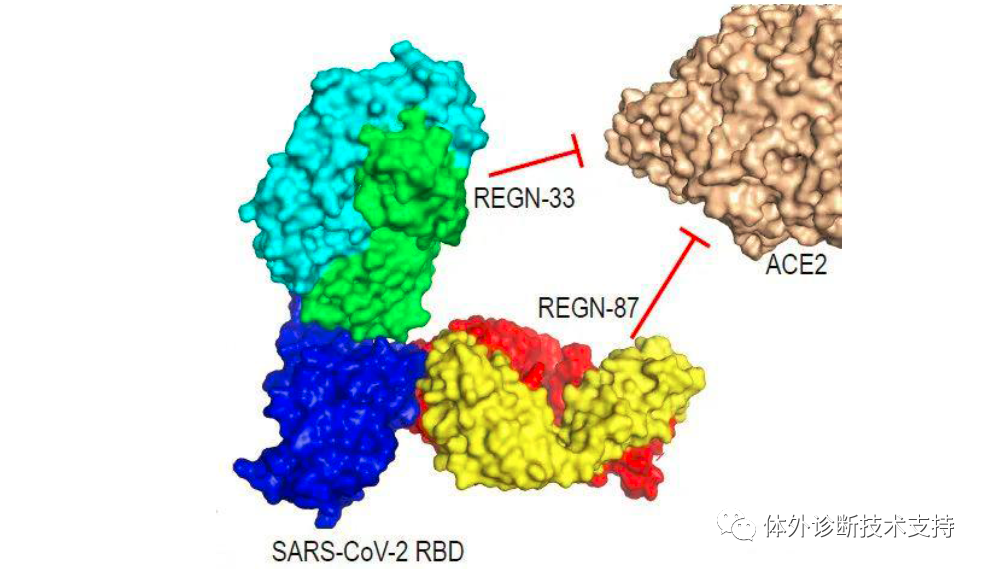
1988 年,再生元(Regeneron)公司由伦纳德•施莱弗尔和乔治•雅克波罗斯创立于美国纽约;1991 年,公司在纳斯达克挂牌上市。成立之初,再生元的定位是研究神经生长因子,试图开发治疗神经系统疾病的药物,但先后均已失败告终。之后公司调整战略方向,开发出“Trap”技术平台,并基于此贡献了著名的眼科药物EYLEA。同时,再生元还开发并整合了另一个值得称道的技术平台VelociSuite®,用于发现、开发和生产人源单克隆抗体,并以此为基础研发出Praluent,Dupixent,Kevzara 和Libtayo 等成功药品。发展至今,再生元已经成为一家从事药物发现、开发、生产和销售的集成化生物制药公司,拥有员工8100 人,拥有7 款美国FDA批准上市的药品。 再生元主要有三大核心技术平台,分别是Trap 技术平台、VelociSuite®技术平台和Cell Production 技术平台。再生元新冠抗体研发项目主要利用VelociSuite®技术平台中的VelocImmune 的小鼠模型。 目前再生元已用该技术成功研发了埃博拉病毒中和抗体药物REGN-EB3、MERS 病毒中和抗体RGEN3048-3051。新冠疫情爆发后,2020 年2 月3 日,再生元宣布与美国卫生和公共服务部(HHS)合作,共同研发针对新冠病毒SARS-CoV-2 的治疗性抗体药物。根据再生元公司披露的预期进度,3 月已经完成预防和治疗性中和抗体的筛选,4 月份推进动物实验,6 月开始小规模生产,进行初期临床试验;并在8 月份扩大生产规模,达到每月几十万份的预防剂量或几万份的治疗剂量。 再生元的新冠病毒抗体药物名为REGN-COV2,是由REGN10987和REGN10933两个单抗组成的鸡尾酒抗体药物。再生元基于VelocImmune 转基因小鼠模型和新冠肺炎康复患者血液这两条途径初步筛选出200 多个候选抗体,最终根据候选抗体和S 蛋白的结合能力、中和能力以及三维结构表征等参数筛选出两个最合适的单抗组成“鸡尾酒”疗法。REGN10987 和REGN10933 非竞争性且同时与SARS-CoV-2 病毒S 蛋白的关键受体结合域(RBD)结合,阻断病毒RBD 与人体细胞受体ACE2 的结合界面。其中REGN10933 靶向处于ACE2 结合界面边缘的刺突样环状区域,REGN10933 从上方结合病毒RBD,极大的阻碍了病毒RBD 和宿主细胞ACE2 的结合;而REGN10987 从正面和左下方结合病毒RBD。
美国国防部签订REGN-COV2鸡尾酒抗体的制造和供应协议。根据协议,美国政府将花费4.5 亿美元购买相当于7-30 万治疗剂量,或42-130 万预防剂量的REGN-COV2 鸡尾酒抗体药物,具体给药剂量将在临床试验中进行评估并加以确定。再生元预计可在夏末生产出第一批药物,秋季完成全部的药物生产。 2020 年8 月19 日,再生元与罗氏共同宣布达成新冠中和抗体药物的生产合作。罗氏拥有全球最大的抗体药物生产基地,与罗氏合作后,再生元生产抗体药物的能力将至少提高3.5 倍。两家公司将合作开发和制造鸡尾酒抗体药物REGN-COV2,再生元负责REGN-COV2 在美国的销售,而罗氏将负责该药物在全球范围内(美国以外)的分销。 2020 年9 月14 日,再生元与牛津大学宣布将开展一项3 期临床试验RECOVERY(Randomised Evaluation of COVid-19thERapY),以评估再生元鸡尾酒疗法REGN-COV2 在2000 名英国住院患者中的治疗效果,主要评估REGN-COV2 对患者死亡率,住院时间和通风需求的影响。
疟疾、流感以及AIDS等常见传染病的猖獗还催生了广谱中和单克隆抗体(broadly neutralizingantibodies)的概念。这类单克隆抗体的联合使用与AIDS 治疗领域传统化学药物“鸡尾酒”疗法可能有着异曲同工之意, 人们期望这类药物的应用可以针对传染性疾病提供广泛的预防和保护作用。单抗在生物医药领域内更具创新性的尝试还有许多, 例如利用非抗体类受体的配体结合结构域来替代抗体可变区段的抗体工程技术。然而, 研究发现, 天然的免疫系统有时也会使用类似的花招, 但总体上来说, 至少在目前, 人工设计抗体的手段还无法在效率和特异性上与历经千万年进化历程考验的免疫系统相比。
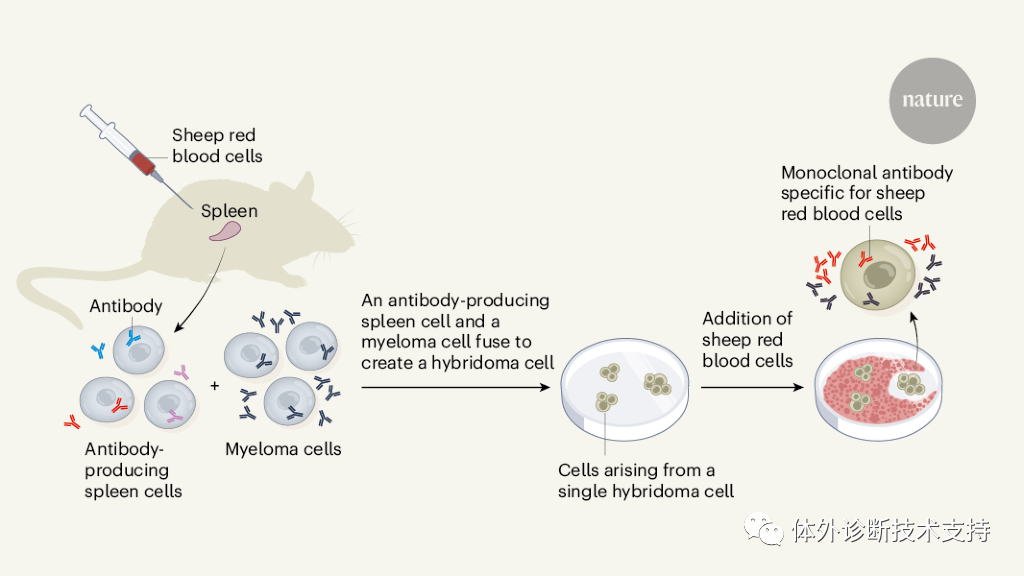
尤其值得一提的是,免疫检查点抑制剂药物anti-PD-1(如已在国内上市的施贵宝公司的纳武单抗Opdivo 及默沙东公司的派姆单抗Keytruda)和anti-CTLA-4(如施贵宝公司的易普单抗Yervoy)就是单抗类药物家族中的重要成果代表。免疫疗法背后的详细作用机制虽然仍未完全解明,但大量基础和临床层面的研究正在如火如荼地进行, 这些研究势必将会提供新的挑战和视角, 并将继续推动针对其他靶点的单克隆抗体药物的发展。 现在单克隆抗体的制备已经不再依靠杂交瘤技术, 而是直接从免疫过后的动物或病人体内分离细胞, 再将这些细胞内编码特定抗体的基因转入合适的细胞系中, 来制备我们需要的单克隆抗体。随着技术的不断发展与完善,单克隆抗体已经渗透在人们生活的方方面面。尤其是在生物医药领域, 单克隆抗体已当之无愧地成为主流新秀。科技的发展、人们的需求以及广阔的前景促使着单克隆抗体研究不断深入, 我们期望着将来会不断有更优化的单克隆抗体产品问世, 守护健康, 造福人类。 值得我们铭记的是,单克隆抗体过去、现在和明天的传奇是从1975 年Köhler 和Milstein 在实验室里制作的那几个涂上了绵羊红细胞的琼脂平板这样最基础的科学研究开始的!