大观霉素间接竞争性ELISA的建立及应用
大观霉素(spectinomycin,SPE)是一种氨基糖苷类广谱抗生素,是Mason于1961年首次从链霉菌中分离得到[1]。从结构上讲,氨基糖苷类抗生素分子中均含有氨基糖苷结构。而SPE(图1)是一种氨基环醇类抗生素,没有氨基糖苷结构,但在许多文献资料中SPE都被归为氨基糖苷类药物。在临床中,SPE多采用盐酸大观霉素的形式,是常用的治疗猪的细菌性肠炎和鸡的呼吸道疾病的口服药[2]。SPE常被用作畜禽饲料添加剂,用于治疗和预防疾病。与其他抗生素一样,SPE在畜禽养殖中被严重滥用,在动物体内蓄积,并通过食物链传递给人类,相当于长期低剂量的服用SPE,导致肌体内细菌的耐药性增加,进而破坏肌体的提抗力,引发过敏反应、听神经损害等。农业部“235”号公告明确规定了大观霉素在动物性食品中的残留限量为500 µg/kg,在牛奶中不得超过200 µg/L[3]。GB 29685-2013规定检测动物性食品中大观霉素的方法是GC/MS [4]。
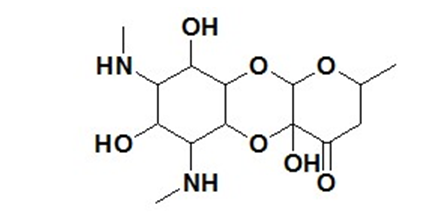
图1大观霉素化学结构式
Fig. 1 The chemical structure of spectinomycin
建立大观霉素残留快速检测方法具有重要意义。本研究在前期抗原抗体制备的工作基础上[5],建立了SPE的ELISA检测体系及其在动物源性食品中残留的检测方法,基于此项研究工作开发的检测试剂已实现商品化。
1 材料与方法
1.1试剂
大观霉素、庆大霉素、新霉素、卡那霉素、双氢链霉素、链霉素购自中国药品与生物制品鉴定所,羊抗兔酶标二抗、牛血清白蛋白(BSA)、Proclin 300、明胶、Tween-20、酪蛋白等购自sigma 公司;ELISA酶标板,深圳金灿华;新生牛血清购自北京元亨生物;其他分析纯化合物均购自北京国药集团。大观霉素包被抗原、大观霉素多克隆抗体由本公司制备。
ELISA所用的缓冲溶液:
(1)包被缓冲液:0.05 M碳酸盐缓冲液,pH 9.6;
(2) 磷酸盐缓冲液(0.02M,PBS):1000 mL 0.01M PB缓冲液中加入8.5 g NaC1,0.02 g KCl,pH 7.4;
(3)洗涤液:1000 mL PBS加入0.5 mL Tween-20;
(4) 酶稀缓冲液:2 mL Tween-20、1 g明胶、200 mL新生牛血清(使用前56℃灭活30 min)、0.2 g酪蛋白和300 μL ProClin 300,加入到0.02 M PBS中,定容到1000 mL;
(5)封闭液:1000 mL PBS加入2.5 g酪蛋白、3%BSA、5%蔗糖和300 μL ProClin 300;
(6)抗体稀释液:0.01M PBS中加入300 μL ProClin 300、200 μL Triton 100、0.1% BSA,定容到1000 mL。
1.2 仪器
MK3酶标仪(美国,Thermo fisher公司);TDL-40C离心机(上海安亭科学仪器厂);HQ-60型涡动仪(北京方正生物科技发展有限公司);电子分析天平(德国,赛多利斯科学仪器公司);Milli-Q型超纯水仪(美国,Milli-Q 公司);微量移液器(德国,Eppendorf公司);SH-2 微孔板脱水仪(北京双和盛源科技发展中心)。
1.3 方法
1.3.1 建立大观霉素的标准抑制曲线
首先,用方阵法筛选包被抗原、抗体的工作浓度,并对包被方式、加样体系进行选择,然后建立SPE的icELISA标准曲线:
(1)包被:根据方阵法确定的浓度稀释包被抗原,每孔100 μL,4℃过夜包被(16h),弃包被液,洗涤一次;
(2)封闭:在每孔中加入150 μL封闭液,室温下封闭2 h,弃封闭液,甩干;
(3)干燥:将甩干后的酶标板倒扣至于37℃恒温箱中,干燥1 h。
(4)加样:将50 μL不同浓度的SPE标准品平行加入微孔中,标准品浓度设置为:0,0.2,0.6,1.8,5.4,16.2 ng/mL。然后顺序加入50 μL酶标二抗工作液、50 μL SPE抗体,室温下(25±2℃),避光反应30 min,洗涤四次;
(4)显色:在每孔中加入按照同样比例刚混合的底物液100 μL,避光孵育8-10 min;
(5)读数:每孔加入50 μL终止液终止,5 min内在450 nm/630 nm 双波长下读出数据;
以SPE标准品浓度的对数为横坐标,不同浓度的SPE标准品的结合率为纵坐标,用软件Origin8.0绘制标准曲线,建立四参数回归方程。回归方程如下:
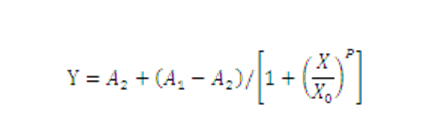
其中Y为结合率,A1代表最低浓度标准品的结合率,A2是最高浓度标准品的结合率,P为曲线拐点的斜率,X0为IC50。
1.3.2 抗体的特异性
以icELISA法分别考察SPE抗体与氨基糖苷类抗生素:庆大霉素、新霉素、卡那霉素、双氢链霉素、链霉素的交叉反应,建立上述药物的标准抑制曲线,并计算各自的IC50,按下式计算交叉反应:
交叉反应(CR%)=IC50(SPE)/IC 50(有关化合物)×100%
1.3.3 样本分析
1.3.3.1 牛奶样本
准确量取0.1 mL牛奶样品于2 mL离心管中,加入0.9 mL 含0.01% Tween-20的去离子水,慢速涡动混匀后取50 µL进行检测。稀释倍数:10。
1.3.3.2 组织样本
准确称取1±0.01 g 均质后的组织样本(猪肉、鸡肉)于50 mL离心管中,加入5 mL 0.01M PBS,充分涡动1 min;4000 g离心10 min;取200 μL上清于新的离心管中,再加入400 μL 0.01M PBS,充分涡动20 s;取50 μL进行检测。稀释倍数:18。
2 结果
2.1 SPE标准抑制曲线
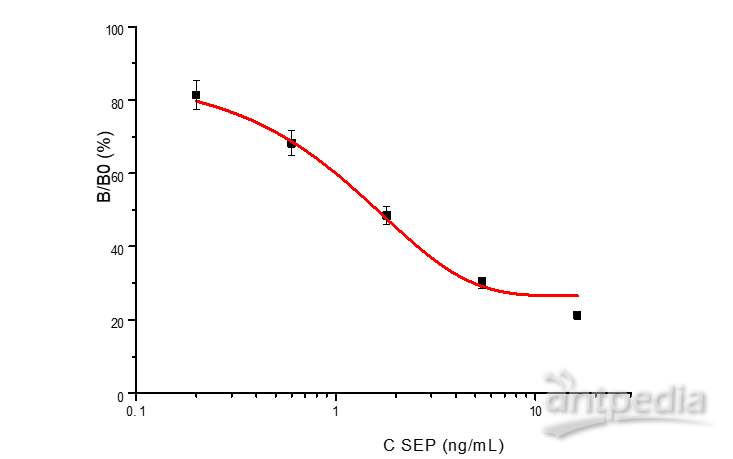
图2 SPE的标准曲线
Fig. 2 The standard curve for SPE by icELISA
对各种工作条件(包括抗原、抗体浓度,酶标二抗浓度、包被方式、抗体稀释液、加样体系、反应时间等)进行优化。根据IC50和ODmax确定最佳工作浓度,总原则是选择使标准曲线IC50值更低、ODmax范围在1.8~2.2的工作条件。图2是使用四参数拟合的SPE标准曲线,IC50=1.78 ng/mL,R2=0.9926。
2.2 抗体特异性
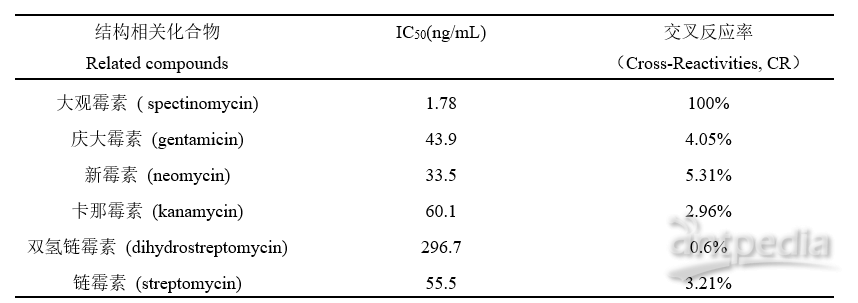
本研究所用的SPE多克隆抗体与氨基糖苷类抗生素的交叉反应情况如表1,SPE抗体与其他氨基糖苷类化合物有轻微交叉,说明抗体的特异性强,可以特异的检测待测样本中SPE。
表1 SPE与结构类似物化合物的交叉反应率
Table 1 The cross-reactivity of SPE with related compounds
2.3 样本检测
2.3.1 确定检测限(LOD)
分别测定20份牛奶、鸡肉、猪肉样本的空白组织,取其测定平均值(X)加3倍标准差(SD),即LOD =X+3SD,计算SPE在牛奶、鸡肉、猪肉的LOD分别为4.8 µg/L、9.3 µg/kg和10.0 µg/kg。
2.3.2 添加实验
准确度和精密度是评价检测方法可靠性的重要指标,在ELISA工作中,准确度和精密度分别用回收率和精密度来评价。根据检测线性范围及检测要求,SPE在牛奶中的添加浓度为4.8 µg/L、9.6 µg/L,在鸡肉中的添加浓度为9.3 µg/kg、18.6 µg/kg,在猪肉中添加浓度为10 µg/kg、20 µg/kg。每种样品分别取三个不同批次,每个批次5个样本,按照本试验确定的ELISA方法检测并计算批内和批间的回收率及其变异系数。
表2 SPE在三种样本的回收率和变异系数
Table 2 The recoveries and coefficient of variation in the three samples of SPE
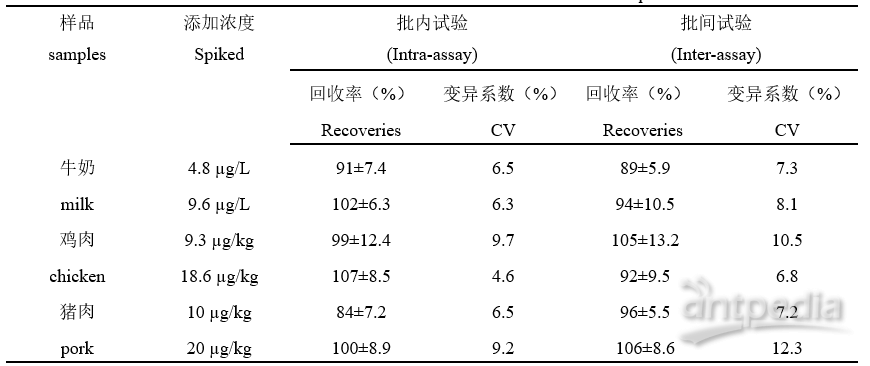
从表2可以看出,在牛奶、鸡肉、猪肉样品中添加不同浓度的大观霉素,批内添加回收率在77.1%至116.0%,批内变异系数在4.6%至9.7%,批间添加回收率在82.3%至118.2%,相应的批间变异系数在6.8%至12.3%。无论是批内还是批间,所有样本的添加回收率均在70%至120%之间,变异系数也都小于15%。结果表明新建立的检测SPE残留的ELISA方法在准确性和精密度上达到了兽药残留检测的要求[6]。
1.3.3 与仪器分析比较
ELISA与GC/MS比较结果见表3。GC/MS条件:色谱柱,毛细管色谱柱Rtx-5,30m×0.25 mm;载气,氦气;柱流速:1mL/min;进样体积:1µL;进样口温度:280℃;扫描离子:145,171,187,201。
表3 IcELISA测定结果与GC/MS测定结果的比较
Table 3 The comparison of results determined by indirect competitive ELISA and GC/MS
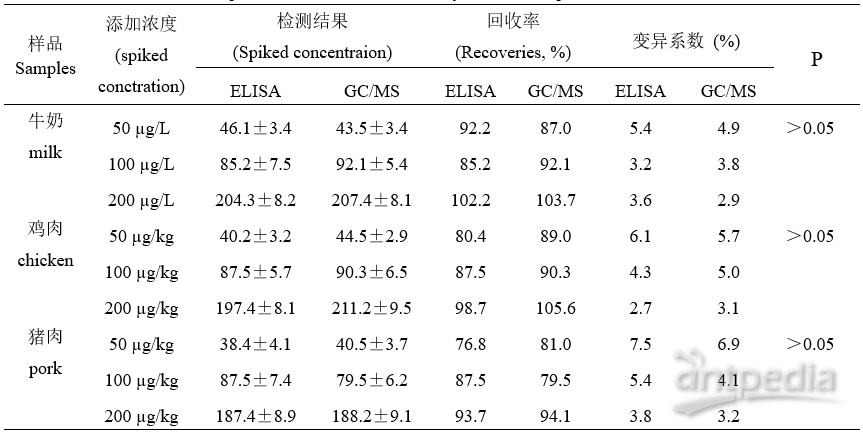
GC/MS检测限是50 µg/kg(µg/L),这个浓度的SPE对于ELISA来说,还需要进一步稀释才能分析。牛奶样本需要稀释10倍,组织样本稀释5倍后应用于ELISA。由表3可知,经单因素方差分析,两种方法的分析结果无显著性差异(P>0.05),进一步说明,本研究所建立的ELISA方法可用于牛奶及组织样品中SPE的检测。
3 讨论
本研究工作的目的是建立大观霉素的ELISA方法并将其应用于样本检测中。关于大观霉素免疫分析方法,国内外报道较少,但都局限于抗体制备及ELISA方法建立,没有关于应用性的研究报道[1,5,7]。
研究过程中发现,反应时间的长短对最后的反应结果会有很大的影响。抗原-抗体的结合是一个动态平衡的过程,需要一定的反应时间达到所谓的“平衡”的状态。时间过则短体系还没有充分反应,这种情况下中断反应会使得反应结果太过依赖操作时间,重复性不好;时间过长虽然反应已充分,但过长的反应时间导致外界影响因素增多,使得反应出现不正常的平衡移动,从而干扰反应结果,影响检测的准确性。在本研究中,反应时间30 min时反应已达到平衡,此时反应灵敏度最高。随着时间的推移,灵敏度反而变小,因此选择反应时间为30 min比较合理。
为满足市场对快检产品的要求,本研究依靠高灵敏度的抗原、抗体,通过对各个条件进行优化,采用“一步法”(one-step),即标准品、酶标二抗、一抗按照顺序先后加入微孔板并进行孵育反应,而不是分成“标准品+一抗”、“酶标二抗”两步进行,减少了其中的洗板过程,简化了反应步骤,适应了市场对快检产品“快”的要求。
参考文献
[1] Thacker, J. D., Casale , E. S., Tucker, C, M. Immunoassays (ELISA) for Rapid, Quantitative Analysis in the Food-Processing Industry [J]. J. Agric. Food Chem. 1996, 44, 2680-2685
[2] Medina A B. Development of a Fluorescent Latex Immunoassay for Detection of a Spectinomycin Antibiotic [J]. J. Agric. Food Chem. 2004, 52, 3231-3236.
[3] 中华人民共和国农业部。GB 29685-2013 动物性食品中林可霉素、克林霉素和大观霉素多残留的测定 气相色谱-质谱法 [S]。2013-09-16。
[4] 中华人民共和国农业部。农业部235号公告:动物性食品中兽药残留最高限量[EB/OL]。http://www.moa.gov.cn/zwllm/tzgg/gg/2002-12-24。
[5] 王照鹏,李向梅,王文珺等。大观霉素人工抗原的合成及其多克隆抗体制备[J]。中国畜牧兽医,2014,41(2):54-57。
[6] 中华人民共和国农业部。农医发[2005]17号:兽药残留酶联免疫试剂(盒)备案参考评判标准[S]。2005-06-23。
[7] 曹馨匀,张云涛,杨福军等。大观霉素酶联免疫吸附检测方法的建立[J]。兰州大学学报(医学版),2009,35(2):44-46。
文章来源:《动物医学进展》,2016,37(1):43-46