刘昌孝:认识SARS-CoV-2,抗病新药研发策略该从“何”说起
过去100年发生的多起事件让世人密切关注未来发生传染病大流行的风险。2018年是1918年流感流行的100周年,估计有数千万人死于100年前那次流感。现在拥有比一个世纪前更好的干预措施,季节性流感疫苗,但不一定完全有效预防。每年需要接种或选择接种的人所占比例较小。世界上还有抗生素可以帮助治疗细菌性肺炎这类继发性感染。然而虽然有进步,但传染性疾病的防控问题并未根本解决。疾病建模研究所(Institute for DiseaseModeling)提供的一项模拟显示如果一种传染性高且通过空气传播的致命病原体在今天出现,例如1918年的流感,将会发生——全球近3300万人将在短短6个月内死亡(图1)。

图1. 1918年世界流感地图(来源:Institute for Disease Modeling)
2003年的SARS从中国广东开始,后在国内传播,并扩散至东南亚乃至全球,直至2003年中期疫情才被逐渐消灭的一次全球性传染病疫情突发事件。流行漫延,引起社会恐慌,造成全球包括医务人员在内的约八百死亡,中国和世界各国对该病的防控处理战胜了流行。后经科学研究将感染疾病的病毒命名为SARS-CoV。联合国、世界卫生组织和中国政府高度关注和重视,有名北京小汤山医院为控制疫情发展创下了奇迹。难忘的经历至今一直留在记忆中。
2019年末,在中国出现新型冠状病毒(SARS-CoV-2,此前称 2019-nCoV)感染疾病以来,疫情的发展引起世界关注。世界卫生组织(WHO)高度关注,多次专家会议最后认定这次疫情是一次“国际关注的突发公共卫生事件”。自疫情确定以来中国举国上下一直将防控疫情,保卫人民生命安全作为全党全国的第一要务。中国采取了认真负责任的积极措施,甚至不惜一切代价,严防严控,控制疫情在最小范围内播散。
本专论主要从综述冠状病毒(SARS-CoV-2)的认识出发,思考一些抗病毒药物研发策略。就药物而言,对病毒性疾病预防用疫苗和治疗用药物是重要组成部分,但创新需要时间来完成,认识这类药物的研发难点,才有利于抗病毒药物研发,而不至于束手无策。
1. WHO关于新型冠状病毒感染性疾病和病毒的命名
2020年2月11在日内瓦召开的全球研究与创新论坛上。WHO总干事谭德塞在记者会上宣布将新冠状病毒命名为“COVID-19”。根据世界卫生组织(WHO)、世界动物卫生组织(OIE)和联合国粮食及农业组织(FAO)之间议定疾病原命名原则,就是疾病名称不能涉及地名、动物、个人或人群名称或包含信息。在听取业界专家建议之后,WHO正式命名新型冠状病毒和疾病为“COVID-19。总干事说正式名称很重要,防止使用不准确或带有污名的名称。也是为以后任何冠状病毒疫情爆发确定了“标准格式”,比如说再新型冠状病毒就是“COVID-xx”。COVID-19疫情是全世界公共卫生共同疫情。

图2. WHO总干事谭德塞在记者会上
基于最新疫情报告将技术,其重点放在新型冠状病毒的人畜共患病成分上的原因。越来越多的证据表明,2019新型冠状病毒与其他已知的在蝙蝠中传播的冠状病毒存在,证明其存在与蝙蝠亚种菊头蝠(Phinolophus bat)关联。国际病毒分类委员会(International Committee onTaxonomy of Viruses, ICTV)声明,将新型冠状病毒命名为“SARS-CoV-2”(SevereAcute Respiratory Syndrome Coronavirus 2)。SARS-CoV和SARS-CoV-2的人畜共患病传播,人类感染SARS-CoV-2的临床表现尚待确认,凸显了对整个病毒类群进行研究的需要。
就药物而言,总干事说“预防性疫苗和治疗药物是重要组成部分,但需要时间来完成”。在获得有效疫苗或治疗新药之前,对其治疗并非束手无策,“现有的许多公共卫生和医疗干预措施也是行之有效,甚至实现有效的疫情预防和病原传播”。我认为中国的做法证明中医药的优势就是行之有效的措施,是世界其他国家都沒有的优势,也是实践证明了的优势。预防性疫苗和治疗药物是重要组成部分,但需要时间来完成。在获得有效疫苗或治疗新药之前,......今天我们还必须使用任何积极预防手段来这种病毒作斗争。本文就其新型冠状病毒及其感染疾病的防治药物的研发策略为主题予以讨论和述说。
2冠状病毒的分类与性质
2.1 冠状病毒科
从冠状病毒认识的发展历史来看,早在1937年,Beaudette和 Hudson从小鸡体内第一次分离到了冠状病毒[1]。1965 年Tyrrell等用人胚气管培养方法,从普通感冒患者鼻洗液中分离出一株病毒及其后来的研究[2-4]。1967年,Almeida等对这些病毒进行了形态学研究,电子显微镜观察,从形态学发现这些病毒的包膜上有形状类似日冕的棘突,故提出命名这类病毒为冠状病毒[5,6]。但人们对它们的认识相当有限。1975年ICTV正式命名冠状病毒科,使其目、科、属关系越见清楚。
巢病毒目(Nidovirales) 内的三个RNA病毒科是冠状病毒科(Coronaviridae)、动脉炎病毒科(Arteriviridae)和杆状套病毒科(Roniviridae),分别是存在于鸟类和昆虫病原体。冠状病毒科(coronaviridae)包括两个亚科,冠状病毒科和环病毒科,后者包含的病毒主要导致马、牛、猪、猫和山羊的肠道感染。虽然环病毒亚科的成员具有重要的经济意义,但迄今还不知它们会引起人类感染。基于50个冠状病毒系统发育树分析冠状病毒分为α、β、γ和δ4属冠状病毒[7,8]。其中对人类致病的冠状病毒主要集中在β属冠状病毒,如SARS-CoV、MERS-CoV和SARS-CoV-2(2019nCoV)。
所有冠状病毒都有一个共同的形态,并拥有一个长达30 kb的单链核糖核酸基因组。冠状病毒亚科的成员分为四个属。阿尔法冠状病毒属包含人病毒HCoV-229E、另一种人冠状病毒(HCoV-NL63)和许多动物病毒。贝塔冠状病毒属包括原型小鼠肝炎病毒(MHV)、三种人类病毒HCoV-OC43、SARS HCoV和HCoV-HKU1、与SARS-CoV、MERS-CoV以及许多动物冠状病毒。
冠状病毒基本性质可以归纳一下9要点:(1) 病毒体是80-220nm的多形性球形冠状病毒;或120-140纳米的圆盘形、肾形或棒状的圆环病毒;(2) 带有大的、间隔很宽的棒状粘合剂的封套;(3) 螺旋对称的管状核衣壳;(4) 线性ssRNA基因组27-33kb,在两端有帽状聚腺苷酸化、感染性的未翻译的序列;(5) 三种或四种结构蛋白:核衣壳蛋白(Nucleocapsid protein, N)、突刺蛋白(Spike protein,S)、跨膜糖蛋白(Membrane glycoprotein, M),有时还有血凝素酯酶(HE);(6) 基因组编码3-10种其他非结构蛋白,包括由从5’端翻译的两种多聚蛋白切割的亚单位组成的RNA依赖性RNA聚合酶; (7) 在细胞质中复制,基因组被转录成全长反向RNA,从它转录出一组3’共端嵌套的RNA,只有其独特的5′序列被翻译;(8) 病毒粒子聚集并萌发到内质网和Golgi池中;释放是通过胞吐;(9) 变异病毒很容易通过突变和重组产生,利用不同受体影响对宿主显现范围[7]。
2.2冠状病毒的结构和基因
冠状病毒病毒颗粒包含三种主要的结构蛋白: (1)非常大的(200 K)突刺糖蛋白(S),它形成在病毒包膜中发现的大体积(15-20nm)的聚体;(2)一种不寻常的跨膜糖蛋白(M)和内部磷酸化的核衣壳蛋白(N)。(3)此外还有一个较小分子的跨膜蛋白E,以及一些冠状病毒还含有一个具有血凝和酯酶功能的包膜蛋白(HE)。30 kb正单链RNA基因组是已知的最大RNA病毒基因组。图3为冠状病毒结构的模式图[7]。该类冠状病毒模式显示由突刺蛋白(S), 核衣壳蛋白(N),膜糖蛋白(M), 包膜蛋白(Envelope protein, E), 和核糖核酸(RNA)聚合链组成。决定病毒和细胞相互识别的突刺蛋白(S)的基因。研究认为突变率在不同的流行期有不同的变化,在SARS流行早期的基因变异大于流行中期,而流行中期又大于流行后期。

图3. 冠状病毒结构模式图(Model of coronavirusstructure[7])
具体说来,在5’端为被封端,具有甲基化的帽状结构,在3’端被聚腺苷酸化,具有poly(A) 尾,并具有传染性。基因组全长27-32kb, 是目前已知RNA病毒中基因组最大的病毒。由于其大小不同的单个基因的表达要通过一个复杂的过程产生,由此产生多组嵌合的信使核糖核酸(mRNA),所有这些mRNA共享相同的5’端序列。异源RNA重组的结果可能会发生广泛的重排。在基因组的5’末端是一个65-98个RNA的非翻译(UTR)序列称为前导RNA,它也存在于所有亚基因组的5’末端。在RNA基因组的3’端是另一个200-500个RNA的非翻译序列,随其后的一个多聚尾。两个非翻译区对调节RNA复制和转录都很重要。冠状病毒基因组包含7-14个开放阅读框(ORFs)。从5’端开始,基因1包含基因组的三分之二,长度约为20-22 kb。它由两个重叠的开放阅读框(1a和1b)组成,共同起着病毒RNA聚合酶(Pol)的作用[7]。结构蛋白的其他四个基因的顺序是5’-S(Spike)-E(包膜)-M(膜)-N(核衣壳)-3’。这些基因散布几个编码非结构蛋白和血红素(HE)糖蛋白的开放阅读框(ORFs)。尽管这些基因在同一血清群中是保守的,但每种基因在冠状病毒中的数量、核苷酸序列、基因顺序和表达方法上有显著差异。
2.3 SARS-CoV
在SARS病毒传染性暴发后,国内外研究者开展了大量有结构和特性的价值的研究[7,9-12]。SARS病毒基因组编码位于基因组3’区的几个较小的ORFs,其他冠状病毒不存在。这些ORFs预计表达8种新的蛋白质,被称为辅助蛋白质。在从SARS病毒患者分离的血清中检测到对所有SARS冠状病毒蛋白有反应的抗体,表明这些蛋白在体内由病毒表达。ORFs 1a和1b首先被翻译成两个多聚蛋白,两者的N末端相同,但是其中一个由于移码而具有C末端延伸。这些前体是转录-复制复合体中蛋白质。所有冠状病毒都编码一种糜蛋白酶样的蛋白酶,称为Mpro(主蛋白酶)或3CLpro,因为它与微小核糖核酸病毒(picornaviruses)的3C蛋白酶有一些相似之处。这种蛋白酶负责处理剩余的多蛋白的能力,产生多达16种非结构蛋白。
SARA-CoV属于β-冠状病毒,含有最多的非结构蛋白。如nsp3是一种多功能蛋白,具有蛋白酶和ADPribose 1”磷酸酶活性。SAILSPLpro特异性识别多聚蛋自ppla(pplab)N端nspl-2、nsp2-3和nsp3-4之间的LXGG序列,参与la(1ab)复制酶蛋白N端的切割加工并释放成熟产物nspl,nsp2和nsp3。SARS-CoV的PLpro蛋白酶结构与功能研究是近几年冠状病毒分子生物学研究的热点之一。SARS-PLpro是由非结构蛋白nsp3编码,nsp3编码7个小的结构域,在PLpro的C端编码一跨膜域TM使PLpro定位在膜上。另两种蛋白(nsp 7和nsp 8)形成一种在冠状病毒RNA合成中可能是很重要的柱状结构形式,还有一种单链RNA结合蛋白(nsp 9)。ORF1b编码病毒RNA依赖性RNA聚合酶和一种多功能解旋酶蛋白。除了解旋酶活性,该蛋白还具有NTPase和dNTPase活性以及5’三磷酸酶活性。这些非结构蛋白基因产物对病毒复制来说不是必需的,但是一个或多个的缺失通常会导致病毒衰减。至少有一种ORF3a的产物,它是一种O-糖基化的三重膜蛋白,被认为是一种结构蛋白,它能够结合N、M和S蛋白,提示在病毒生物发生中起作用。
2.4 SARS-CoV-2(2019-nCoV)
SARS-CoV-2也属于β-冠状病毒,其序列与在蝙蝠中发现的β-冠状病毒相似。新该病毒易出现就引起国内外广泛关注,国内外的研究文章给我们认识该病毒提供了有价值的信息[13-24]。发现该病毒在遗传上不同于SARS和MERS冠状病毒,与SARS冠状病毒相似,属于β冠状病毒B属 (Sarbecovirus亚属),其RNA序列长度约30 kb, SARS-CoV-2的3CL水解酶的分子结构已经被中国科学家公布, 2019年首次报道SARS-CoV-2是一种正链单股RNA冠状病毒[13-16]。 3C9L水解酶是病毒的一个关键蛋白质,病毒需要利用它来复制RNA。如果3CL水解酶的功能抑制,就可以阻断病毒复制。已经对新冠状病毒 Spike(S)蛋白的受体结合蛋白(RBD)进行了也多次蛋白质建模. 截至2020年1月底, 中国的两个研究组认为S蛋白与SARS受体(血管紧张素转换酶2, ACE2)的亲和力足够大, 病毒因此得以进入细胞。进入细胞后, 病毒会复制RNA基因组, 形成一个长的多聚蛋白, 所有的蛋白都附着于。此. 冠状病毒具有一个非结构性蛋白(蛋白酶), 它能够分离链中的蛋白. 对于病毒, 这是基因上较为经济的一种做法, 能够以少量的核苷酸编码最大数量的基因。一些临床结果也为研究该病毒的危害提供小有益证据[18-20]。
2.5 SARS-CoV-2与SARS-CoV的区别
从系统发生分析,已经将冠状病毒分为α、β、γ和δ4属冠状病毒[7,8]。其β属冠状病毒有可以分为A, B, C, D个亚属。已知β属冠状病毒中有α属的 HCoV-229E、HCoC-NL63、VHCoV-OC43、HCoV-HKU1, 和β属的SARS-CoV, MERS-CoV, SARS-CoV-2可以感染人类。但是α属与β属的危险性前者小于后者。
虽然SARS-CoV与SARS-CoV-2同属于β属冠状病毒,但是通过文献研究分析两者间的差别[21,22],认为其差异有四方面:
(1)从病毒分类角度认识:SARS-CoV和SARS-CoV-2同属于冠状病毒科、冠状病毒亚科、β冠状病毒属。类SARS病毒种。(2)SARS-CoV-2与两种来源于蝙蝠的SARS样有较大相似关系,其相似度为88%,SARS-CoV和SARS-CoV-2两者全基因组水平相似度为79%。(3)用于病毒鉴别的7个保守越与SARS-CoV的氨基酸高达94.5%的相似度。(4)SARS-CoV可以通过细胞膜表面的ACE2受体,病毒进入细胞,通过S蛋白与宿主的受体结合而达到感染的目的。 SARS-CoV-2也具有相同进入细胞的途径。而且SAR S-CoV-2的S蛋白与人的ACE2受体有显著的亲和力。证明两者在气源上有密切关系。
3新型冠状病毒SARS-CoV-2 (2019-nCoV)的研究
3.1中国科学家对所致肺炎的基础研究贡献
我们已经知道, SARS-CoV和MERS-CoV大规模暴发,感染后造成不同的病死率,而且目前特异性抗冠状病毒药物或疫苗有效治疗尚需重视。NEJM还发表了来自美国衣阿华大学的Stanley Perlman的文章[23],高度肯定了中国科学家对新型冠状病毒研究,同时指出还要在确证SARS-CoV-2(2019-nCoV)对肺炎的致病病毒、确定该病毒作为人畜共患病的最初宿主来源等开展研究,减少社会恐慌和有效控制感染,也需要从SARS-CoV和MERS-CoV的传播中汲取经验。采取社区隔离、及时诊断和严格遵守公共卫生中的普遍预防措施,出现新型冠状病毒感染时,减少SARS-CoV-2的传播和需要全球公共卫生机构提高警惕具有重要意义。
中国疾控中心(CDC)等在患者下呼吸道获得病毒株,获得完整基因序列,并绘制SARS-CoV-2(2019-nCoV)与其他乙型冠状病毒基因系统发育树图,其系列为病毒溯源的后续研究提供了充分的实验数据[13-15]。在完成完整基因组提交给GASAID网站共享,也将SARS-CoV-2基因组的特异性引物集和标准操作程序均已与WHO共享。周鹏博士等在Nature的论文显示武汉新型冠状病毒SARS-CoV-2(2019-nCoV)的序列与一种蝙蝠中的冠状病毒序列一致性高达96%,可认为引发武汉新型冠状病毒的自然宿主可能仍然是蝙蝠,但不明确其中间宿主。武汉病毒所还确认该病毒进入细胞的路径与SARS-CoV一样,即通过ACE2细胞受体,为后续疫情防控和药物研究等奠定了重要基础。论文指出自18年前SARS爆发以来,大量与严重急性呼吸综合征相关的SARS-CoV在它们的天然宿主蝙蝠中被发现,对公共健康构成了潜在威胁。先前的研究表明,其中一些蝙蝠SARS -CoV有可能感染人类[17]。周鹏等于2020年1月在BioRxiv[13]上发表文章还指出新型肺炎病毒与SARS-CoV一样,通过ACE2进入细胞。
朱博士等在NEMJ在线发表武汉不明原因肺炎病原学确证的原创性研究[16]。该论文揭示武汉新型冠状病毒SARS-CoV-2与一种蝙蝠中的冠状病毒的序列一致性高达96%。这意味着,新型冠状病毒可能与18年前的SARS-CoV一样,其自然宿主都来自蝙蝠。该研究成果的发表无疑为疫情防控提供了有力的科学支持。武汉2019-nCoV肺炎早期病例可能与武汉华南海鲜市场暴露经历有关,但可能的感染最初来源仍然不明确。
黄朝林等在LANCET线刊发了描述新型冠状病毒感染肺炎主要疾病特征的临床研究[18]。收集2019-12-16—2020-1-2期间的41例入院确诊感染病例,发现患者缺乏上呼吸道症状、肠道症状、淋巴细胞、非ICU患者影像学资料。在二代三代病例逐渐增多的情况下对临床特征的总结将协助更多临床医生“快速识别、加强管理、减少暴露、建立疾病风险”模型,为了解疾病潜在发展和制定干预措施产生效果。在危重患者中,还发现可见的细胞因子变化,为开展基础研究阐明SARS-CoV-2影响人类免疫系统提供基础认识。但是要为门诊更大规模的研究来确认疾病谱和指导优化临床防控策略还要做大量工作。在基础研究方面,香港大学袁国勇教授团队聚焦于家庭聚集性病例,通过家庭流行病学、临床、实验室和微生物学验证,证实新型冠状病毒在医院和家庭环境中出现人际传播。其在LANCET刊发了关于该新冠状病毒的遗传分析研究[20]。
2020年1月NEJM发表的文章指出,这次的新冠状病毒是过去20年来在人类中出现的第三种冠状病毒[23,24]。这些研究推动了WHO对疫情作出快速反应,WHO在1月10日发布了患者监测、标本采集和治疗指南[25],提供了有关疫情的最新信息,推动了多个国家和地区避免病毒在世界范围内进一步传播。国际药学联合会也对防控新型冠状病毒发布了一份试行指南[26]。
3.2病毒传染源宿主的证实
记得上次2003年SARS暴发时,科研者最早检测出病毒在中间宿主果子狸,进而确定了SARS病毒来源于菊头蝠。而这次新型冠状病毒NCP-CoV最早报道也发现,SARS-CoV-2与蝙蝠身上的病毒相似度很高,达到90%左右,认为这种该似度是不足以支持该病毒是直接由蝙蝠传染,因此查找中间宿主成为关键。
我们早就见到北京大学、广西中医药大学、宁波大学、武汉生物工程学院的研究人员联合完成,在线发表新型冠状病毒中间宿主的研究结果[27]。研究人员对新型冠状病毒的基因序列进行了分析,评估这些序列中的RSCU。然后将前述的冠状病毒RSCU与不同物种动物基因序列的RSCU进行比较。研究结果显示与其他动物相比,蛇最有可能是携带前述新型冠状病毒的动物。“同义密码子相对使用度”对同义密码子使用的偏好(偏倚)程度。发现基因排列在不同物种中出现的频率有差异。论文称新型冠状病毒是一种重组病毒,病毒的重组区域位于病毒的纤突蛋白,用于识别宿主细胞的表面受体,证实新型冠状病毒的部分基因序列来自蝙蝠冠状病毒。
除上述研究外,可以追溯到去年10月份,广东省动物保护中心陈金平团队就在Viruses杂志上发表文章,通过宏基因组测序分析发现马来亚穿山甲中携带有仙台病毒和冠状病毒,提醒穿山甲可能是一病毒传播者。在这11只穿山甲中发现2只个体中检测到多种冠状病毒。并利用系统发育分析,发现这些冠状病毒与四个冠状病毒属复杂关系,揭示了穿山甲中冠状病毒的复杂遗传关系和高物种多样性[28]。今年2月7日,华南农业大学发布消息,华南农业大学等科研人员联合中国人民解放军军事科学院军事医学研究院、广州动物园科研部开展研究,结果表明穿山甲为新型冠状病毒潜在中间宿主。研究团队通过分析1000 多份宏基因组样品,锁定穿山甲为新型冠状病毒的潜在中间宿主。再继而通过分子生物学检测揭示穿山甲中β冠状病毒的阳性率为 70%,结合病毒分离鉴定、电镜下观察冠状病毒颗粒结构,最后通过对病毒的基因组分析,发现分离的病毒株与目前感染人的毒株序列相似度高达 99% [29]。这些证据说明穿山甲是新冠病毒的潜在中间宿主。希望有助于疫情的科学防控,希望更多科学家开展进一步研究工作。今年2月7日,Cyranoski 在 NATUR杂志也发表新闻观点支持上述结果, Scripps研究所免疫与计算生物学专家Kristian Andersen绝对相信这一结果(来源于穿山甲)是真的,而且已经完成了相关序列的比对[30]。所以将这三种病毒传播给出如图4的途径。

图4. 冠状病毒传播的途径
在此我总觉得确定中间宿主是穿山甲还值得研究。今年1月24日,金银潭医院副院长等人在在LANCET刊载的文章里提到过,武汉新型冠状病毒第一例患者症状开始日期推定在12月1日。但是第一个病人和后来的病例之间没有发现流行病学联系。难道他就是传说中的零号病人么?但由于缺乏信息,至今仍不能完全锁定,而从流行病学来说,寻求中间宿主是重要旁证。如果按照12月1日发病推算,至少11月中旬,这个人就被感染了。要关心的是这篇论文还有另外一个非常重要的细节:在前四位发病的病人里,有三位都跟海鲜市场没有关系。如果寻找零号病人?如何认定中间宿主是穿山甲?都还是问题。
3.3冠状病毒人-人传染的证实
2020年1月20日,国家卫健委高级别专家组组长钟南山院士根据目前的资料,可以证实新型冠状病毒肺炎存在人传人现象。如广东有2个病例是因家人去过武汉后染上了新型冠状病毒肺炎,肯定有“人传人”,有14例确诊,还表示有14名医务人员感染,是在围绕一个感染者的传播造成有医务人员感染。世界卫生组织官员也注意到新型冠状病毒有在密切接触的人-人之间传播的事实。
钟南山等在1099例患者的流行病学研究时,71.8%的患者接触过来自疫区,仅仅只有1.18%的患者有接触野生动物史, 数据证明此新型冠状病毒感染可在人际间传播[31]。表1显示人际间给出可以传播的7种冠状病毒的种属病毒名称、主要可就的部位、传播方式、导致的疾病和危险程度。

表1. 人际间可以传播的7种冠状病毒
4.抗病毒新药的研究策略
4.1 病毒感染的致病机理
病毒侵入机体是否引起发病,取决于病毒的毒力和宿主的抵抗力和免疫功能(包括特异性和非特异性免疫),二者的相互作用受外界各种因素的影响[32-37]。病毒侵入体并在靶器官细胞中增殖,与机体发生相互作用。不同的病毒由于侵犯的靶器官不同而表现出不同的临床症状。当机体免疫功能低下无力完全清除病毒时,病毒就会在感染部位生长;某些病毒基因可整合到宿主细胞的基因组中;某些病毒被免疫细胞亲嗜;某些病毒无免疫原性。
近年来基础医学和生命科学对自由基的研究在不断深入,认识到自由基已经介入到病毒感染性疾病的致病过程,对疾病的发生、发展和预后起着重要作用[38-40]。病毒可诱导宿主细胞产生氧化应激,释放大量活性氧自由基,在活性氧自由基的作用下病毒复制増强。过多的自由基作用机体会造成生物膜的脂质过氧化损伤,引起酶、氨基酸、蛋白质的氧化破坏等,从而引起患者机体和器官的损伤,甚至如肺、心、肝、肾功能衰竭而死亡。目前公布的药物防治方案中还未见推荐应用自由基清除剂的相关药物。
4.2 RNA病毒和DNA病毒
RNA病毒的遗传物质由RNA组成,由于其遗传信息保存在RNA上,复制过程通常发生在细胞质中,包括自我复制和逆转录复制两种形式。病毒RNA在复制过程中,因纠正其错误复制酶的活性较低,很容易出现病毒错误复制,导致病毒变异株的出现。
DNA病毒则是以DNA为遗传物质的病毒,大多数DNA病毒的复制过程需要在细胞核内完成。DNA病毒不多,目前已知的有乙肝病毒,天花病毒,花椰菜花叶病毒等几种。
与DNA病毒相比,RNA病毒更容易突变,致使临床致病毒株种类复杂,有效疫苗研制难度较大,同时增加了临床临床预防和治疗的难度。
4.3 初筛是低成本发现新药的基础
活性物质发现-成药性评估-临床前研究-人体临床试验-正式上市推广应用等五个环节是新药研发中的必要过程。
针对新型CoVs复制快、宿主范围广、变异高、跨物种传播快等问题,广谱抗病毒药物的开发是抗新型CoVs的重要策略。虽然SARS-CoV、MERS-CoV及2019-nCoV毒株被迅速发现及鉴定,但由于多种因素的影响,抗病毒药物的研究进展仍受到阻碍。目前SARS-CoV和MERS-CoV的动物模型并不足以支持抗病毒治疗药物研发,因此在创新药物研发和老药再开发的过程中,建立并使用有效的体内外快速筛选模型和筛选方法尤为重要。
4.4 筛选研究的生物信息学方法
4.4.1 蛋白同源建模
同源建模法是预测蛋白结构的首选方法,基于相似的氨基酸序列对应相似的蛋白质结构的原理。同源建模是虚拟筛选、分子动力学模拟、蛋白空间结构分析等方法的前提,可用于预测PDB数据库中没有蛋白晶体结构,创建蛋白模型。如望石智慧科技公司网上公布利用蛋白同源建模、计算化学虚拟筛选等技术,发现了二十余个可能对2019-nCoV病毒RNA聚合酶具有潜在的抑制作用的核苷母核分子。
4.4.2 分子对接
指两个或多个分子之间通过几何匹配和能量匹配相互识别找到最佳匹配模式的过程。分子对接计算以受体活性位点区域为基础,通过空间结构互补和能量最小化原则,搜寻配体与受体是否能产生相互作用以及它们之间的最佳结合模式。
4.4.3 分子动力学模拟
分子动力学模拟是分子模拟中最接近实验条件的模拟方法,能够从原子层面给出体系的微观演变过程,直观的展示实验现象发生的机理与规律,促使研究者向着更高效,更经济,更有预见性的方向发展的重要部分。模拟使用蛋白质的势能模型、计算机模拟力场能量重复求解蛋白质分子和溶剂分子中原子的牛顿运动方程、构象在模拟中,根据热力学定律,系统趋向于自由能最低的状态。目的在于解决如下问题:(1)比较野生型与突变体蛋白的蛋白特性;(2)配体-受体结合的机制;(3)研究蛋白与膜的作用(脂质力场);(4)蛋白折叠。
4.4.4 虚拟筛选
虚拟筛选(virtual screening)也称计算机筛选,即在进行生物活性筛选之前,利用计算机上的分子对接软件模拟目标靶点与候选药物之间的相互作用,计算两者之间的亲和力大小,以降低实际筛选化合物数目,同时提高先导化合物发现效率。虚拟筛选可以分为两类:(1)基于受体的虚拟筛选:从靶蛋白的三维结构出发,研究靶蛋白结合位点的特征性质以及它与小分子化合物之间的相互作用模式。(2)基于配体的虚拟筛选:利用已知活性的小分子化合物,根据化合物的形状相似性或药效团模型在化合物数据库中搜索能够与它匹配的化学分子结构。
4.5 开发前期的体外、体内(in vitro/in vivo)生物活性筛选研究
前人开展的针对高致病性人类冠状病毒SARS-CoV和MERS-CoV有效筛选方法有借鉴作用,但最终必须对新的CoV病毒有活性,才有可能成为有价值的候选药物,因此需要考虑以新CoV为靶点的广谱药物研发,探寻阻断病毒复制的生物学机制,掌握病毒对机体所产生的生物标志物(Biomarkers),建立具有不同作用方式或干扰病毒复制周期的药物筛选系统。
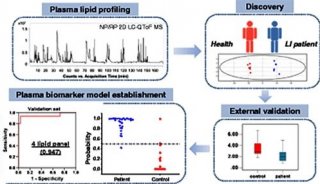
以生物信息学为基础的预测分析,虽然为进一步广谱抗CoVs药物由筛选到开发的流程奠定了基础,但信息提供的数据往往有较大的局限。图5给出抗病毒药物由筛选到开发的基本流程。只有经过这三个流程的研究,获得推荐进入开发阶段,并经风险评估后才有可能成为进入成药性研发的推荐候选药物。

图5 广谱抗病毒药物由筛选到开发的流程示意图
4.5.1体外(in vitro)生物活性
(1) 体外抗病毒活性许多感染人体的病毒可以在细胞培养系统或动物宿主体内完成完整的生命周期。研发者可以在临床试验前通过体外试验证明所研究药物和/或其代谢产物的特异性、可定量的抗病毒活性。这些数据能够预测药物在体内可接受的风险/收益比,以及发挥抗病毒作用的药物浓度,从而为人体试验提供支持。试验需要使用相关的细胞和病毒临床分离株进行的体外抗病毒活性和细胞毒性评价。
(2) 细胞毒性和治疗指数:可为临床试验制定安全的用药剂量范围提供指导。由于病毒的基因容易发生变异,应使用多种临床分离株考察所研究药物的抗病毒活性,即临床分离株应能代表临床试验中的病毒群。抗病毒活性研究包括:一是评价药物对一系列病毒实验室适应株和临床分离株(包括不同的亚群(clades)、亚型(subtypes)或基因型(genotypes))的特异性抗病毒活性。二是评价对相同作用靶点和适应症、并对其他已上市药物产生耐药的代表性病毒株的抗病毒活性。三是评价药物的抗病毒活性和细胞毒性。
4.5.2体内(in vivo)生物活性研究
参考国家有关抗病毒研究指导原则[41-43],体内研究需在体外抗病毒活性研究的基础上,通过动物感染模型评价药物的抗病毒活性。评估指标包括药物对病毒感染后发病率、死亡率、组织病理学变化、不同时间点的病毒载量的影响,同时观察抗原和抗体量的变化、以及药代动力学数据。
4.6 以成药性为核心的新药临床前评价研究
新药研究是药物创新研发的系统工程。为保证药物安全、有效、质量可控,防止各类要害事件发生,各国纷纷加强管理,并逐步制订出新药管理办法。1985年以来,国家医药管理局制定了“新药管理办法”、“新药审评办法”和“技术指导原则”。后来多次进行修订。重视各国对新药研究制定的技术指导原则利用[41-43]。
由于药物来源和临床适应症的差别,各类药物的研究内容不可能完全一致。新药临床前研究内容包括处方组成、工艺、药学、药剂学、药理、毒理学六个方面。对于具有选择性药理效应的药物,在进行临床试验前还需测定药物在动物体内的吸收,分布及消除过程。对于抗病毒药物,非临床病毒学研究有助于在进行人体试验前评价药物的有效性和安全性。
4.6. 1 药物在模型系统选择特定抗病毒活性的研究
临床上常将一种药物与其他已上市的治疗相同适应症的药物联合使用,通过体外试验研究两种或两种以上药物联合用药的抗病毒活性,考察相互作用(如拮抗、协同、增强、叠加等)。因此在抗病毒药物的研发过程中,下列研究内容非常重要:(A)测定所研究药物对相同作用靶点的其他已上市药物的耐药病毒株的抗病毒活性。(B)测定已上市药物对由相同作用靶点的所研究药物诱导的耐药病毒株的抗病毒活性。
4.6.2作用机制研究
药物作用机制是药效发挥的关键。充分掌握药物的作用机制对于临床试验的设计非常重要,为此需要了解病毒基因组中发生导致耐药性突变的可能区域,选择适当的病毒抑制靶点(如聚合酶、合成酶、突刺蛋白、壳蛋白酶)。病毒生命周期的很多阶段都可以选择潜在的作用靶点,药物通过病毒特异性的编码功能而发挥直接抗病毒作用(如酶抑制剂),或者其他途径发挥间接的抗病毒作用。主要机制研究包括:(A)药物的特异性病毒复制抑制功能。(B)确定药物作用靶点(如病毒复制酶、蛋白酶等)或作用于病毒复制的不同阶段。当宿主细胞中存在或可能存在与病毒酶类似的酶时,需要证明药物对病毒聚合酶的抑制活性,同时比较其对宿主细胞的DNA/RNA聚合酶的抑制活性。
4.6.3 病毒感染的致病机制:
一方面开展病毒对宿主细胞的致病作用研究,如细胞效应、稳定状态感染、包涵体形成、细胞凋亡、基因整合与细胞转化等。同时开展病毒感染的免疫病理学研究,包括病毒对易感组织器官的亲嗜性和损伤,抗体介导的免疫病理损伤,细胞免疫引起的损伤,炎症因子导致的病理反应,以及病毒对免疫系统的损伤作用等。
近年的研究表明,自由基可介导病毒感染性疾病的致病过程,对疾病的发生、发展和预后起着重要作用。自由基是一些具有不配对电子的分子、原子、离子或原子团,在体内具有非常强的氧化能力,从而影响机体正常物质代谢过程。当自由基的产生和清除的平衡被打破时,可造成对机体的损伤。从自由基对机体的作用来看:一是参与免疫调节,以及ATP、前列腺素的合成和巨噬细胞的吞噬作用; 二是引起机体发生癌变、诱发炎症、病理损伤及自身免疫。
4.6.4 耐药性
体外耐药病毒株的选择:病毒可因基因突变导致病毒对特定的抗病毒药物的敏感性降低而产生耐药性。在开始以感染特定病毒的患者为对象的临床试验前,先通过体外试验选择对药物耐药的病毒株,鉴定耐药株的表型和基因型,并进行交叉耐药性分析。
通过在细胞培养中选择对药物耐药的病毒株,可以了解耐药性产生遗传阈值的高低。而遗传阈值较高的药物则可能在病毒株中发生多处突变才产生耐药性。药物和目标病毒的许多因素可对耐药性产生影响,如药物浓度。突变株的出现速率取决于病毒复制速率、产生的病毒基因组的数量、复制机制的保真度以及宿主因素。对这些因素的了解有助于设计检测耐药株的体外试验。在评价耐药性的体外试验中,药物的浓度范围应覆盖其在人体内的预期浓度。选择对药物耐药的突变毒株的试验应在下列条件下重复进行:使用不同的野生株、使用不同的耐药株,并确定不同的试验中产生的耐药性突变的类型是否相同,以评价药物浓度与耐药性遗传屏障之间的关系。
基因型分析:针对体外试验中筛选出的耐药株进行基因型分析,确定可能导致病毒产生药物敏感性降低的基因突变类型。对病毒基因组中的相关部分进行RNA或DNA序列分析,鉴定耐药相关突变,有利于预测临床疗效,并且可以为阐述药物的作用机制提供证据。
表型分析:表型分析用于确定变异株对药物的敏感性是否变化。通过基因型分析鉴定出与耐药性产生可能相关的突变后,需进一步评价每一种突变导致的表型耐药能力。通过体外试验测定重组病毒对药物的敏感性,并确定EC50值。计算突变株与对照株的EC50比值,计算病毒表型的耐药变化。
交叉耐药性:使用针对相同靶点的抗病毒药物治疗时,对一种药物敏感性降低的变异,同时也可能会对相同靶点的其他药物的敏感性降低,即交叉耐药。在评价同类已上市药物对在研药物的耐药毒株的有效性时,如果药物的作用靶点相同,但结构类型不同,建议对不同类型的药物进行交叉耐药性分析。
针对耐药性产生的监测:抗病毒药物的耐药性信息可以帮助临床医生做出最佳的治疗决策,因此有必要在药物研发的各期临床试验中进行全面的耐药性监测。在某些病毒,病毒载量的变化可作为判定抗病毒药物临床疗效的终点指标,因此可以用测定病毒载量的方法进行耐药性监测。
4.6.5研究管理的突出问题
从管理角度,使用人靶细胞的原代培养细胞开展抗病毒活性研究时,由于病毒的基因容易发生变异,所以应使用多种临床分离株考察所研究药物的抗病毒活性,临床分离株应能代表临床试验中的病毒群。
实施临床前研究时必须注意以下内容:(1) 重视对药物研发机构的要求,包括人员、场地、设备、仪器和管理制度,确保所有试验数据和资料的真实性。(2) 严格按照国家食品药品监督管理局发布的相关技术指导原则开展研究。(3) 历史发展给我们留下的疫情急用药物研发指南也值得参考,如2003年国家食品药品监管局发布的《防治传染性非典型肺炎药物研究的基本技术要求》[43],有利于针对突发公共卫生事件的应急药物的研发。
参考文献:略
文献来源:刘昌孝, 伊秀林, 王玉丽, 闫凤英.认识新冠病毒(SARS-CoV-2),思考抗病毒药物研发策略[J].药物评价研究,2020,43(3):361-372.