等电点与酸碱的区别介绍
氨基酸具有氨基和羧基的典型反应,例如氨基可以羟基化、酰基化,可与亚硝酸作用;羧基以成酯或酰氯或酰胺等。此外,由于分子中同时具有氨基与羧基,还有氨基酸所特有的性质。
氨基酸分子中既含有氨基,又含有羧基,所以氨基酸与强酸强碱都能成盐,氨基酸是两性物质,本身能形成内盐。
氨基酸的高熔点(实际为分解点)、难溶于非极性有机溶剂等性质说明氨基酸在结晶状态是以两性离子存在的。
在水溶液中,氨基酸二偶极离子既可以与一个H+结合成为正离子,又可以失去一个H+成为负离子。这三种离子在水溶液中通过得到或失去互相转换同时存在,在pH值达到等电点时溶液处于平衡。
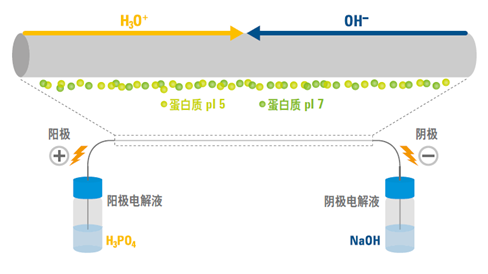
等电点不是中性点,不同氨基酸由于结构不同,等电点也不同。酸性氨基酸水溶液的等电点必然小于7,所以必须加入较多的碱才能使正负离子量相等。反之,碱性氨基酸水溶液中负离子较多,则必须加入酸,才能使正离子量增加。所以碱性氨基酸的等电点必然大于7。
各种氨基酸在其等电点时,溶解度最小,因而用调节等电点的方法,可以分离氨基酸的混合物。
氨基酸形成内盐
氨基酸的晶体是以偶极离子的形式存在。
这种偶极离子是分子内的氨基与羧基成盐的结果,故又叫内盐。
核酸的等电点比较低。如DNA的等电点为4~4.5,RNA的等电点为2~2.5。
等电点
在氨基酸溶液中存在如下平衡,在一定的pH值溶液中,正离子和负离子数量相等且浓度都很低,而偶极浓度最高,此时电解以偶极离子形式存在,氨基酸不移动。这时溶液的pH值便是该氨基酸的等电点。