大满贯!2019年施一公团队连续发表Cell,Nature,Science文章
2015年,通过单粒子冷冻电子显微镜(cryo-EM)分析确定剪接体的第一个近原子分辨率结构,报道了来自S. pombe的ILS复合物。从那时起,已经阐明了13种冷冻-EM结构,大部分分辨率在3.3和5.8之间,已经阐明了来自酿酒酵母的组装剪接体的七种不同状态,人类剪接体的7种不同状态的11种这样的结构。在剪接体的八种已知功能状态中,仅B *复合物在结构上保持未表征。
2019年3月14日,施一公研究组在Cell在线发表题为“Structures of the Catalytically Activated Yeast Spliceosome Reveal the Mechanism of Branching”的研究论文,该研究得到了酿酒酵母的两种不同前mRNA上组装了B *复合物,并确定了四种不同B *复合物的冷冻EM结构,总分辨率为2.9-3.8Å。
U2核小RNA(snRNA)和分支点序列(BPS)之间的双链离散地远离5个B *复合物中的5'-剪接位点(5'SS),其缺乏步骤I剪接因子Yju2和Cwc25。 将Yju2募集到活性位点使U2 / BPS双链体进入5'SS附近,BPS亲核试剂位于距催化金属M24Å处。 该分析揭示了Yju2和Cwc25在分支中的功能机制。 不同前mRNA上的这些结构揭示了在主要功能状态下剪接体的底物特异性构象。 这些构象状态的比较揭示了对支化反应的机理见解。
2019年1月11日,清华大学施一公团队在Science在线发表题为“Recognition of the amyloid precursor protein by human γ-secretase”的研究论文,该论文报告了人类γ-分泌酶与跨膜APP片段的复合物的冷冻电子显微镜(cryo-EM)结构,分辨率达到2.6Å。 APP的跨膜螺旋(TM)与PS1的五个周围TM(γ-分泌酶的催化亚基)紧密相互作用。 该结构与结合Notch的γ-分泌酶的结构一起揭示了底物结合的对比特征,其可用于设计底物特异性抑制剂。因此,该结构用作发现γ-分泌酶的底物特异性抑制剂和理解γ-分泌酶的生物学功能以及AD的疾病机制的重要框架。

2019年1月1日,施一公研究组在Nature在线发表题为“Structural basis of Notch recognition by human γ-secretase”的研究论文,该论文报告人类γ-分泌酶与Notch片段的复合物的冷冻电子显微镜结构,分辨率为2.7Å。 Notch的跨膜螺旋被PS1的三个跨膜结构域包围,并且Notch片段的羧基末端β-链形成β-折叠,其在细胞内侧具有两个底物诱导的PS1的β-链。 杂合β-折叠的形成对于底物裂解是必需的,其发生在Notch跨膜螺旋的羧基末端。 PS1在底物结合后经历明显的构象重排。 这些特征揭示了Notch识别的结构基础,并且对γ-分泌酶对淀粉样蛋白前体蛋白的募集具有意义。
在1977年,Phillip Sharp和Richard Roberts俩个研究组独立发现了剪切这一过程,紧接着,1979年, Steitz研究组发现五种称为U1,U2,U4,U5和U6 snRNA的富含尿苷的小核RNA(snRNA)和7种12-35kDa的蛋白质(snRNPs)。之后, Steitz等研究组发现U1 snRNA的5'末端序列被识别为与5'剪接位点(5'SS)互补,并且snRNP被部分纯化。纯化的U1snRNP在体外特异性结合到5'SS上,并且U1snRNP的消耗抑制了体外剪接。随后,证实了多个snRNPs参与前mRNA剪接。

施一公
剪接测定的发展使得剪切反应的描绘成为可能。 发现ATP和镁(Mg2 +)对于腺病毒前体mRNA的体外剪接是必不可少的。 通过分支点序列(BPS)中的腺苷核苷酸和5'SS的5'末端的鸟嘌呤核苷酸之间的连接形成内含子套索结构,得到了生物化学证实。
前体mRNA剪接是由剪接体催化的,剪接体是一种高度动态和复杂的分子机器,它含有前体mRNA,U1,U2,U4 / U6和U5 snRNPs以及许多非snRNP蛋白。 U1和U2 snRNP分别与内含子的5'剪接位点(ss)和分支位点(BS)相互作用,同时为U4 / U6.U5 tri-snRNP的稳定整合铺平了道路,产生了剪接体B复合物。然而,尽管tri-snRNP引入了必需的催化组分,但是剪接体B复合物仍然需要转化成催化活性复合物,这一过程需要广泛的结构重排。通过解开U4 snRNA的U4 / U6双链体(通过RNA解旋酶Brr2)启动活化, U6随后与U2(U2 / U6螺旋Ia和螺旋Ib)以及内部茎环(U6 ISL)自由地形成短双链体。最终在剪接体激活期间建立的催化RNA-RNA网络与II组自我剪接内含子的催化核心非常相似。
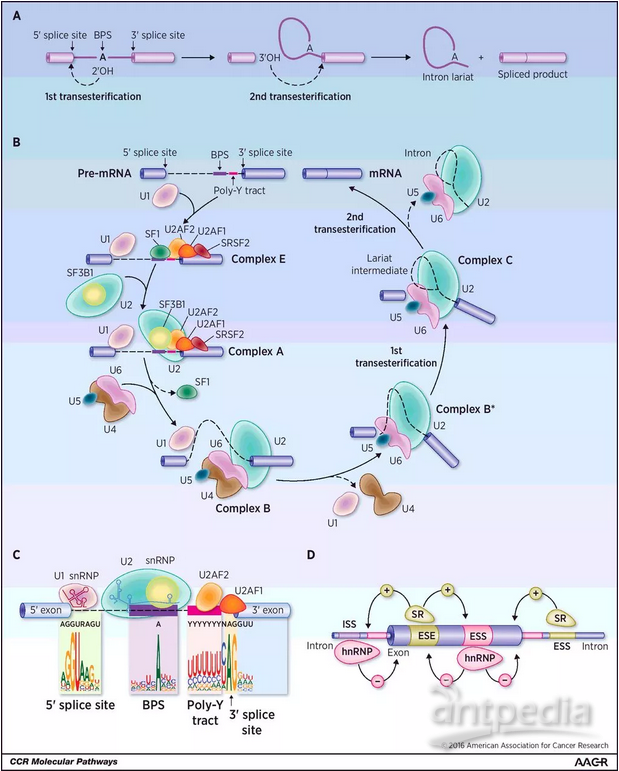
剪切过程
随后通过RNA解旋酶PRP2将所得的活化的但是预催化的B(Bact)复合物转化为催化剪接体(命名为B *)。在人类中,B-to-B *转换也需要AQR RNA解旋酶的ATP酶活性,这在酵母酿酒酵母的剪接体中是不存在的。这表明人类剪接体中催化活化所需的构象重排比酵母中的那些更复杂。 B *复合物催化剪切的第一步,产生切割的5'外显子和内含子3'外显子套索中间体,产生剪接体C复合物。额外的RNP重排将C复合物转化为C *复合物,然后催化第二步剪接,并且5'和3'外显子的连接形成mRNA并释放内含子作为套索。
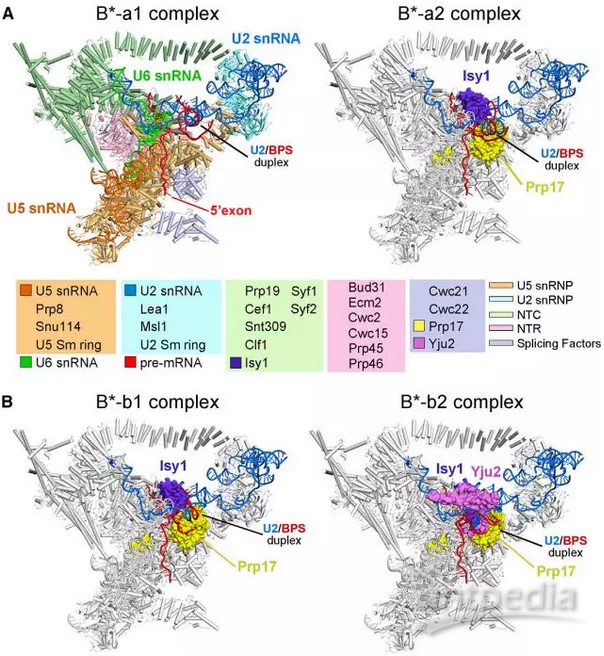
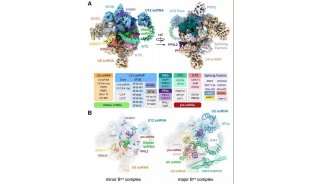
来自酿酒酵母的催化活化的剪接体(B *复合物)的冷冻电子显微镜结构
2015年,通过单粒子冷冻电子显微镜(cryo-EM)分析确定剪接体的第一个近原子分辨率结构,报道了来自S. pombe的ILS复合物。从那时起,已经阐明了13种冷冻-EM结构,大部分分辨率在3.3和5.8之间,已经阐明了来自酿酒酵母的组装剪接体的七种不同状态,人类剪接体的7种不同状态的11种这样的结构。在剪接体的八种已知功能状态中,仅B *复合物在结构上保持未表征。
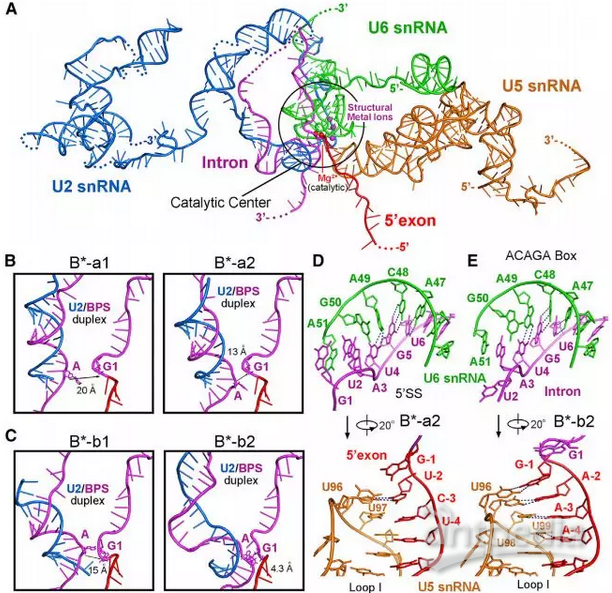
酿酒酵母B *复合物中的RNA元件
在这项研究中,研究人员报告了来自酿酒酵母的B *复合物的冷冻-EM结构。该研究得到了酿酒酵母的两种不同前mRNA上组装了B *复合物,并确定了四种不同B *复合物的冷冻EM结构,总分辨率为2.9-3.8Å。 U2核小RNA(snRNA)和分支点序列(BPS)之间的双链离散地远离5个B *复合物中的5'-剪接位点(5'SS),其缺乏步骤I剪接因子Yju2和Cwc25。 将Yju2募集到活性位点使U2 / BPS双链体进入5'SS附近,BPS亲核试剂位于距催化金属M24Å处。
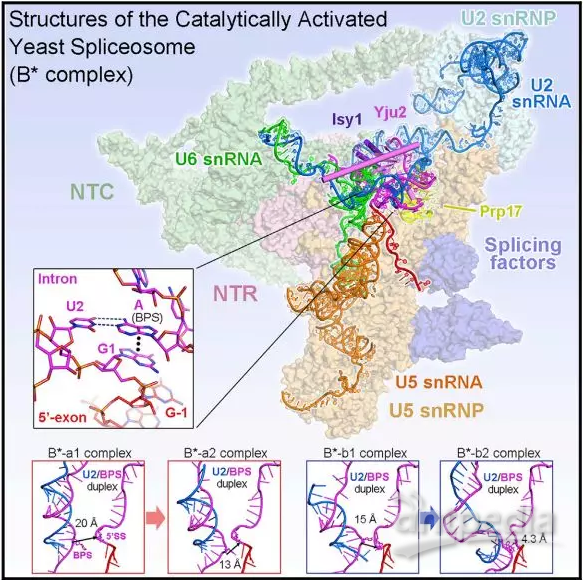
结构总结
该分析揭示了Yju2和Cwc25在分支中的功能机制。 不同前mRNA上的这些结构揭示了在主要功能状态下剪接体的底物特异性构象。这些构象状态的比较揭示了对支化反应的机理见解。
-
项目成果

-
焦点事件

-
焦点事件
-
精英视角

-
焦点事件

-
焦点事件
-
焦点事件

-
焦点事件
-
焦点事件





















