张锋Cell:新一代CRISPR基因组编辑系统
在发表于《细胞》(Cell)杂志上的一项研究中,哈佛-麻省理工Broad研究的张锋(Feng Zhang)及其同事们报告称发现了一种不同的CRISPR系统,其有潜力实现更简单、更精确的基因组工程操作。他们描述了这一新系统一些出乎意外的生物学特征,证实可以操控它来编辑人类细胞基因组。
人类基因组计划的主要领导者之一、Broad研究所所长Eric Lander说:“这一系统有着巨大的潜力推动遗传工程。这篇论文不仅揭示了从前未知的一种CRISPR系统的功能,还证实了可以利用Cpf1完成人类基因组编辑,其具有一些非凡和强大的特性。这一Cpf1系统代表了新一代的基因编辑技术。”
CRISPR序列是在1987年第一次被描述出来,在2010年和2011年它们的自然生物学功能初步被确定。2013年张锋及哈佛医学院的George Church各自第一次报道了,将CRISPR-Cas9系统应用于哺乳动物基因组编辑。
在这篇新文章中,张锋和合作者们在不同类型的细菌中搜寻了成百上千种的CRISPR系统,寻找具有一些有用的特性,可改造用于人类细胞的酶。来自氨基酸球菌属(Acidaminococcus)和毛螺菌科(Lachnospiraceae)的Cpf1酶成为了两个有前景的候选物,张锋和同事们随后证实了其可以靶向人类细胞的基因组位点。
张锋说:“发现了可以利用来推动研究和人类健康的、完全不同的CRISPR酶,我们感到激动万分。”
这一新发现的Cpf1系统有几个重要的方面不同于以往描述的Cas9,对于研究和治疗及商业和知识产权均具有重要的意义:
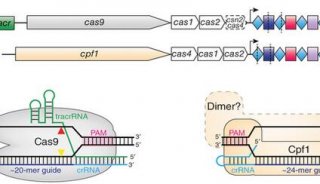
首先:在它的自然形态下,DNA切割酶Cas9与两条小RNAs形成了一种复合物,两条RNAs均是获得切割活性的必要条件。Cpf1系统更简单一些,它只需要一条RNA。Cpf1酶也比标准SpCas9要小,使得它更易于传送至细胞和组织内。
第二:且有可能最重要的是,Cpf1以一种不同于Cas9的方式切割DNA。当Cas9复合物切割DNA时,它切割的是同一位点的两条链,留下的“平端”(blunt ends)在重新连接时往往会发生突变。采用Cpf1复合物生成的两条链切口是偏移的,在裸露端留下了短悬端(overhang)。这预计有助于精确插入,使得研究人员能够更有效及精确地整合一段DNA。
第三:Cpf1切口远离识别位点,这意味着即便在切割位点靶基因突变,仍然可以进行再度切割,提供了多次机会来校正编辑。
第四:Cpf1系统为选择靶位点提供了新的灵活性。像Cas9一样,Cpf1复合物必须首选附着PAM,短序列,选择的靶点靠近自然存在的PAM序列。Cpf1系统识别的PAM序列与Cas9截然不同。这在靶向某些基因组如疟原虫及人类基因组时可能是个优势。
Broad研究所成员Levi Garraway(未参与该研究)说:“Cpf1这些意外的特性及更精确的编辑为各种应用,包括癌症研究打开了大门。”
张锋、Broad研究所和麻省理工学院打算广泛分享这一Cpf1系统。与较早期的Cas9工具一样,这些研究团体将通过张锋实验室质粒共享网站Addgene,免费提供这一技术用于学术研究。通过Addgene张锋实验室已与全球各地的研究者共享Cas9试剂达23,000多次以推动加速研究。张锋实验室还提供了免费的在线工具和资源,研究人员可通过网站http://www.genome-engineering.org获取。
Broad研究所和麻省理工学院计划提供非专属授权推动工具商业化,使得服务提供商能够将这种酶添加到他们的CRISPR管道和服务中,进一步确保提供这种新酶用于研究中。这些研究团体还计划提供授权,以最好地支持快速及安全地开发合适及重要的临床应用。张锋说:“我们正致力实现可广泛获取CRISPR-Cpf1技术。”
“我们的目标是开发出一些可以加速研究,最终促成一些新治疗应用的工具,我们看到将来会有更多,甚至超越Cpf1和Cas9的成果,或许可以改变其他一些酶的用途来进一步推动基因组编辑。”
-
项目成果

-
项目成果

-
企业风采

-
焦点事件

-
焦点事件

-
科技前沿