HPLC对花生中黄曲霉毒素的测定
方案优势
灵敏、准确和实用
采用标准
相关标准
方法/原理/步骤
目前,常用的黄曲霉毒素检测方法主要有薄层色谱法(TLC)、酶联免疫吸附法(ELISA)和碘化荧光光度法(SFB)。由于上述方法都有操作繁琐、实验过程长、精确度低以及直接接触毒素等缺点,并且由于非常重要的黄曲霉毒素B1和G1的低荧光性,只有黄曲霉毒素B2和G2有其自己的荧光,那么,黄曲霉毒素B1和G1就不得不通过衍生来检测。通过光化学反应(如下图),黄曲霉毒素B1和G1被羟基化(水解)从而得到稳定的可测荧光。
如果通过加入碘的甲醇衍生剂,通过质谱测得,碘和甲氧基分别加成到了黄曲霉毒素B1和G1双键两侧,反应形式类似于上述光化学反应,那些其他重要的用于检测的黄曲霉毒素B2和G2的化学性质在光化学反应中并不改变,并且B2a和G2a有着区别于B2和G2的荧光强度。
所以食品及饲料越来越多地采用高效液相色谱柱后衍生法来检测黄曲霉毒素,一个样品只需5 min,就能达到定量准确、快速检测的要求。柱后衍生荧光检测具有选择性强、灵敏度高、重现性好等优点。
检测过程
提取:样品全部磨碎,通过40目筛,混匀,称取试样25.0g(精确到0.1g)于500mL烧杯中,加入5g氯化钠及125mL甲醇水溶液(体积比3:2),用均质器高速搅拌3min,过滤。移取20mL滤液到50mL量筒中,并加入20mL水稀释,搅匀,以玻璃纤维滤纸过滤1-2次,至滤液澄清,随即进行免疫亲和柱(高度富集和纯化)净化操作。
净化:将免疫亲和柱连接于10mL玻璃针筒下,准确移取8mL上述澄清液,注人玻璃针筒内,以1-2滴/s的流速全部通过免疫亲和柱。再用10mL水以同样的流速淋洗柱子两次,弃去全部流出液。再用1.0mL甲醇淋洗亲和柱,洗脱流速为1-2滴/s,将所有样品淋洗液(1mL)及1.0mL水收集于2mL玻璃测试瓶中,待测。
色谱条件
色谱柱:SMT C18,250mm×4.6mm×5μm
色谱柱温度:室温
流动相:甲醇-乙腈-水溶液(22+22+56);
流速:1.0mL/min;
柱后衍生试剂:0.03%的碘溶液
流速:0.3 mL/min
衍生化温度:70℃
荧光检测器:激发波长360 nm,发射波长450 nm;
进样量:20μL
黄曲霉毒素样品进样液相色谱检测,所得图谱如下图
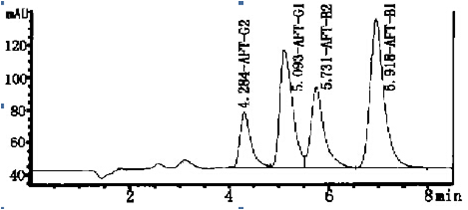
回收率:≥90%
精密度(RSD):1%~2%
线性范围:0.1-50μg/kg
相关系数:≥0.9950
最低检出限:0.1mg/kg
低于国家限量规定
仪器设备
兰博series 4060高效液相色谱







