如何有效应对新冠病毒变异?科学家研发出纳米体新法
一波未平,一波又起,人类对抗新冠病毒真是一场持久战。新冠病毒变异?原来的疫苗是否还有效?能否让疫苗应对变异的病毒?近来,哥廷根的一组研究团队为了应对目前严峻的形势,研制出了一种微型抗体,或有望应对多种变异病毒。
最近,哥廷根的研究人员研发出了一种微型抗体,能有效阻止可怕的新冠病毒及其对人类威胁极大的新变种病毒入侵。这些微型抗体,也被称作纳米体,在结合以及中和病毒的能力方面比之前研发出来的微型抗体要强1000倍。此外,他们新研发的这种微型抗体具有较高的稳定性和对极端高温的抵抗力。这种独特的组合使它们成为非常有希望能治疗新冠患者的药物。由于纳米体可以以低成本且大批量地生产,它可以满足全球对新冠治疗药物的需求。目前,这种新的微型抗体正在准备进行下一步的临床试验。
抗体可以帮助我们的免疫系统抵御病原体。例如,这些构成抗体的分子附着在病毒上然后并中它们,这样病毒分子就会变成另一种和原来的构成不同的分子从而失去原本的毒性,这样,人们就不会被这种病毒感染了。抗体也可以用于工业化生产,也可以用来治疗急性疾病患者。然后它们就像药物一样,帮助人们缓解症状、在更短的时间内康复。这是治疗乙型肝炎和狂犬病的既定做法。此外,抗体也被用于治疗新冠患者。然而,如果按照工业规模来生产这些分子,它就会变得过于复杂和昂贵,从而无法满足全球需求。在这种情势下,微型抗体可以解决这个问题。这项发现被发表在《The EMBO Journal》杂志的一篇题目为“Neutralization of SARS-CoV-2 by highly potent, hyperthermostable, and mutation-tolerant nanobodies”的文章中:
位于哥廷根(德国)的马克斯·普朗克生物物理化学研究所和哥廷根大学医学中心的科学家们现在已经研发出了微型抗体(也称为VHH抗体),这种抗体将一种有效治疗新冠病毒药物所需的所有特性结合了起来。马克斯·普朗克生物物理化学研究所主任Dirk Görlich强调说:“它们首次将两种很关键的优点融合,一种是极端的稳定性,另一种是对病毒及其阿尔法、贝塔、伽马和德尔塔突变体的出色的疗效。”
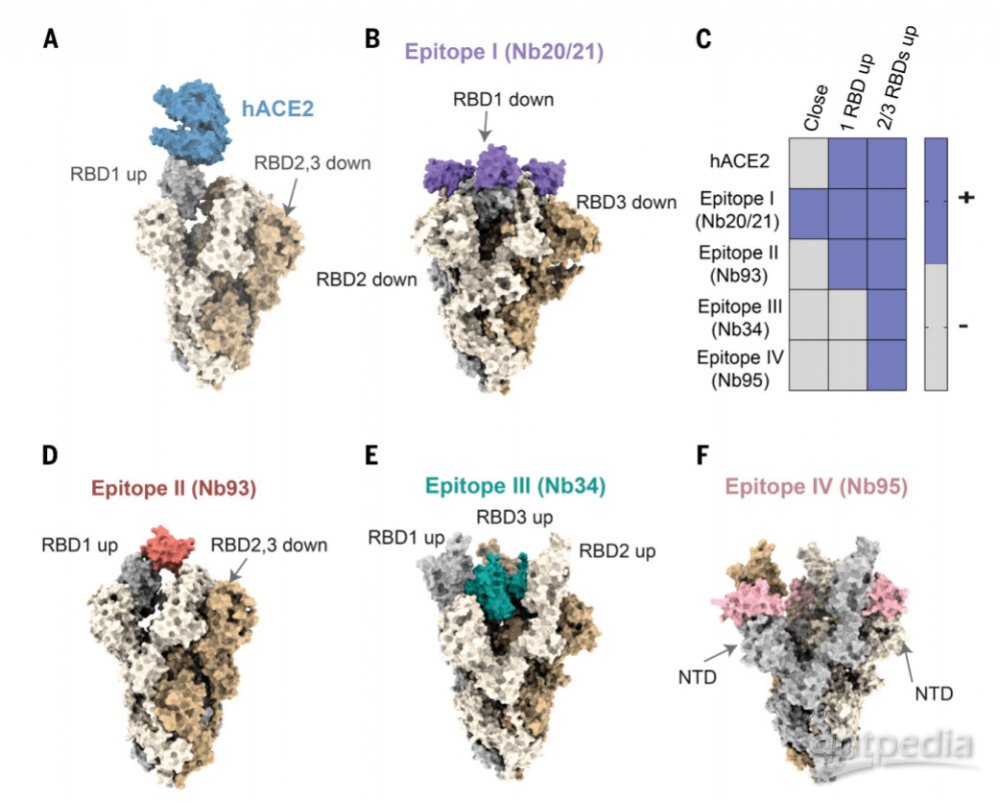
乍一看,这种新研发出来的微型抗体与其它实验室研发的抗新冠病毒纳米体没有什么不同。它们都是针对冠状病毒尖峰的关键部分,即病毒部署用于入侵宿主细胞的受体结合域。微型抗体在这发挥的作用就是阻断了这个结合域,从而阻止了宿主细胞感染病毒。
哥廷根大学医学中心分子肿瘤学研究所教授兼主任Matthias Dobbelstein解释说:“我们的微型抗体除了上述优点之外,还有另一个优势,那就是它很耐高温,可以承受高达95°C的温度,并且不会失去它的功能,也不会形成聚集物。一方面,这告诉我们,这种纳米体可能会在体内保持足够长的活跃时间,从而发挥了很大作用;另一方面,耐热纳米体在生产、加工和存储中更加便利。”
单、双、三重微型抗体
哥廷根研发的最简单的微型抗体与刺突蛋白的结合强度是之前报道的纳米体的1000倍。它们也能很好地结合突变的受体结合域的阿尔法、贝塔、伽马和德尔塔菌株。Dobbelstein说:“我们的单一微型抗体可能适合吸入,因此可以在呼吸道中直接中和病毒。此外,因为这种纳米体非常小,它们可以很容易地穿透组织,最终防止病毒在感染部位进一步传播。”
“微型抗体三联体”进一步改善了这种结合方式:研究人员根据刺突蛋白的对称性捆绑了三个相同的纳米体,刺突蛋白由三个具有三个结合域的相同构建块组成。Görlich团队的科学家Thomas Güttler报告说:“有了微型抗体三联体,我们就真的融合了它的力量:在理想的情况下,三个微型抗体中的每一个都能连接到三个结合域中的一个。”这实际上形成了一种不可逆转的纽带。三重纳米体不会释放刺突蛋白,甚至能比单一的微型抗体更好地中和病毒,达到3万倍。另一个优点是:更大尺寸的微型抗体可以延迟肾脏的排泄。这使它们在体内停留的时间更长,有望产生更持久的治疗效果。
作为第三种设计,科学家们制造了一种串联的模式。它们结合了两个针对受体结合区域不同部分的微型抗体,并结合了刺突蛋白。Görlich团队的研究人员Metin Aksu解释说:“这种串联基因对病毒突变和由此产生的‘免疫逃逸’具有极强的抵抗力,因为它们与病毒尖峰结合得特别紧密。”
研究人员发现,对于所有的微型抗体变体(单体、两倍或三倍),非常小的量就足以阻止病原体。如果把它作为一种药物使用,这将会只需要比较低的剂量,从而有助于减少它产生的副作用,也有助于降低生产成本。
羊驼为我们的研究提供了微型抗体的蓝图
Görlich说:“我们的来源于羊驼,这种微型抗体会比传统抗体更小、更简单。”为了产生对抗新冠病毒的微型抗体,研究人员用冠状病毒刺突蛋白的部分免疫了三只羊驼——马克斯·普朗克生物物理化学研究所I的生物物理化学研究中的羊驼Britta、Nora和Xenia。然后这些母马产生了抗体,科学家们从这些动物身上提取了一小份血液样本。对于羊驼来说,接下来的所有步骤都是在酶、细菌、所谓的噬菌体和酵母的帮助下完成的。Görlich解释说:“我们对动物的总体负担非常低,与人类的疫苗接种和血液检测相当。”
Görlich的团队从羊驼的血液中提取了大约10亿份微型抗体。接下来进行的是经过多年研究完善出的实验室程序:生化学家用噬菌体从最初的大量候选微型抗体中选择最好的种类。然后测试它们对抵抗新冠病毒的有效性,并在连续几轮优化中进一步改进。
并不是每一种抗体都具有“中和作用”。因此,Dobbelstein小组的研究人员确定了纳米体到底在多大程度上阻止了病毒在实验室培养的细胞中复制。Dobbelstein团队的Antje Dickmanns解释说:“通过测试广泛的纳米体稀释度,我们找到了达到这种效果的量。”她的同事Kim Stegmann补充道:“一些微型抗体的功效确实让我们惊奇,给我们留下了深刻的印象。每升培养基中不到百万分之一克就足以帮助人们完全防止感染。就微型抗体三元组而言,即使再稀释20倍也足够了。”
对目前的冠状病毒变种也有效
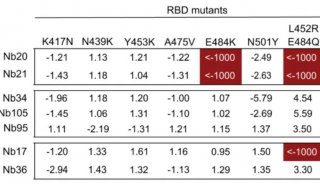
在新冠病毒大流行的过程中,新的病毒出现了变异,这些变异病毒迅速发展为主导,越来越恶劣地威胁着人们的生命和健康。这些变异通常比首次出现在武汉的菌株更具传染性。他们的突变刺突蛋白也可以“逃脱”一些原本有效的抗体的中和,这些抗体包括:感染者,康复者或接种过新冠疫苗的人者。这使得已经训练有素的免疫系统更难消除病毒。这个问题也阻碍了以前研发的治疗性抗体和微型抗体发挥作用。
我们新研发的这项新微型抗体技术是攻破了这种局限,因为它们也能有效对抗冠状病毒变体。研究人员给他们的羊驼接种了新冠病毒的刺突蛋白的一部分,但值得注意的是,动物的免疫系统也产生了针对不同病毒变体的抗体。“如果我们的微型抗体被证明对未来的变种病毒没有任何的抵御效果,我们可以对羊驼进行再免疫。Güttler自信地断言:“它们已经接种了这种病毒疫苗,所以它们会很快产生针对这种新变种的抗体。”
治疗应用前景
哥廷根团队目前正在为微型抗体的治疗实践做充足的准备。Dobbelstein强调说:“我们希望尽快通过某种手段验证纳米体作为一种药物在使用时是安全的,以便它们能够造福于新冠重症患者和那些还没有接种疫苗或自身不能构建有效免疫力的人。”该团队由技术转移专家支持,包括:马克斯·普朗克生物物理化学研究所的Dieter Link、德国多特蒙德首席研究中心的Johannes Bange和肯普基金会的Holm Keller。
据悉,新冠病毒的受体结合域是蛋白质疫苗的一个优良的候选区域,但迄今为止很难进行经济地大规模生产,并以激活免疫系统对抗病毒的形式生产。相应的细菌程序会产生错误的折叠材料。哥廷根的研究人员找到了解决这个问题的方法:他们确定了一种特殊的纳微型抗体米体,可以在不阻碍受体结合域的关键和部分的情况下,加强细菌细胞的正确折叠。这可能使疫苗廉价生产,从而能够更迅速地适应新的病毒变种,甚至可以在基础设施很少的国家通过简单的物流分发。微型抗体有助于蛋白质折叠这一事实以前并不为人所知,这对于研究和制药应用来说有着重大的意义!
虽然这项发现目前还没有被应用到实践中,但是相信通过科研人员的努力和后续的研究,这种微型抗体最终会被制成疫苗,为世界带来和平!
参考资料:
Highly potent, stable nanobodies stop SARS-CoV-2 (medicalxpress.com)
关于纳米体对抗变异病毒,此前美国匹兹堡大学的Yi Shi(时毅)团队与 2020年11月5日在 Science中发表了“Versatile and multivalent nanobodies efficiently neutralize SARS-CoV-2”,同样介绍了该种纳米体。
团队使用骆驼免疫和蛋白质组学技术鉴定了大量对SARS-CoV-2 spike (S)蛋白受体结合结构域(RBD)具有很强中和作用的纳米抗体(Nbs)。作者发现Nbs具有皮摩尔到飞摩尔的亲和力,可在亚ng/ml浓度下抑制病毒感染,并确定了与RBD最有效复合物之一的结构。结构蛋白质组学和综合建模揭示了多个不同和不重叠的表位,并指出了一系列潜在的中和机制。最终构建了具有超高中和能力(IC50低至0.058 ng/ml)并可能阻止突变逃逸的 多价Nb结构体。这些耐高温的Nbs可以从微生物中快速批量生产,并能抵抗冻干和气溶胶作用。
Nbs中和SARS-CoV-2的潜在机制
在作者的研究中,体内抗体亲和力的成熟以及随后的蛋白质组学技术使人们迅速发现了多种高亲和力的RBDNb,包括具有亚皮摩尔亲和力的超强中和剂,这对于天然的单域抗体片段而言是罕见的。该研究证明了 Nb生物工程技术的简单性和多功能性以及单体Nbs及其多价形式的理想理化特性。多价构建体代表了迄今为止最有效的SARS-CoV-2中和剂。灵活有效的给药方式(如吸入)可进一步提高其抗病毒功效,同时将剂量,成本和对临床应用的潜在毒性降至最低。Nbs与人IgG之间的高度序列相似性可能会限制免疫原性。可以将抗病毒Nbs与高度稳定的白蛋白Nb构建体融合,以改善药代动力学,这些高质量的Nb也可以用作快速,经济的即时诊断服务。 Nb技术将有助于遏制当前的大流行以及未来的大流行。
-
科技前沿
-
科技前沿