2020药典三部--生物制品生产检定用菌毒种管理及质量控制
一、总则
1. 本通则所称之菌毒种,系指直接用于制造和检定生物制品的细菌、真菌、支原体、放线菌、衣原体、立克次体或病毒等,包括各种经过基因工程修饰的菌毒种,以下简称菌毒种。菌毒种以中国《人间传染的病原微生物名录》为基础,结合生物制品生产和检定用菌毒种的特殊性分类。
2. 生产和检定用菌毒种,来源途径应合法,并经国家药品监督管理部门批准。
3. 生物制品生产用菌毒种应采用种子批系统,并应尽量减少传代次数,以降低发生遗传变异的风险。原始种子应验明其历史、来源(包括重组工程菌毒种的构建过程)和生物学特性。从原始种子传代和扩增后保存的为主种子批。从主种子批传代和扩增后保存的为工作种子批,工作种子批用于生产产品。工作种子批的生物学特性应与原始种子一致,每批主种子批和工作种子批均应按各论要求保管、检定和使用。由主种子批或工作种子批移出使用的菌毒种无论开瓶与否,均不得再返回贮存。生产过程中应规定各级种子批允许传代的代次,并经国家药品监督管理部门批准。
4. 菌毒种的传代及检定实验室应符合国家生物安全的相关规定。
5. 各生产单位对本单位的菌毒种施行统一管理。
6. 治疗性产品可参照相关要求执行。
二、菌毒种登记程序
1. 由国家菌毒种保藏机构统一编号的菌毒种,使用单位不得更改及仿冒。
2. 保管菌毒种应有严格的登记制度,建立详细的总账及分类账和档案。收到菌毒种后应立即进行编号登记,详细记录菌毒种的学名、株名、历史、来源、特性、用途、批号、传代冻干冻存日期和数量。在保管过程中,凡传代、冻干冻存及分发,记录均应清晰,可追溯,并定期核对库存数量。
3. 收到菌毒种后一般应及时进行检定。用培养基保存的菌种应立即检定。
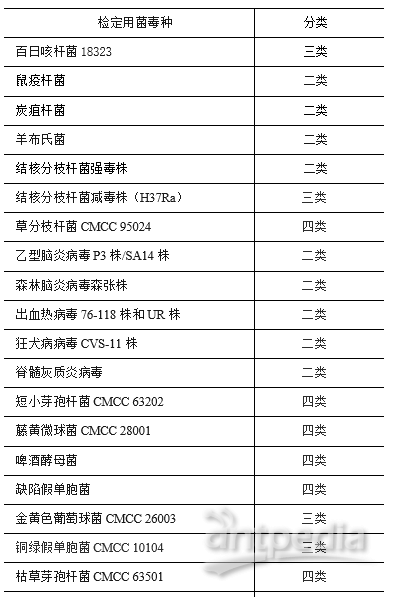
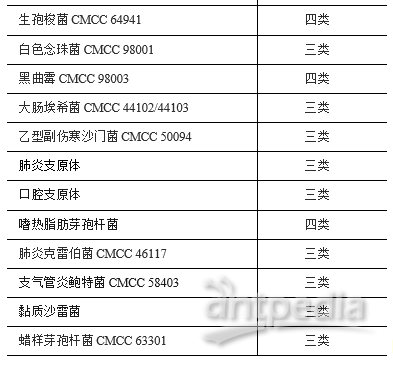
三、生物制品生产检定用菌毒种生物安全分类(见本通则附录)
以《人间传染的病原微生物名录》为基础,根据病原微生物的传染性、感染后对个体或者群体的危害程度,将生物制品生产检定用菌毒种分为四类。
1. 第一类病原微生物,是指能够引起人类或者动物非常严重疾病的微生物,以及中国尚未发现或者已经宣布消灭的微生物。
2. 第二类病原微生物,是指能够引起人类或者动物严重疾病,比较容易直接或者间接在人与人、动物与人、动物与动物间传播的微生物。
3. 第三类病原微生物,是指能够引起人类或者动物疾病,但一般情况下对人、动物或者环境不构成严重危害,传播风险有限,实验室感染后很少引起严重疾病,并且具备有效治疗和预防措施的微生物。
4. 第四类病原微生物,是指在通常情况下不会引起人类或者动物疾病的微生物。
四、菌毒种的检定
1. 生产用菌毒种应进行生物学特性、生化特性、血清学试验和分子遗传特性等的检定。生产用菌毒种的检定应符合各论要求。建立生产用菌毒种种子批全基因序列的背景资料,生产用菌毒种主种子批应进行全基因序列测定。应对生产用菌毒种已知的主要抗原表位的遗传稳定性进行检测,并证明在规定的使用代次内其遗传性状是稳定的。减毒活疫苗所含病毒或细菌的遗传性状应与主种子批一致。
细菌性疫苗生产用菌种主种子批检定
生产用菌种的种、属、型分类鉴定,包括形态、生长代谢特性和遗传特性。活菌制剂还应进行抗生素敏感性测定。细菌性疫苗生产用菌种主种子批检定一般应包括培养特性、革兰氏等染色方法镜检、生化反应、血清学试验、毒力试验、免疫效价测定、培养物纯度、活菌数测定、16S rRNA序列测定、全基因序列测定等项目。
病毒性疫苗生产用毒种主种子批检定
一般应包括鉴别试验、病毒滴度、外源污染因子检查(无菌、分枝杆菌、支原体、外源病毒因子检查),主要功能基因和遗传标志物测定,免疫原性检查,动物神经毒力试验,动物组织致病力或感染试验,全基因序列测定等项目。
重组工程菌生产用菌种主种子批检定
一般应包括培养特性、菌落形态大小、革兰氏等染色方法镜检、对抗生素的抗性、生化反应、培养物纯度、全基因序列测定、目的产物表达量、透射电镜检查、目的基因序列测定、外源基因与宿主基因的检定、外源基因整合于宿主染色体的检定、外源基因拷贝数检定、整合基因稳定性试验、目标产物的鉴别、质粒的酶切图谱等项目。
重组工程毒种生产用主种子批检定
一般应包括全基因序列测定,目的基因序列测定,病毒滴度检测,目的蛋白表达量,细菌、真菌、分枝杆菌、支原体、内外源病毒因子检查等项目。
2. 检定用菌毒种是生物制品质量控制的关键因素之一,应确保其生物学特性稳定,并且适用于检定要求。
五、菌毒种的保存
1. 菌毒种经检定后,应根据其特性,选用冻干、液氮、≤-60℃冻存或其他适当方法及时保存。
2. 不能冻干、液氮、≤-60℃冻存的菌毒种,应根据其特性,置适宜环境至少保存2份或保存于两种培养基。
3. 保存的菌毒种传代、冻干、液氮、≤-60℃冻存均应填写专用记录。
4. 保存的菌毒种应贴有牢固的标签,标明菌毒种编号、名称、代次、批号和制备日期等内容。
5. 非生产用菌毒种应与生产用菌毒种严格分开存放。工作种子批与主种子批应分别存放。每批种子批应有备份,并应在不同地方保存。
六、菌毒种的销毁
无保存价值的菌毒种可以销毁。销毁一、二类菌毒种的原始种子、主种子批和工作种子批时,须经本单位领导批准,并报请国家卫生行政主管部门或省、自治区、直辖市卫生行政主管部门认可。销毁三、四类菌毒种须经单位领导批准。销毁后应在账上注销,作岀专项记录,写明销毁原因、方式和日期。
七、菌毒种的索取、分发与运输
应符合中国《病原微生物实验室生物安全管理条例》等国家相关管理规定。
附录 常用生物制品生产检定用菌毒种生物安全分类
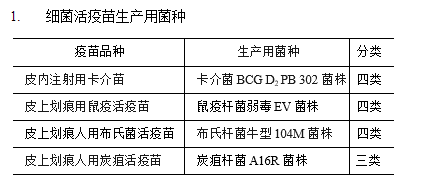

1. 细菌活疫苗生产用菌种
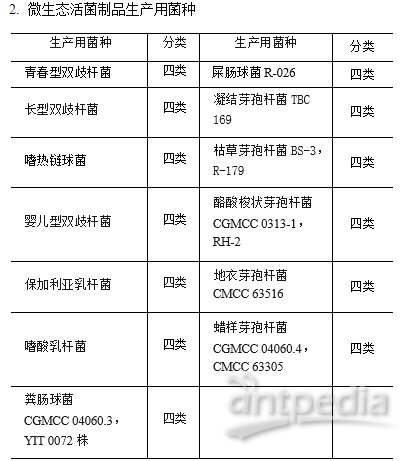
2. 微生态活菌制品生产用菌种
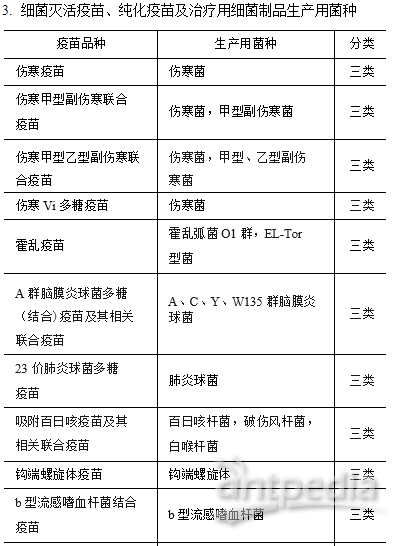
3. 细菌灭活疫苗、纯化疫苗及治疗用细菌制品生产用菌种
4. 体内诊断制品生产用菌种
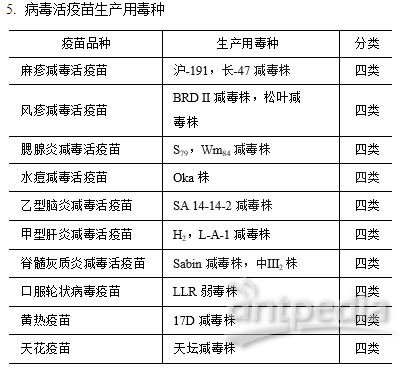
5. 病毒活疫苗生产用毒种
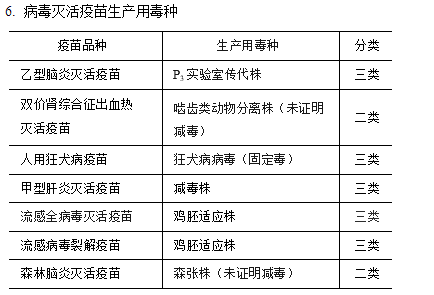
7. 重组产品:重组产品生产用工程菌株的生物安全按第四类管理。
8. 其他产品:基因治疗等以病毒为载体的生物技术制品参考相应病毒分类进行管理。
9. 生物制品检定用菌毒种