MS明星免疫组合Opdivo+Yervoy联合有限疗程化疗方案进入审查
百时美施贵宝(BMS)近日宣布,美国食品和药物管理局(FDA)已受理其提交的一份补充生物制品许可申请(sBLA):将抗PD-1疗法Opdivo(欧狄沃,通用名:nivolumab,纳武单抗)联合Yervoy(ipilimumab,易普利姆玛)和有限疗程的含铂双药化疗(platinum-doublet chemotherapy),一线治疗不可手术切除的、晚期或复发性非小细胞肺癌(NSCLC)。FDA已授予该sBLA优先审查和快速通道资格,并已指定处方药用户收费法(PDUFA)目标日期为2020年8月6日。
此外,欧洲药品管理局(EMA)也已受理Opdivo与Yervoy联合有限疗程化疗用于治疗上述相同适应症的II类变更申请,并已启动集中审评程序。此前,在2020年3月,小野制药与BMS合作,在日本提交了一份关于Opdivo与Yervoy联合有限疗程化疗一线治疗NSCLC的补充申请。
2020年1月,Opdivo+Yervoy组合一线治疗无EGFR或ALK基因组肿瘤畸变的转移性或复发性非小细胞肺癌(NSCLC)患者的补充生物制品许可申请(sBLA)获美国FDA受理,并正在进行优先审查,处方药用户收费法(PDUFA)目标日期为2020年5月15日。该申请基于III期CheckMate-227研究的第一部分(Part 1)结果。数据显示,与化疗相比,Opdivo+Yervoy组合方案显著延长了总生存期(OS)。
值得一提的是,在欧盟方面,BMS于1月底撤回了这份申请。原因是EMA人用医药产品委员会(CHMP)认为BMS对申请中涉及的临床试验进行了多次方案更改,尽管患者数据具有完整性,但无法对申请进行全面评估。BMS表示对CHMP的意见感到失望,并表示没有计划在欧盟重新提交这一申请。
Opdivo+Yervoy联合有限疗程化疗方案的申请,是基于关键性III期CheckMate-9LA研究的结果。这是一项全球多中心、随机、开放标签研究,有小野制药与百时美施贵宝合作开展,评估了Opdivo+Yervoy+含铂双药化疗(2个周期)联合治疗方案、含铂双药化疗方案一线治疗不可手术切除的、晚期或复发性NSCLC患者,而不考虑PD-L1表达和组织学。研究中,试验组接受Opdivo(360mg,每三周一次,Q3W)+Yervoy(1mg/kg,每六周一次,Q6W)+化疗(2个周期),治疗长达两年,或直至疾病进展或不可接受的毒性。对照组接受化疗(多达4个周期)之后是可选的培美曲赛维持疗法(如果符合条件),治疗直至疾病进展或毒性。主要终点是意向性治疗(ITT)群体中的总生存期(OS),次要终点包括无进展生存期(PFS)、总缓解率(ORR)和根据生物标志物的疗效评估。
2019年10月,BMS宣布,该研究在预先指定的中期分析中达到了优越总生存期(OS)主要终点:与化疗组相比,Opdivo+Yervoy+化疗组OS有显著改善。该研究中,Opdivo联合低剂量Yervoy和2个周期化疗的安全性反映了一线NSCLC中免疫治疗和化疗组分已知的安全性。
BMS胸部癌症开发负责人Sabine Maier医学博士表示:“尽管近年来已取得了治疗进展,但对于全球肺癌患者而言,对额外创新治疗方案仍存在着严重的未满足医疗需求。FDA和EMA对我们申请的受理,对肺癌患者来说是一个重要的里程碑,我们期待着与监管部门合作,尽快为患者带来第一个也是唯一一个双重免疫治疗加有限化疗方案。”
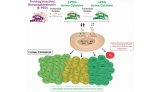
Opdivo是一种程序性死亡-1(PD-1)免疫检查点抑制剂,旨在通过阻断PD-1及其配体之间的相互作用,独特地利用人体自身免疫系统帮助恢复抗肿瘤免疫应答。Opdivo于2014年7月在日本率先获得批准,是全球获批的首款PD-1免疫疗法。目前,Opdivo已成为多种癌症的重要治疗选择。
Opdivo和Yervoy均为肿瘤免疫疗法(I-O),通过靶向免疫系统中不同的调控元件,利用人体自身的免疫系统对抗肿瘤,其中Opdivo靶向阻断PD-1/PD-L1通路,Yervoy则靶向阻断CTLA-4。目前,百时美施贵宝正在开发Opdivo+Yervoy免疫组合用于多种类型肿瘤的治疗。
Opdivo+Yervoy是美国FDA批准的唯一一种双重免疫疗法,该疗法具有潜在的协同作用机制,针对2个不同的免疫检查点(PD-1和CTLA-4),并以互补的方式发挥作用。截至目前,Opdivo+Yervoy组合已获FDA批准用于治疗4种类型的癌症(黑色素瘤、肾细胞癌、结直肠癌、肝细胞癌)。
-
焦点事件

-
焦点事件

-
焦点事件