一例急性淋巴细胞白血病缓解9年后继发非霍奇金淋巴...
一例急性淋巴细胞白血病缓解9年后继发非霍奇金淋巴瘤病例分析
资料
患者,男性,32岁,因无明显诱因下出现双下肢膝关节疼痛于1996年7月到来我院住院治疗。体检:重度贫血貌,皮肤未见出血点,浅表淋巴结未触及,胸骨压痛明显,心率90 次/min,律齐,无病理性杂音,双肺未闻及干湿性啰音,肝脾肋下未及。实验室检查:白细胞1.5x109/L,红细胞2.40x109/L,血红蛋白61 g/L,血小板50x109/L;骨髓穿刺示骨髓增生极度活跃,原幼淋巴细胞占90%;细胞化学染色:原幼稚细胞POX染色阴性;PAS染色87%阳性。
诊断为白血病" target="_blank" title="急性淋巴细胞白血病">急性淋巴细胞白血病(ALL-L2),给予VP(长春新碱+泼尼松)、VDP(长春新碱+柔红霉素+泼尼松)、VDLP(长春新碱+柔红霉素+左旋门冬酰胺酶+泼尼松)化疗后骨髓象提示缓解,继用VDCP(长春新碱+环磷酰胺+柔红霉素+泼尼松)、HDMTX(大剂量氨甲喋呤)方案各3次巩固化疗,出院后定期回院化疗,骨髓象持续缓解状态,于1998年10月停止化疗。
2007年12月,患者因“双侧腹股沟肿块8月”人我院普外科。体检:无贫血貌,皮肤、黏膜无黄染及出血点,双颈部可及数枚黄豆大小、质中、移动、无触痛的淋巴结,双侧腹股沟可及8 cm x 4 cm,3 cm x 6 cm大小,右侧较大,固定、质中、无触痛的淋巴结,余淋巴结未及,胸骨无压痛,腹平软,肝脾肋下未及。实验室检查:白细胞6.4x109/L,血红蛋白147 g/L,血小板140x109/L。淋巴结B超提示:双侧颈部、双侧腋下、双侧腹股沟多发淋巴结肿大,左锁骨上多发实质性团块,右腹股沟实质性团块。腹部B超提示腹腔淋巴结肿大,CT腹膜后盆腔淋巴结肿大,腹腔淋巴结增多,纵隔淋巴结肿大。骨髓涂片检查提示ALL-CR,骨髓活检:骨髓造血细胞轻度增生,三系比例正常,粒系以中晚幼细胞为主,红系以中晚幼细胞多见,巨核细胞2〜3个/HPF,网状纤维染色示网纤维(+),提示骨髓组织轻度增生(图1)。
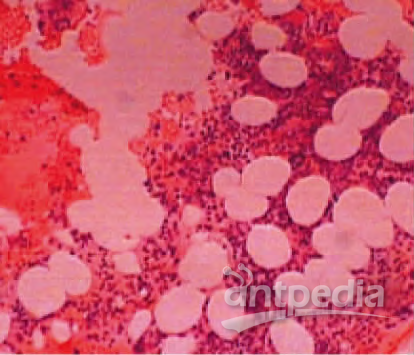
图1
染色体检查正常,左侧腹股沟淋巴结病理活检(图2):“左腹股沟”非霍奇金淋巴瘤">恶性淋巴瘤,滤泡性淋巴瘤,部分为弥漫性。免疫组化:CD20(++)、CD79a(++)、CD10(++)、Bcl-2(+)、CD3(±)、MPO(-)、CD99(+)、CD5(+)、CyclinD1(-)、CD15㈠、CD30(-)、Bcl-6(±)。病毒检测:EB病毒-IgM(+),CMV-IgG(-),HbsAb(+)。乳酸脱氢酶(LDH)182 U/L。
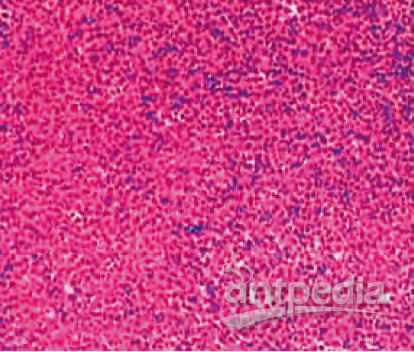
图2
最后诊断:①非霍奇金淋巴瘤" target="_blank" title="非霍奇金淋巴瘤">非霍奇金淋巴瘤(NHL),滤泡性淋巴瘤,部分弥漫性,:ⅢA期;②ALL-CR9年。给予CHOP(环磷酰胺+多柔比星+长春新碱+泼尼松)、ECHOP(依托泊苷+环磷酰胺+多柔比星+长春新碱+泼尼松)方案化疗一共6个疗程,化疗第5个疗程结束后行腹股沟局部放疗(共25Gy),双侧腹股沟、腋下、颈部等肿大的淋巴结完全消失,于2008年9月17日停止化疗出院。
2010年1月于当地医院CT复査显示颈部外侧以及枕后淋巴结肿大,至2010年5月发展至触及枕后及颈部外侧群淋巴结肿大,于2011年3月来我院治疗,经血、骨髓象、胸片、B超等检査结合临床诊断:①NHL复发,滤泡性淋巴瘤,部分弥漫性,MA期;②ALL-CR 12年。
予MINE(异环磷酰胺+美司钠+米托蒽醌+依托泊苷)方案化疗5个疗程后,患者颈部、腋下、腹股沟等肿大淋巴结再次消失,于2011年9月12日停止化疗,至今患者无病生存已3年。
讨论
随着临床上化疗药物大剂量广泛地应用,特别是靶向药物不断地研发应用,肿瘤患者的生存率不断提高,但是,威胁患者生命的最严重的化疗相关副作用之一就是发生继发性肿瘤。本例患者为ALL治疗持续缓解后9年出现了继发性第二肿瘤——NHL,继发性NHL作为继发性肿瘤发生率仅为0.08%,临床上罕见,外文文献报道治疗后发生继发性NHL的发病时间在原发病确诊后3.1〜16.6年。ALL是一种起源于淋巴细胞的B系或T系细胞在骨髓内异常增生的恶性肿瘤性疾病,异常增生的原始细胞可在骨髓内聚集并抑制正常造血功能,表现为贫血、出血、发热感染等,同时可以侵犯到骨髓外的组织,如脑膜、淋巴结、肝脏、脾脏、性腺等。淋巴瘤是起源于淋巴造血系统的恶性肿瘤,白血病继发恶性淋巴瘤的发病机制目前尚未完全清楚。
目前发病机制可能为:①白血病和淋巴瘤存在着共同病因,近年来已证实逆转录病毒为致瘤病毒,可诱发爬行类、灵长类哺乳动物白血病、淋巴瘤及乳腺肿瘤等。
②白血病和淋巴瘤有共同的祖细胞来源。
③细胞遗传学异常。染色体的异常及癌基因的存在使得具有潜在的多能分化作用的多能干细胞发生恶性克隆,在不同时期其病变部位和表现形式不同。染色体的损伤可以激活癌基因诱导复制,产生异常克隆,促使肿瘤的发生。
④白血病患者均有不同程度的免疫缺陷,经过放疗和化疗后,机体免疫系统受到抑制,使得肿瘤细胞的免疫监视作用失控,从而给肿瘤细胞的增殖提供了条件,导致了继发性恶性淋巴瘤的发生。
⑤化学药物等引起的治疗相关性白血病,其作用取决于药物使用剂量、化疗方案、疗程及宿主因素,其中蒽环类药物(如米托蒽醌、阿霉素、表阿霉素等)作用于DNA拓扑异构酶Ⅱ,可以引起治疗相关性血液系统肿瘤,本例患者可能与既往使用蒽环类化疗药物有关。
本例患者ALL缓解9年后发生NHL,国内外报道较少,患者骨髓象正常,可排除髓源性复发,其发病机制是否同以上几种机制有关,还有待进一步研究。




















